氯离子的检验 知识点题库
在未知溶液中加入AgNO3溶液有白色沉淀生成,加入稀硝酸后,沉淀部分溶解,有无色无味气体放出,将气体通入澄清石灰水变浑浊.则水溶液中含有( )
A . Cl﹣、SO42﹣
B . Cl﹣、NO3﹣
C . Cl﹣、CO32﹣
D . Cl﹣、OH﹣
自来水是用氯气杀菌消毒的,不法商贩用自来水冒充纯净水销售,为辨别纯净水真伪,可用下列哪种试剂鉴别( )
A . 酚酞试液
B . 氯化铁溶液
C . 硝酸银溶液
D . 氢氧化钠溶液
某溶液中可能含有 、Cl﹣ , 为了检验其中是否含有Cl﹣ , 需要加入的试剂有( )
、Cl﹣ , 为了检验其中是否含有Cl﹣ , 需要加入的试剂有( )
 、Cl﹣ , 为了检验其中是否含有Cl﹣ , 需要加入的试剂有( )
、Cl﹣ , 为了检验其中是否含有Cl﹣ , 需要加入的试剂有( )
A . NaNO3
B . AgNO3
C . HCl
D . HNO3
氯仿(CHCl3)可作麻醉剂,但常因保存不妥而被氧气氧化,产生剧毒物质光气(COCl2),其化学反应方程式为2CHCl3+O2﹣→2HCl+2COCl2 , 为了防止事故的发生,在使用前需检验氯仿是否变质,应选用的试剂是( )
A . 氢氧化钠溶液
B . 盐酸
C . 硝酸银溶液
D . 水
下列物质中无Cl﹣的是( )
A . KCl溶液
B . KClO3
C . NaCl晶体
D . 氯水
简述实验室检验Cl﹣的方法.
向某溶液中加入BaCl2溶液,再加入稀HNO3至溶液呈酸性,有白色沉淀产生。该溶液一定含有( )
A . CO32―
B . OH―
C . SO42―
D . HCO3―
某白色固体混合物,为了鉴定其成分进行如下实验:
①取少量样品加足量水充分混合,观察到气体产生,反应后仍有部分固体未溶解,过滤;
②滤渣加入足量NaOH溶液,滤渣溶解;
③滤液中加足量稀硝酸酸化,再加几滴AgNO3溶液,产生白色沉淀。该白色粉末可能是()
A . AlCl3和NH4HCO3
B . AlBr3和NaHCO3
C . Ba(OH)2和(NH4)2CO3
D . CaCl2和(NH4)2SO3
下列实验方案可行的是( )
A . 用澄清石灰水检验CO2含有的CO
B . 用经盐酸酸化的AgNO3溶液检验溶液中含有的Cl-
C . 用可见光束照射可区别溶液与胶体
D . 用溶解、过滤的方法分离 CaCl2 和NaCl固体混合物
市场上常有一些不法商贩为牟取暴利,用自来水冒充纯净水(蒸馏水)出售,为辨别真伪,请你选择以下试剂来鉴别,该试剂是( )
A . 酚酞
B . 氯化钡
C . 硝酸银
D . 氢氧化钠
下列有关实验原理、方法和结论都正确的是( )
A . 向某溶液中加入盐酸酸化的氯化钡溶液有白色沉淀生成,该溶液不一定含SO42-
B . 向蛋白质溶液中加入硫酸铜溶液,将得到的沉淀分离出来,再加水可重新溶解
C . 等体积的pH都为3的酸HA和HB分别与足量的Mg反应,HA放出的H2多,说明酸性:HA>HB
D . 在硫酸钡中加入足量饱和Na2CO3溶液,振荡、过滤、洗涤,沉淀中加入盐酸有气体产生,说明Ksp(BaSO4)>Ksp(BaCO3)
某溶液中含有较大量的Cl-、  、OH-等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是( )
、OH-等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是( )
 、OH-等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是( )
、OH-等3种阴离子,如果只取一次该溶液就能够分别将3种阴离子依次检验出来,下列实验操作顺序正确的是( ) ①滴加Mg(NO3)2溶液 ②过滤 ③滴加AgNO3溶液 ④滴加Ba(NO3)2溶液
A . ①②③②④
B . ④②①②③
C . ④②③②①
D . ①②④②③
对废银合金触电材料进行分离回收既节约矿物资源,又可以减少环境污染。某废银合金触电材料含Ag、Cu、Sn等,现欲利用以下工艺流程回收其中的金属资源。
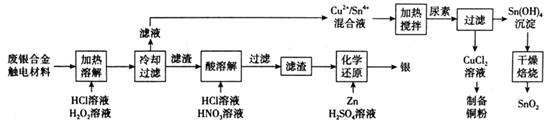
回答下列问题:
-
(1) “加热溶解”时Cu发生的离子方程式为。
-
(2) “加热溶解”时温度常控制在50℃左右,温度不宜过高也不宜过低的原因为。
-
(3) “酸溶解”过程中会产生少量遇空气变为红棕色的无色气体,则“酸溶解”过程主要的化学方程式为。
-
(4) 常温下,Cu2+/Sn4+混合液中c(Cu3+)=0.022mol·L-1 , 将混合液“加热搅拌”后冷却至室温,再加“尿素”调节溶液的pH范围为。(当溶液中的离子浓度小于10-5mol·L-1时,沉淀完全,已知:Ksp[Sn(OH)4]=1×10-55;Ksp[Cu(OH)2]=2.2×10-20)
-
(5) 检验Sn(OH)4沉淀是否洗涤干净的方法是。
-
(6) 用惰性电极电解CuCl2溶液,阴极反应式是,若想由CuCl2溶液得到无水CuCl2固体,则需进行的实验操作为。
为了检验某氯代烃中的氯元素,现进行如下操作,其中合理的是( )
A . 取氯代烃少许,加入AgNO3溶液
B . 取氯代烃少许与NaOH水溶液共热,然后加入AgNO3溶液
C . 取氯代烃少许与NaOH水溶液共热后,加入稀硝酸酸化,再加入AgNO3溶液
D . 取氯代烃少许与NaOH水溶液共热后,加入稀盐酸酸化,再加入AgNO3溶液
下列说法错误的是( )
A . 向某溶液中滴加KSCN溶液,溶液呈血红色,证明存在Fe3+
B . 碳酸钠比碳酸氢钠热稳定性强
C . 漂白粉常作环境消毒剂
D . Cl-和CO  加入硝酸银溶液都有白色沉淀,再加入稀硝酸沉淀都溶解
加入硝酸银溶液都有白色沉淀,再加入稀硝酸沉淀都溶解
 加入硝酸银溶液都有白色沉淀,再加入稀硝酸沉淀都溶解
加入硝酸银溶液都有白色沉淀,再加入稀硝酸沉淀都溶解
有资料显示:过量的氨气和氯气在常温下可合成岩脑砂(主要成分为  ),某兴趣小组对岩脑砂进行如下探究:
),某兴趣小组对岩脑砂进行如下探究:
 ),某兴趣小组对岩脑砂进行如下探究:
),某兴趣小组对岩脑砂进行如下探究:
-
(1) I.岩脑砂的制备
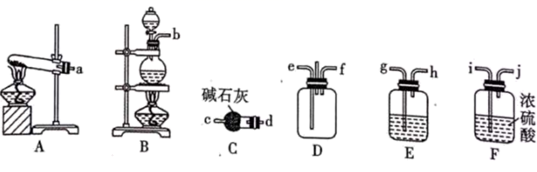
实验室制取氨气的化学反应方程式为。
-
(2) 该实验中用浓盐酸与
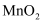 反应制取所需
反应制取所需  ,则装置E中的试剂是。
,则装置E中的试剂是。
-
(3) 为使氨气和氯气在D中充分混合并反应,上述装置的连接顺序为→e、f←(用小写字母和箭头表示,箭头方向与气流方向一致)。
-
(4) 装置D处除导管易堵塞外,还存在的不足之处是。
-
(5) 要证明氨气和氯气反应有岩脑砂生成,所需检验试剂除蒸馏水、稀
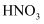 、NaOH溶液外,还需要。
、NaOH溶液外,还需要。
-
(6) II.岩脑砂中元素的测定(杂质不影响
 纯度测定)
纯度测定) 已知:
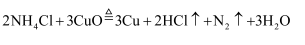
实验步骤:准确称取ag岩脑砂,将其与足量氧化制混合加热(装置如下)。
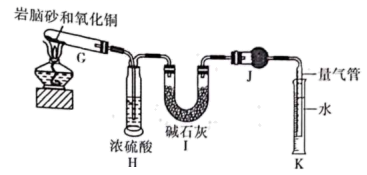
连接好仪器后,检查装置气密性时,先向H和K中装入蒸馏水,然后加热G,若(填实验现象),则气密性良好。
-
(7) 若装置I增重bg,利用装置K测得气体体积为VL(标准状况下),则岩脑砂中
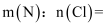 (用含b、V的代数式表示)。
(用含b、V的代数式表示)。
-
(8) 已知装置J中装有碱石灰,若去掉装置J,则
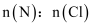 的值会(填“偏大”、“偏小”或“无影响”)。
的值会(填“偏大”、“偏小”或“无影响”)。
下列“实验结论”与“实验操作及现象”不相符的一组是( )
实验操作及现象 | 实验结论 | |
A | 向紫色石蕊溶液中滴加氯水,溶液先变红后褪色 | 氯水具有酸性和漂白性 |
B | 向某溶液中滴加AgNO3溶液,产生白色沉淀 | 该溶液中一定含有Cl- |
C | 向Al(OH)3沉淀中滴加NaOH溶液,沉淀溶解 | 铝元素表现出一定的非金属性 |
D | 把绿豆大的Na和K分别投入水中,K与水反应更剧烈 | 金属性:Na<K |
A . A
B . B
C . C
D . D
下列说法正确的是( )
A . 向某溶液中加入稀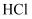 产生能使澄清石灰水变浑浊的无色气体,则溶液中一定含有
产生能使澄清石灰水变浑浊的无色气体,则溶液中一定含有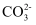 B . 向某溶液中加入
B . 向某溶液中加入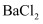 溶液,产生白色沉淀,则溶液中一定含有
溶液,产生白色沉淀,则溶液中一定含有 C . 向某溶液中依次加入
C . 向某溶液中依次加入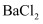 溶液、
溶液、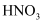 溶液,有白色沉淀产生,则溶液中一定含有
溶液,有白色沉淀产生,则溶液中一定含有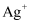 D . 向某溶液中加入
D . 向某溶液中加入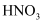 酸化的
酸化的 液,有白色沉淀产生,则溶液中一定含有
液,有白色沉淀产生,则溶液中一定含有
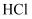 产生能使澄清石灰水变浑浊的无色气体,则溶液中一定含有
产生能使澄清石灰水变浑浊的无色气体,则溶液中一定含有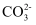 B . 向某溶液中加入
B . 向某溶液中加入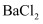 溶液,产生白色沉淀,则溶液中一定含有
溶液,产生白色沉淀,则溶液中一定含有 C . 向某溶液中依次加入
C . 向某溶液中依次加入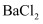 溶液、
溶液、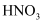 溶液,有白色沉淀产生,则溶液中一定含有
溶液,有白色沉淀产生,则溶液中一定含有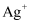 D . 向某溶液中加入
D . 向某溶液中加入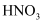 酸化的
酸化的 液,有白色沉淀产生,则溶液中一定含有
液,有白色沉淀产生,则溶液中一定含有
下列检验Cl-的方法正确的是( )
A . 向某溶液中滴加AgNO3溶液,若产生白色沉淀说明该溶液中有Cl-
B . 向某溶液中先滴加盐酸,再滴加AgNO3溶液,若产生白色沉淀,说明溶液中有Cl
C . 向某溶液中先滴加AgNO3溶液,产生白色沉淀,再滴加盐酸,沉淀不消失,说明溶液中有Cl-
D . 向某溶液中滴加用HNO3酸化的AgNO3溶液,若产生白色沉淀,说明溶液中有Cl
一包固体粉末可能含有Na+、K+、Fe3+、Cl-、NO 、SO
、SO 、HCO
、HCO 中的若干种,小明同学为探究该固体成分,进行如图实验:
中的若干种,小明同学为探究该固体成分,进行如图实验:
 、SO
、SO 、HCO
、HCO 中的若干种,小明同学为探究该固体成分,进行如图实验:
中的若干种,小明同学为探究该固体成分,进行如图实验:
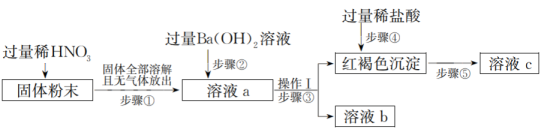
回答下列问题:
-
(1) 由步骤①可推知该粉末中一定不存在的离子为(填离子符号,下同),步骤②中涉及的离子方程式为。
-
(2) 操作I的名称为,根据步骤③、步骤⑤的现象可确定该粉末中一定不存在的离子为,步骤④中发生反应的离子方程式为。
-
(3) 检验固体粉末中是否含Cl-的具体操作为。
最近更新



