铵盐 知识点题库
下列用品的主要成分及用途对应不正确的是( )


-
(1) B点的沉淀物的化学式为。
-
(2) 原溶液中Cu2+的物质的量为,原溶液中Cl-物质的量浓度为。
-
(3) 原溶液的pH=,x-y= 。
-
(4) 经过滤得到D点的沉淀物,并多次用蒸馏水洗涤沉淀,判断沉淀是否洗涤干净的方法是
-
(1) 科学家研究利用某种催化剂,成功实现将空气中的碳氧化合物和氮氧化合物转化为无毒的大气循环物质。已知:
①N2(g)+O2(g)
 2NO(g) △H1=+179.5 kJ·mol-1
2NO(g) △H1=+179.5 kJ·mol-1②NO2(g)+CO(g)
 NO(g)+CO2(g) △H2=-234 kJ·mol-1
NO(g)+CO2(g) △H2=-234 kJ·mol-1③2NO(g)+O2(g)
 2NO2(g) △H3=-112.3 kJ·mol-1
2NO2(g) △H3=-112.3 kJ·mol-1则反应2NO(g)+2CO(g)
 N2(g)+2CO2(g)的△H=kJ·mol-1;某温度下,反应①②③的平衡常数分别为K1、K2、K3 , 则该反应的K=用K1、K2、K3表示)
N2(g)+2CO2(g)的△H=kJ·mol-1;某温度下,反应①②③的平衡常数分别为K1、K2、K3 , 则该反应的K=用K1、K2、K3表示) -
(2) 用活化后的V2O5作催化剂,氨气将NO还原成N2的一种反应历程如图所示

①写出总反应化学方程式。
②测得该反应的平衡常数与温度的关系为:1gK=5.08+217.5/T,该反应是反应(填“吸热”或“放热”)。
③该反应的含氮气体浓度随温度变化如图所示,则将NO转化为N2的最佳温度为;当温度达到700K时,发生副反应的化学方程式。

-
(3) 利用氨水吸收工业废气中的SO2 , 既可解决环境问题,又可制备(NH4)2SO3。可用(NH4)2SO3为原料,以空气氧化法制备(NH4)2SO4 , 其氧化速率与温度关系如下图:
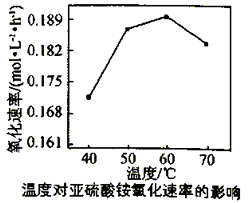
试解释在温度较高时,(NH4)2SO3 氧化速率下降的原因是;相同条件下,等浓度的(NH4)2SO3和(NH4)2SO4溶液中,c(NH4+)前者(填“大”小”)


-
(1) 操作①盛放药品的仪器名称是,发生反应的化学反应方程式为。
-
(2) 进行操作②后,如何判断杂质是否除尽?。
-
(3) 操作③的目的是。
-
(4) 请你评价该设计方案设计是否严密?若不严密,请说明理由,并提出改进方案。
-
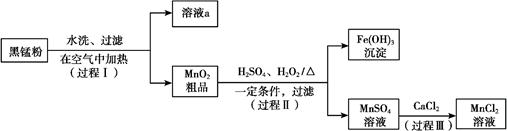
(1) 过程Ⅰ,在空气中加热黑锰粉的目的是除炭、氧化MnO(OH)等。
O2氧化MnO(OH)的化学方程式是。
-
(2) 溶液a的主要成分为NH4Cl,另外还含有少量ZnCl2等。
① 溶液a呈酸性,原因是。
② 根据下图所示的溶解度曲线,将溶液a (填操作名称),可得NH4Cl粗品。

③ 提纯NH4Cl粗品,有关性质数据如下:
化合物
ZnCl2
NH4Cl
熔点
365℃
337.8℃分解
沸点
732℃
根据上表,设计方案提纯NH4Cl:
-
(3) 检验MnSO4溶液中是否含有Fe3+:取少量溶液,加入(填试剂和现象),证明溶液中Fe3+沉淀完全。
-
(4) 探究过程Ⅱ中MnO2溶解的适宜条件。
ⅰ.向MnO2中加入H2O2溶液,产生大量气泡;再加入稀H2SO4 , 固体未明显溶解。
ⅱ.向MnO2中加入稀H2SO4 , 固体未溶解;再加入H2O2溶液,产生大量气泡,固体完全溶解。
① 用化学方程式表示ⅱ中MnO2溶解的原因:。
② 解释试剂加入顺序不同,MnO2作用不同的原因:
上述实验说明,试剂加入顺序不同,物质体现的性质可能不同,产物也可能不同。
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 蘸有浓氨水的玻璃棒靠近溶液X | 有白烟产生 | 溶液X一定是浓盐酸 |
| B | 用玻璃棒蘸取溶液Y进行焰色反应实验 | 火焰呈黄色 | 溶液Y中一定含Na+ |
| C | 向Fe(NO3)2溶液中滴加硫酸酸化的H2O2溶液 | 溶液变黄 | 氧化性:H2O2>Fe3+ |
| D | 用煮沸过的蒸馏水将Na2SO3固体样品溶解,加稀盐酸酸化,再加入氯化钡溶液 | 有白色沉淀产生 | Na2SO3样品中含有SO42- |
-
(1) 工业合成氨是制取氮肥的基础。合成氨反应中,反应物 N2 的结构式是,产物NH3 的电子式是。
-
(2) 某小组在实验室模拟以 NH3 为原料, 制备少量硝态氮肥 Ca(NO3)2 , 转化途径如下(转化所需试剂及条件已略去)。
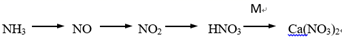
①NO→NO2 的现象是, NO2→HNO3 的化学方程式为。
②将HNO3 转化为 Ca(NO3)2 , 列举两种不同类别的化合物 M(写化学式) 。
-
(3) ①NH4HCO3 是一种铵态氮肥,需阴凉处保存,原因是(写化学方程式)。
②实验室检验某化肥是铵态氮肥,检验过程中发生反应的离子方程式为。
-
(4) 过渡施用氮肥将导致大气中NH3含量增高,加剧雾霾的形成。(NH4)2SO4是雾霾的成分之一,其形成过程如下图所示(转化所需试剂及条件已略去)
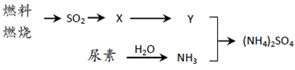
①X可能是SO3 或,Y是。
②尿素CO(NH2)2是一种常用有机氮肥,缓慢与 H2O 发生非氧化还原反应释放出NH3和另外一种气体,该反应的化学方程式为。
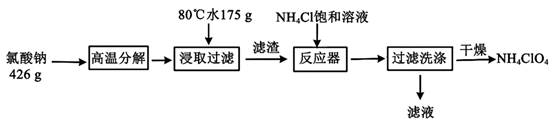
已知:氯酸钠受热分解生成高氯酸钠和氯化钠。
-
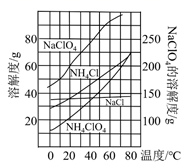
(1) 根据如下溶解度与温度的关系图像推测,80℃时浸取液冷却至0℃过滤,滤渣的主要成分为(写化学式)。反应器中加入氯化铵饱和溶液,然后加热并搅拌使其充分反应,反应的化学方程式为。若氯化铵用氨气和浓盐酸代替上述反应,则无需加热反应就能进行,其原因是。
-
(2) 反应得到的混合液中NH4ClO4和NaCl的质量分数分别为0.40和0.20。根据溶解度与温度的关系图像,从混合溶液中获得较多NH4ClO4晶体的实验操作依次为、(均填实验操作名称)、过滤、冷水洗涤、干燥,冷水洗涤的作用是。
-
(3) 已知NH4ClO4在400℃时开始分解,某课题组设计实验探究NH4ClO4的分解产物(假设装置内的药品均足量)。甲同学设计如图实验(部分夹持装置已省略):
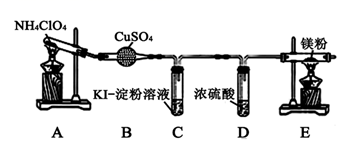
①若高氯酸铵分解有氯气生成,则可能观察到C中的现象是,写出产生该现象的离子方程式。
②通过查阅资料:NH4ClO4在加热分解时还产生了一种使带火星木条复燃的气体。写出高氯酸铵分解的化学方程式。实验完毕后,取出E处硬质玻璃管中固体于试管中,滴加蒸馏水,产生的气体R能使湿润的红色石蕊试纸变蓝,R的电子式为。

①农业生产中常使用的氮肥都是易溶于水的;②生产中使用的尿素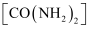 不属于有机物;③铵态氮肥可以与草木灰混合施用;④铵态氮肥在使用时宜深施盖土,避免受热;
不属于有机物;③铵态氮肥可以与草木灰混合施用;④铵态氮肥在使用时宜深施盖土,避免受热;



