合理利用金属资源 知识点题库
下列叙述正确的是 ( )
A . 推广使用太阳能、风能、海洋能、氢能,有利于缓解温室效应
B . 乙醇和汽油都是可再生能源,应大力推广“乙醇汽油”
C . 废电池需回收,主要是要利用电池外壳的金属材料
D . 升高温度可降低活化能
化学与科学.技术.社会.环境和生活密切相关.下列有关说法中不正确的是( )
A . 钢铁在海水中比在河水中更易腐蚀,主要原因是海水含氧量高于河水
B . 废弃的塑料.金属.纸制品及玻璃都是可回收再利用的资源
C . 食品添加剂的使用可改善食品品质.延长食品保质期、增加食品营养成分,但必须严格遵守卫生部门的规定
D . 在燃煤发电过程中有如下能量变化:化学能→热能→机械能→电能
镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、碳粉、氧化铁等涂覆在铝箔上制成.由于电池使用后电极材料对环境有危害.某兴趣小组对该电池电极材料进行资源回收研究,设计实验流程如下:
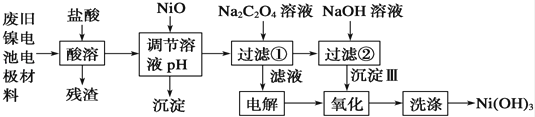
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+ . ②Ksp(Ni(OH)2):5.0×10﹣16 Ksp(NiC2O4):4.0×10﹣10
回答下列问题:
(1)酸溶后所留残渣的主要成分 (填物质名称).
(2)用NiO调节溶液的pH,析出沉淀的成分为 (填化学式);用pH试纸测定某溶液pH的具体操作是 .
(3)写出加入Na2C2O4溶液后反应的化学方程式 .
(4)写出加入NaOH溶液所发生反应的离子方程式 ,该反应的平衡常数为 .
(5)沉淀Ⅲ可被电解所得产物之一 (填化学式)氧化生成Ni(OH)3 , 如何洗涤Ni(OH)3沉淀? .
某工业矿渣中主要含有Cu2O,还有少部分Al2O3、Fe2O3、SiO2 , 从该矿渣中提取铜的操作流程如下:(已知:Cu2O+2H+═Cu+Cu2++H2O)

-
(1) 固体混合物B与氢氧化钠溶液反应的化学方程式为.该反应物的一种重要用途为.
-
(2) 滤液A中铁元素的存在形式只能为Fe2+ , 理由是.涉及的离子方程式为(不必书写Cu2O与盐酸的反应)、.检验滤液A中Fe2+的试剂为.
-
(3) 若将滤液C中的铝元素以沉淀形式析出,可选用的最佳试剂为(填序号).
A.氢氧化钠溶液 B.硫酸溶液 C.氨水 D.二氧化碳
金属E与固体F某一成分发生的反应可用于焊接钢轨,该反应的化学方程为.
某厂的酸性工业废水中含有一定量的Fe3+、Cu2+、Au3+等离子,有人设计了图中的工艺流程,从废水中回收金,并生产一定量的铁红和氧化铜(图中标号处只利用工业生产中的常用的酸、碱和废铁屑).

-
(1) 图中标号处需加入的相应物质分别是①、②、③、④、⑤;
-
(2) 写出①处所有可能发生的离子方程式
-
(3) 写出③处发生反应的化学方程式;
-
(4) 铁红的化学式为;写出铁红在工业上的一种主要用途.
从铝土矿(主要成分是Al2O3 , 含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如下:

请回答下列问题:
-
(1) 流程甲加入盐酸后生成Al3+的离子方程式为.
-
(2) 流程乙加入烧碱后生成SiO32﹣的离子方程式为.
-
(3) 验证滤液B含Fe3+ , 可取少量滤液并加入(填试剂名称).
-
(4) 滤液D产生沉淀F的离子方程式为.
-
(5) 滤液E、K中溶质的主要成分是(填化学式),写出该溶质的一种用途
如图为某工厂处理含Fe3+、Cu2+、Ag+废水的流程图:

据图回答下列问题:
-
(1) 操作①中发生反应的离子方程式为.
-
(2) 操作②中H2O2起了(填“氧化”或“还原”)的作用.
-
(3) 操作③中产生的沉淀为(填化学式).
-
(4) 操作④中通入的X气体为(填化学式).
将金属钙置于空气中充分燃烧,然后向所得固体产物中加入一定量蒸馏水,观察到剧烈反应,产生大量的热,并且放出有臭味的气体。对此,化学兴趣小组的同学们在老师的指导下进行了探究。
【査阅资料】①Mg在氮气中燃烧生成氮化镁(Mg3N2),氮化镁与水发生复分解反应,有NH3生成。
②CaO2遇水反应生成H2O2 , H2O2会分解产生一定量的O3。
③碘量法是最常用的臭氧测定方法,其原理为:O3+2KI+H2O=O2+I2+2K0H
【査阅资料】①Mg在氮气中燃烧生成氮化镁(Mg3N2),氮化镁与水发生复分解反应,有NH3生成。
②CaO2遇水反应生成H2O2 , H2O2会分解产生一定量的O3。
③碘量法是最常用的臭氧测定方法,其原理为:O3+2KI+H2O=O2+I2+2K0H
-
(1) 甲同学提出:运用类比学习的思想,Ca与Mg是同一主族元素,化学性质具有一定的相似性,因此可以推断Ca在空气燃烧时,能与空气中的氮气反应生成。
-
(2) 乙同学提出:Ca的性质比Na活泼,在空气中燃烧也有CaO2生成,其化学方程式为:。
-
(3) 丙同学对臭味气体的成分提出三种假设。
【提出假设】假设1:产生臭味的气体只是O3;
假设2:产生臭味的气体只是;
假设3:产生臭味的气体是。
-
(4) 【实验探究】为此,同学们对臭味气体的成分进行了实验探究。实验室提供的实验试剂有:红色石蕊试纸、蓝色石蕊试纸、淀粉-KI试纸、蒸馏水。
请按下列表格填写完成实验操作、与结论相应的预期现象:
实验操作
预期现象
结论
取少量钙在空气中充分燃烧后的 固体产物于试管中,加少量蒸熘水,分别用、在短时间内快速检测产生的气体。
假设1成立
假设2成立
假设3成立
最近更新



