离子方程式的书写 知识点题库
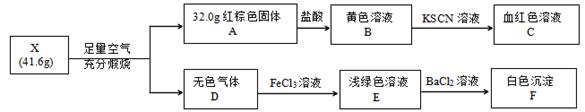
请回答:
-
(1) X含有的两种元素是,其化学式是。
-
(2) 无色气体D与氯化铁溶液反应的离子方程式是。
-
(3) 已知化合物X能与稀盐酸反应,生成一种淡黄色不溶物和一种气体(标况下的密度为1.518 g·L-1),写出该反应的化学方程式。
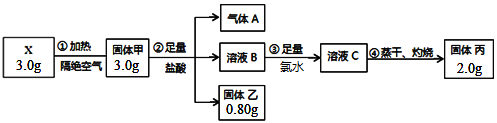
固体乙是一种单质,固体丙呈红棕色,将气体A通入溶液C中也能生成固体乙。
请回答:
-
(1) X的化学式是,步骤①的化学方程式是。
-
(2) 气体A通入溶液C发生反应的离子方程式是。
了以下两种方案。请你帮助他们完成有关实验项目:
方案Ⅰ:有人提出将大小相等的铁片和铜片,分别同时放入稀硫酸(或稀盐酸)中,观察产生气泡的快慢,据此确定它们的活动性。该原理的离子方程式为
方案Ⅱ:有人利用Fe、Cu作电极设计成原电池,以确定它们的活动性。试在下面的方框内画出原电池装置图,标出原电池的电极材料和电解质溶液,并写出电极反应式。

正极反应式:。
负极反应式:。
方案Ⅲ:结合你所学的知识,帮助他们再设计一个验证Fe、Cu活动性的简单实验方案(与方案Ⅰ、Ⅱ不能雷同):,用离子方程式表示其反应原理:。

已知1:生成氢氧化物沉淀的pH
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)2 | 7.6 | 9.6 |
| Fe(OH)3 | 2.7 | 3.7 |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
已知2:几种难溶电解质的溶解度(20℃)
| 物质 | 溶解度/g |
| Fe(OH)2 | 5.2×10-5 |
| Fe(OH)3 | 3×10-9 |
| MgCO3 | 3.9×10-2 |
| Mg(OH)2 | 9×10-4 |
(已知:Fe2+氢氧化物呈絮状,不易从溶液中除去)
请回答:
-
(1) 步骤Ⅱ中加入的试剂X为漂液(含25.2%NaClO)。
①用玻璃棒蘸取漂液滴在pH试纸上,pH试纸先变蓝,后褪色。说明漂液具有的性质是。
②用化学用语表示NaClO溶液使pH试纸变蓝的原因。
③步骤Ⅱ中漂液的主要作用是。
④若用H2O2代替漂液,发生反应的离子方程式为。
-
(2) 步骤Ⅲ中加入的试剂Y为NaOH,应将溶液的pH调节为,目的是。
-
(3) 步骤Ⅳ中加入的试剂Z为Na2CO3 , 发生反应的离子方程式为。
-
(4) 结合化学用语,应用化学平衡移动原理解释步骤Ⅴ中反应发生的原因。
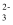 +2H+=CO2↑+H2O
C . 用惰性电极电解MgCl2溶液:2Cl-+2H2O
+2H+=CO2↑+H2O
C . 用惰性电极电解MgCl2溶液:2Cl-+2H2O  +Fe2++8H+=Mn2++Fe3++4H2O
+Fe2++8H+=Mn2++Fe3++4H2O
-
(1) 能导电的是;
-
(2) 属于非电解质的是 ;
-
(3) 既不属于电解质也不属于非电解质的是 ;
-
(4) 写出上述物质中②和⑤反应的离子方程式
-
(5) 写出上述物质中⑤和Ba(OH)2反应的离子方程式
选项 | 离子方程式 | 评价 |
A | 将2mol Cl2通入到含1mol FeI2的溶液中:2Fe2++2I−+2Cl2=2Fe3++4Cl−+I2 | 正确:Cl2过量,可将Fe2+、I−均氧化 |
B | Ba(HCO3)2溶液与足量的NaOH溶液反应:Ba2++HCO-+OH−=BaCO3↓+H2O | 正确:酸式盐与碱反应生成正盐和水 |
C | 过量SO2通入到NaClO溶液中:SO2+H2O+ClO−=HClO+HSO3- | 正确:说明酸性: H2SO3强于HClO |
D | 1mol/L的NaAlO2溶液和2.5mol/L的HCl 溶液等体积互相均匀混合: 2AlO-+5H+=Al3++Al(OH)3↓+H2O | 正确:AlO-与 H+均无剩余 |
|
产品标准 |
GB5461 |
|
产品等级 |
一级 |
|
配料 |
食盐、碘酸钾、抗结剂 |
|
碘含量(以1计) |
20~50mg/kg |
|
分装时期 |
|
|
分装企业 |
-
(1) 碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处)
KlO3+KI+H2SO4=K2SO4+I2+H2O
-
(2) 上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应的离子方程式是 。
②某学生设计回收四氯化碳的操作步骤为:
a.将碘的四氯化碳溶液置于分液漏斗中;
b.加入适量Na2SO3稀溶液;
c.分离出下层液体。
以上设计中遗漏的操作及在上述步骤中的位置是。
-
(3) 已知:I2+2S2O32-=2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取wg食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液10.0mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是。
②b中反应所产生的I2的物质的量是mol。
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示)mg/kg。
-
(1) ①写出2-甲基丁烷的结构简式: ②写出小苏打的化学式:
-
(2) 写出铜与氯化铁溶液反应的离子方程式:
-
(3) 铁片、铜片链接后浸入稀硫酸形成原电池,正极反应式是
-
(4) 写出苯和液溴在催化剂作用下生成溴苯的化学方程式
-
(5) 已知0.25mol N2H4(g)完全燃烧生成氮气和气态水时放出133.5KJ热量。写出该反应的燃烧热化学方程式
 =BaSO4↓
C . 将铜丝插入AgNO3溶液中:Cu+2Ag+=Cu2++2Ag
D . 将氧化镁与稀盐酸混合:O2-+2H+=H2O
=BaSO4↓
C . 将铜丝插入AgNO3溶液中:Cu+2Ag+=Cu2++2Ag
D . 将氧化镁与稀盐酸混合:O2-+2H+=H2O
-
(1) 大理石与盐酸反应
-
(2) 二氧化碳通入足量澄清石灰水中
-
(3) 小苏打(NaHCO3)与盐酸反应
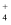 +OH-
+OH-  NH3↑+H2O
B . NaOH与NH4Cl溶液混合加热:NH
NH3↑+H2O
B . NaOH与NH4Cl溶液混合加热:NH 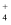 +OH-=NH3·H2O
C . 氨水加入盐酸中:NH3·H2O+H+=NH
+OH-=NH3·H2O
C . 氨水加入盐酸中:NH3·H2O+H+=NH 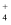 +H2O
D . 氨水加入稀H2SO4中:NH3+H+=NH
+H2O
D . 氨水加入稀H2SO4中:NH3+H+=NH 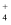
 +H+=CO2↑+H2O
C . 向溴化亚铁溶液中通入足量氯气:2Br-+Cl2=Br2+2Cl-
D . 向澄清石灰水中通入过量二氧化碳:Ca2++2OH-+CO2=CaCO3↓+H2O
+H+=CO2↑+H2O
C . 向溴化亚铁溶液中通入足量氯气:2Br-+Cl2=Br2+2Cl-
D . 向澄清石灰水中通入过量二氧化碳:Ca2++2OH-+CO2=CaCO3↓+H2O



