氯气的物理性质 知识点题库
实验室模拟合成氨和氨催化氧化的流程如下,气体混合的装置如图甲所示,合成氨的装置如图乙所示,氨吸收和氨氧化的装置如图丙所示.

(1)已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气.则制取氮气的装置为 (从图A、B、C中选择,下同),制取氢气的装置为 .
(2)甲装置的作用除了使气体充分混合外,还有① 、② .
(3)乙装置发生反应的化学方程式为 .其中催化剂为Fe粉,它能否用Fe2O3代替? .说明理由 .
(4)丙装置吸收一段时间氨气后,再通入空气,同时将经加热的铂丝插入到锥形瓶内,可观察到:有红棕色气体和白烟生成,请用化学方程式说明催化氧化后,产生以上现象的原因: ; , .
①新制氯水久置后→浅黄绿色消失
②淀粉溶液遇单质碘→蓝色
③蔗糖中加入浓硫酸搅拌→白色
④SO2通入品红溶液中→红色褪去
⑤氨气通入酚酞溶液中→红色.

实验操作和现象:
操作 | 现象 |
点燃酒精灯,加热 | i.A中部分固体溶解,上方出现白雾 ii.稍后,产生黄色气体,管壁附着黄色液滴 iii.B中溶液变蓝 |
-
(1) 现象i中的白雾是,形成白雾的原因是。
-
(2) 分析现象ii,该小组探究黄色气体的成分,实验如下:
a.直接加热FeCl3·6H2O,产生白雾和黄色气体。
b.将现象ii和a中的黄色气体通入KSCN溶液,溶液均变红。
通过该实验说明现象ii中黄色气体含有。
-
(3) 除了氯气可使B中溶液变蓝外,该小组还提出其他两种可能的原因:
原因①:实验b检出的气体使之变蓝,反应的离子方程式是。
原因②:在酸性条件下,装置中的空气使之变蓝,反应的离子方程式是。
-
(4) 为进一步确认黄色气体中是否含有Cl2 , 小组提出两种方案,均证实了Cl2的存在。
方案1
在A、B间增加盛有某种试剂的洗气瓶C
B中溶液变为蓝色
方案2
将B中KI-淀粉溶液替换为NaBr溶液;检验Fe2+
B中溶液呈浅橙红色;未检出Fe2+
①方案1的C中盛放的试荆是。
②方案2中检验Fe2+的试剂是。
③综合方案1、2的现象,说明方案2中选择NaBr溶液的依据是。
-
(5) 将A中产物分离得到Fe2O3和MnCl2 , A中产生Cl2的化学方程式是。
-
(1) 若发生大量氯气泄漏事故,下列措施中正确的是。
a. 立即通报相关部门,迅速撤离事故现场
b. 用蘸有NaOH溶液的毛巾捂住口鼻
c. 逆风疏散
d. 顺风疏散
-
(2) 事故发生后,可用NaOH稀溶液处理泄漏的氯气,反应的离子方程式是。
-
(3) 某学生用下图装置制备氯气并与潮湿的
 反应制取少量漂白粉(这是一个放热反应),据此回答下列问题:
反应制取少量漂白粉(这是一个放热反应),据此回答下列问题: 
①圆底烧瓶中发生反应的化学方程式是。
②此实验结果所得
 产率太低。经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:
产率太低。经分析并查阅资料发现,主要原因是在U形管中存在两个副反应:i温度较高时氯气与
 反应生成
反应生成  ,为避免此副反应的发生,可采取的措施是。
,为避免此副反应的发生,可采取的措施是。ii试判断另一个副反应(写出此反应方程式):。为避免此副反应发生,应采取的措施是。
-
(4) 在一定量的NaOH溶液中通入一定量
 ,二者恰好完全反应。生成物中含有
,二者恰好完全反应。生成物中含有 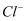 、
、  、
、  三种含氯元素的离子,其中
三种含氯元素的离子,其中  、
、  两种离子的物质的量(n)与反应时间(t)的曲线如下图所示。则
两种离子的物质的量(n)与反应时间(t)的曲线如下图所示。则  时被氧化的氯元素和被还原的氯元素质量之比为。
时被氧化的氯元素和被还原的氯元素质量之比为。 
| 选项 | 实验现象 | 解释 |
| A | Cl2使鲜艳的红色花瓣褪色 | Cl2具有强还原性 |
| B | NH3与HCl气体接触时有白烟产生 | NH3与HCl反应生成固体小颗粒 |
| C | 新切开的Na表面在空气中很快变暗 | Na容易与空气中的氧气等反应 |
| D | 氯化铝溶液中滴入过量的氢氧化钠溶液,白色沉淀溶解 | 氢氧化铝具有两性 |

①可用于氯气的收集 ②若气球干瘪,证明Cl2可与NaOH反应 ③可证明氯气具有漂白性 ④可用于实验室中氯气的尾气吸收
 制备Cl2
B .
制备Cl2
B .  收集Cl2
C .
收集Cl2
C .  验证Cl2具有氧化性
D .
验证Cl2具有氧化性
D .  吸收Cl2尾气
吸收Cl2尾气
 氧化性强,稳定性好,常用于杀菌消毒
C . 氯水呈酸性,可用
氧化性强,稳定性好,常用于杀菌消毒
C . 氯水呈酸性,可用  试纸准确测得其
试纸准确测得其  D . 溶液中加入
D . 溶液中加入  溶液有白色沉淀生成,则原溶液中一定有
溶液有白色沉淀生成,则原溶液中一定有 

关于I、II、III步溶液中导致变色的微粒的对应判断,正确的是( )

选项 | 实验操作、现象 | 结论 |
A | 将湿润的有色布条放入充满氯气的集气瓶中,布条褪色 | 氯气具有漂白性 |
B | 向次氯酸钙溶液中通入过量CO2气体,无沉淀产生 | 酸性:HClO> H2CO3 |
C | 盛有氯气的试管倒扣在水槽中,静置一段时间后,试管中液面上升一段距离 | 氯气能溶于水 |
D | 用小刀切割金属钠,钠表面光亮的银白色迅速变暗 | 金属钠质软,易与水反应生成NaOH |



