高一化学试题
下列各组粒子中,互为同位素的是( )
A . 1224Mg和1124Na
B . O2和O3
C . 11H2和12H2
D . 1735Cl和1737Cl
BaCl2•xH2O中结晶水数目可通过重量法来确定:
①称取1.222g样品,置于小烧杯中,加入适量稀盐酸,加热溶解,边搅拌边滴加稀硫酸到沉淀完全,静置;
②过滤并洗涤沉淀;
③将盛有沉淀的滤纸包烘干并中温灼烧;转入高温炉中,反复灼烧到恒重,称得沉淀质量为1.165g.
回答下列问题:
-
(1) 在操作②中,需要先后用稀硫酸和洗涤沉淀;检验沉淀中氯离子是否洗净的方法是.
-
(2) 计算BaCl2•xH2O中的x=;(要求写出计算过程).
-
(3) 操作③中,如果空气不充足和温度过高,可能会有部分沉淀被滤纸中的碳还原为BaS,这使x的测定结果(填“偏低”、“偏高”或“不变”).
三氯异氰尿酸是一种极强的氧化剂和氯化剂,利用氰尿酸(如图1)与次氯酸在一定pH下反应可制备三氯异氰尿酸(如图2),若原料完全反应生成三氯异氰尿酸.则氰尿酸和次氯酸的物质的量之比应为( )
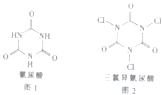
A . 1:1
B . 2:3
C . 1:2
D . 1:3
在托盘天平的两盘中各放入一个质量相等的烧杯,两烧杯中各盛有100mL1mol/L 硫酸溶液,向两烧杯中分别加入各组中的两种物质,反应后天平保持平衡的是( )
A . 0.1mol Zn,0.1mol Fe
B . 1mol Fe,1mol Zn
C . 1g Zn,1g Fe
D . 10g Zn,10g Fe
根据化肥尿素CO(NH2)2的化学式,计算:
(1)尿素的相对分子质量 .
(2)一个CO(NH2)2分子中的质子数是 ;
(3)元素质量比:C:O:N:H= ;
(4)100kg尿素中含氮元素的质量 (保留一位小数).
用等体积的0.15mol L﹣1的BaCl2溶液,可使相同体积的Na2SO4、Fe2(SO4)3、KAl(SO4)2三种溶液中的SO42﹣完全沉淀,则三种硫酸盐的物质的量浓度之比为.
等质量的铝分别投入等物质的量浓度等体积的盐酸和氢氧化钠溶液中,充分反应后下列情况不可能出现的是( )
A . 金属铝均剩余
B . 金属铝均溶解
C . 盐酸中铝剩余,而氢氧化钠中铝全部溶解
D . 氢氧化钠这铝剩余,而盐酸中铝全部溶解
我国自主研发的5G通信芯片主要原料是氮化镓,下图是氮元素在元素周期表中的部分信息及镓(Ga)原子的结构示意图。下列说法错误的是( )
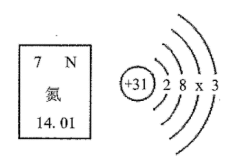
A . x=18
B . 氮化镓的化学式为GaN
C . 镓元素位于第四周期第三主族
D . 氮原子核电荷数为7,氮元素的相对原子质量为14.01
如图是某元素的原子结构示意图,下列说法正确是( )
![]()
A . 该原子的核外电子数是16
B . 该原子在化学反应中容易失去6个电子
C . 该元素属于非金属元素.不能与氧元素形成化合物
D . 该原子的电子层数为6
下列各组物质中互为同位素的是( )
A . 2040Ca和1840Ar
B . H2O和H2O2
C . D和T
D . O3和O2
某粒子的结构示意图为 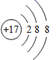 ,关于该粒子的说法错误的是( )
,关于该粒子的说法错误的是( )
 ,关于该粒子的说法错误的是( )
,关于该粒子的说法错误的是( )
A . 核电荷数为17
B . 核外有3个电子层
C . 属于非金属元素的离子
D . 在化学反应中容易得到1个电子
密闭容器中盛有一定量的CH4与O2混合气体及足量的Na2O2固体,电火花点燃充分反应后,恢复至室温,发现容器为真空,则原混合气中CH4与O2的体积比为( )
A . 2:1
B . 1:2
C . 1:1
D . 任意比
诺贝尔化学奖得主Gerhard Ertl对金属Pt(78号元素)表面催化CO氧化反应的模型进行了深入研究。下列关于202Pt和198Pt的说法正确的是( )
A . 202 Pt和198Pt的质子数相同,互称为同位素
B . 202 Pt和198Pt的中子数相同,互称为同位素
C . 202Pt和198Pt的核外电子数相同,是同一种核素
D . 202 Pt和198Pt的质量数不同,不能互称为同位素
下列各组微粒中,互为同位素的是( )
A .  和
和  B .
B . 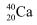 和
和  C .
C .  和
和  D .
D .  和
和 
 和
和  B .
B . 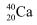 和
和  C .
C .  和
和  D .
D .  和
和 
许多元素有多种核素,如氧元素存在 、
、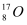 、
、 三种核素,氢元素有
三种核素,氢元素有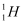 、
、 、
、 三种核素。下列说法正确的是( )
三种核素。下列说法正确的是( )
 、
、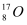 、
、 三种核素,氢元素有
三种核素,氢元素有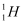 、
、 、
、 三种核素。下列说法正确的是( )
三种核素。下列说法正确的是( )
A . 由168O、11H、21H三种核素最多可能组成4种水分子
B . 10.0g由21H、168O组成的水分子其中含质子数为5NA
C . 10.0g由31H、168O组成的水分子其中含中子数为5NA
D . 由 31H和168O两种核素组成的水分子,其摩尔质量为18
含SO2的工业尾气可用石灰乳吸收处理,再经氧化制得CaSO4•2H2O(石膏),若处理含SO2 0.224%(体积分数)的尾气1×106 m3(标准状况),假定原料利用率均为100%,理论上可得到石膏的质量为(吨)( )
A . 17.2
B . 1.72
C . 1.2
D . 0.0172
在一定条件下,2mol XY3气体分解生成1mol Y2和2mol气态化合物甲.则甲的化学式为( )
A . XY
B . XY2
C . XY3
D . X2Y3
下列微粒结构示意图中,错误的是( )
A . 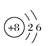 B .
B . 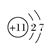 C .
C .  D .
D . 

称取两份铝粉,第一份加足量NaOH溶液,第二份加足量硫酸,如果要得到相同体积(同温同压)的氢气,两份铝粉的质量比是( )
A . 1:1
B . 1:3
C . 3:2
D . 1:2
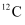 和
和 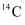 互为( )
互为( )
A . 同位素
B . 同分异构体
C . 同系物
D . 同素异形体
最近更新



