初中 化学
-
(1) 人类目前消耗的能源主要来自化石燃料,属于(填“可再生”或“不可再生”)能源。为节约煤资源,将煤块粉碎处理后使其在空气中燃烧得更快、更充分,这是因为。
-
(2) 金属材料在生产生活中有着广泛的应用。
①近年来,我国高铁建设促进了经济、社会的快速发展。制造铁轨的材料是铁合金,与纯铁相比较,铁合金具有(答一点)的优良性能。
②工业上将铁加入铬和镍可以制成不锈钢。如图是铬元素在元素周期表中的信息以及原子结构示意图。铬元素的相对原子质量为,x的数值是。

③工业上在加热条件下用氢气还原氧化镍(NiO)可得金属镍。氧化镍中镍元素的化合价为;该反应的化学方程式为:。
-
(1) 根据下列粒子结构示意图,回答问题:

①上述示意图中,共包含种元素。
②A、B、C、E中属于阴离子的是
 填离子符号
填离子符号  。
。③若D表示某元素的原子,则该粒子在化学变化中容易
 选填“得到”或“失去”
选填“得到”或“失去”  电子。
电子。④若D为离子,则BD构成的化合物的化学式为。
-
(2) 根据你对元素化合物的理解,请写出A与C组成化合物的化学式,B与E组成化合物的化学式。
-
(1) 2个亚铁离子
-
(2) 天然气的主要成分;
-
(3) 2个氢原子;
-
(4) 纯碱.
(提出问题)氧化铁能否作过氧化氢溶液分解的催化剂?如果能,其催化效果如何?
(实验探究)
|
实验步骤 |
实验现象 |
|
Ⅰ.分别量取5mL5%过氧化氢溶液放入A、B两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星木条,观察现象 |
A试管中产生气泡,带火星木条复燃,B试管中无明显现象 |
|
Ⅱ.待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,如此反复多次实验,观察现象 |
试管中均产生气泡,带火星木条均复燃 |
|
Ⅲ.将实验Ⅱ中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag |
|
|
Ⅳ.分别量取5mL5%过氧化氢溶液放入C、D两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象 |
(实验结论)
-
(1) 实验Ⅱ、Ⅲ证明:氧化铁的和在反应前后均没有发生变化,可以作过氧化氢分解的催化剂。
-
(2) 写出氧化铁催化过氧化氢分解的化学方程式。
-
(3) (实验评价)
设计实验Ⅳ的目的是。
-
(4) 若实验Ⅳ观察到D试管中产生气泡的速率更快,由此你可以得到的结论是。
-
(5) (实验拓展)
查阅资料得知,CuO、CuSO4、猪肝、马铃薯等也可以作过氧化氢溶液分解的催化剂。下列有关催化剂的说法中正确的是。
A.MnO2只能作过氧化氢溶液分解的催化剂
B. 同一个化学反应可以有多种催化剂
C.催化剂只能加快化学反应的速率
D.用作催化剂的物质不可能是其他反应的反应物或生成物
下图是a、b两种固体物质(不含结晶水)的溶解度曲线。下列叙述正确的是( )
如图粉尘爆炸实验装置,请仔细观察并回答下列问题:
-
(1) 吸入空气的目的是;
-
(2) 该实验说明可燃性其他粉尘点燃前应.

-
(1) 检验装置气密性,按图1连接装置,先,再加水至A下端形成一段水柱,静置,若观察到长颈漏斗内水柱不下降,说明气密性良好。
-
(2) 加入药品。添加块状CaCO3固体时,为避免打破锥形瓶,应将锥形瓶横放,再滑入固体。添加盐酸时,将稀盐酸从(填仪器A的名称)倒入锥形瓶至。
-
(3) 实验室探究制取二氧化碳的原料时,用碳酸钠与稀盐酸制取二氧化碳的化学方程式为;反应剧烈的原因是,并不适合作为实验室制取二氧化碳的原料。
-
(4) 如图2所示,有一瓶汽水,打开汽水瓶盖,有大量气泡冒出,其原因是。
-
(5) 如图3所示,在C处放入用石蕊溶液染成紫色的干燥的纸花完成以下实验:
在A处持续而缓缓地通入气体X。当关闭K时,C处的紫色石蕊纸花不变色;当打开K后,C处的紫色石蕊纸花变为红色。若气体X为未经干燥且混有氯化氢的二氧化碳,则B瓶中盛放的溶液不可能是____(填字母序号)。
A . 浓硫酸 B . 氢氧化钠溶液 C . 饱和碳酸氢钠溶液 -
(6) 如图4是利用数字化仪器测定CO2含量的探究实验。

①采用D图装置,将注射器中等量、等浓度的浓氢氧化钠溶液分别注入用排水法和排空气法收集的CO2气体的锥形瓶内(NaOH溶液均过量),得到如图5所示的压强随时间变化的曲线图。请说明锥形瓶内压强变化的原因。
②该实验说明收集到CO2的含量较高(填“排水法”或“排空气法”)。
③设计实验验证400秒时溶液中有溶质碳酸钠。
-
(1) 高氯酸钾(
 )可用作火箭燃料,其中氯元素的化合价为.
)可用作火箭燃料,其中氯元素的化合价为.
-
(2) 在运载火箭上用到了稀罕的钪钛合金.钪(
 )在元素周期表中的信息及原子结构示意图如图
)在元素周期表中的信息及原子结构示意图如图  所示.
所示. 
①钪属于(填“金属”或“非金属”)元素,位于第周期;钪离子的符号为.
②图
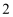 所表示的四种粒子中,与钪原子的化学性质相似的是,(填序号)因为它们.
所表示的四种粒子中,与钪原子的化学性质相似的是,(填序号)因为它们.
下列操作正确的是
A .  点燃酒精灯 B .
点燃酒精灯 B .  称量 10.05g 固体 C .
称量 10.05g 固体 C .  液体加热 D .
液体加热 D .  量取 9.5mL 液体
量取 9.5mL 液体
金属钛(Ti)是21世纪最重要的金属之一.某化学兴趣小组的同学为探究铝、铜、钛的金属活动顺序,做了如下实验:①先用砂布将金属表面擦光亮.②将大小、厚薄相同的三种金属片分别放入到盛有相同体积的同种盐酸的试管中,观察到的现象如下:
| 金属 | 钛 | 铝 | 铜 |
| 与盐酸反应的现象 | 放出气泡缓慢 | 放出气泡快 | 无现象 |
(1)依据上表现象推断三种金属的活动性顺序从强到弱为: ,把金属钛放在硫酸铜溶液中能否发生反应? (填“能”或“不能”);
(2)根据三种金属的性质和用途回答:①建筑常用铝合金做门窗,原因是 (答2点);②把钛或钛合金放在海水中数年,取出后仍光亮如新,这说明金属钛具有很强的 性.
写出下列反应的文字或符号表达式,并在括号内注明反应的基本类型:
⑴硫在空气中燃烧: ( )
⑵氯![]() 酸钾和二氧化锰混合物加热: ( )
酸钾和二氧化锰混合物加热: ( )
⑶任写一个既是化合反应又是氧化反应的例子:
实验室制取气体选择收集方法时,下列性质:①颜色;②密度;③溶解性;④可燃性;⑤能否与水反应,必须考虑的是( )
A.①②③ B.②③④ C.③④⑤ D.②③⑤
空气中能维持生命的气体是
A.氧气 B.氮气 C.二氧化碳 D.稀有气体



