中考化学试题
一定质量的金属铁和稀硫酸恰好完全反应,产生气体的质量为0.2 g。
(1)反应后溶液中溶质FeSO4的质量为_____g。
(2)向反应后的溶液中加入BaCl2溶液,当加入的BaCl2溶液质量为208 g时,恰好完全反应,此时生成沉淀的质量为________g。
(3)计算所加BaCl2溶液的溶质质量分数__________。
某补钙剂的主要成分是碳酸钙,欲测定补钙剂中碳酸钙的质量分数,某同学进行了如图的操作: 已知:其他成分不参与反应且不溶于水
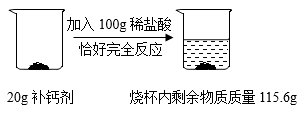
(1) 生成 CO 2 的质量为 _______g 。
(2) 计算该补钙剂中碳酸钙的质量分数。 ( 根据化学方程式计算,写出完整步骤 )
(3) 反应后,向烧杯中再加入 5.4g 水,求所得溶液中溶质的质量分数。
芹菜中的芹黄素 (C 15 H 10 O 5 ) 具有抗肿瘤、抗病毒等生物学活性。下列关于芹黄素的说法正确的是
A . 属于氧化物 B . 碳、氢、氧元素的质量比为 15 : 10 : 5
C . 由碳、氢、氧三种元素组成 D . 其中氧元素的质量分数最小
化学是一门以实验为基础的科学,根据下图所示实验回答下列问题:
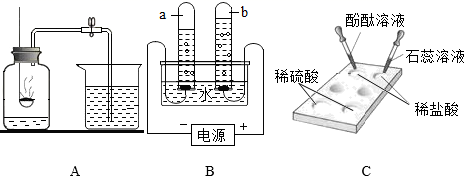
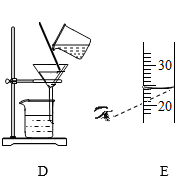
( 1 ) A 图中不用燃烧铁丝代替燃烧红磷进行实验的原因是 ______ 。
( 2 ) B 图电解水时 a 、 b 两试管中气体体积比约为 ______ 。
( 3 ) C 图中点滴板的优点 ______ (答一点即可)。
( 4 ) D 图中过滤后滤液仍浑浊的原因是 ______ (答一点即可)。
( 5 )在配制一定溶质质量分数氯化钠溶液时,量取水的操作如 E 图所示,其他操作均正确,所配制溶液中氯化钠的质量分数 ______ (填 “偏大”、“偏小”或“不变”)。
氢氧化钡与氢氧化钙同属于碱类物质,其化学性质相似吗?某兴趣小组的同学对此进行探究。
Ⅰ.定性探究
| 序号 | 操作 | 现象 | 结论 |
| 实验一 | 向氢氧化钡溶液中滴入_____试剂 | 溶液变红 | 氢氧化钡溶液呈碱性 |
| 实验二 | 向实验一的溶液中通入适量的二氧化碳 | 产生_____, 红色消失 | 氢氧化钡溶液能与 二氧化碳反应 |
| 实验三 | 另取氢氧化钡溶液,滴入一定量 的碳酸钠溶液 | 产生白色沉淀 | 氢氧化钡溶液能与 碳酸钠溶液反应 |
(1)写出实验三中发生反应的化学方程式_____;
同学们将上述三个实验中反应后的废液都倒入一个烧杯中,过滤后,得到白色沉淀和红色滤液,他们决定对沉淀和滤液进行探究。
探究一:(提出问题)沉淀能否与酸发生反应?
(实验探究)向沉淀中加入足量的稀硫酸,观察到有气泡产生,最终沉淀_____(填“消失”或“不消失”)。
探究二:(提出问题)滤液中除指示剂外,还有哪些溶质?
(作出猜想)①氢氧化钠, ②氢氧化钠、碳酸钠, ③_____。
(实验探究)
| 序号 | 操作 | 现象 | 结论 |
| 实验四 | 取滤液样品于试管中, 加入几滴稀盐酸 | 没有明显现象 | 猜想②不成立 |
| 实验五 | 取滤液样品于试管中, 加入几滴碳酸钠溶液 | 产生沉淀 | 猜想_____成立 |
(2)有同学提出:实验四的操作存在问题,导致结论不准确,请你改正:_____。
(3)小组同学讨论后发现,只用一种溶液做一次实验,就可以验证猜想,该溶液是_____。
Ⅱ.定量探究
向100g氢氧化钡溶液中滴加溶质质量分数为10%的硫酸铜溶液,溶液的导电能力随着硫酸铜溶液的加入发生如图的变化关系。
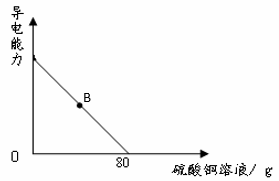
(1)溶液处于B点时,其中含有的是_____、_____、_____(填微粒符号)。
(2)计算氢氧化钡溶液的溶质质量分数_____。
碳及其化合物与生产、生活密切相关,是化学学习和研究的重要内容。
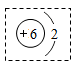
( 1 )请将如图虚线框内碳原子的结构示意图补画完整 ______ 。
( 2 )金刚石和石墨都属于碳单质,它们的化学性质相似,物理性质却有很大差异,其原因是 ______ (填字母代号)。
a 构成它们原子的大小不同 b 两种物质有不同种原子构成
c 构成它们的原子数目不同 d 两种物质里碳原子的排列方式不同
( 3 )某同学用如图装置(铁架台等略去)制取纯碱干燥的 CO 2 ,并探究 CO 2 的性质。
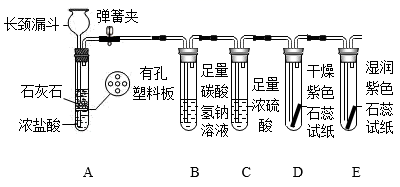
① A 装置能控制反应的发生和停止,请简述使反应停止的原理 ______ 。
② B 装置中可能发生反应的化学方程式为 ______ 。
③证明 CO 2 与水发生了化学反应的实验现象为 ______ 。
( 4 )制取 CO 2 后的酸性废液需处理后再排放;除去 CO 2 常用碱液吸收法。
①检验某废液是否呈酸性,可选用的一种试剂(或用品)是 ______ 。
②为探究足量 NaOH 溶液吸收 CO 2 后溶液中溶质成分,某同学设计了如下方案:取少量溶液,加入足量 Ca(OH) 2 溶液,反应后静置,取上层清液滴加酚酞溶液。若溶液变红,溶质为 Na 2 CO 3 和 NaOH 。请指出该方案中的错误并加以改正 ______ 。
( 5 )某温室大棚需用到 440LCO 2 (按标准状况计算, CO 2 密度为 1.964gL ),用足量盐酸与含 CaCO 3 80% 的石灰石反应制取,需要这种石灰石的质量是多少 ______ ?
学习化学要科学使用化学符号。下列叙述正确的是
A . 氯化镁( MgCl 2 )中含有 1 个 C 元素
B . 微粒 H 、 H + 的质子数相同但电子数不同
C . 空气、地壳中含量最多的元素都是 N
D . 铝表面致密氧化膜的化学式是 3O2A1
中华文化博大精深。下列古诗所述一定发生化学变化的是
A.飞流直下三千尺,疑似银河落九天
B.春蚕到死丝方尽,蜡炬成灰泪始干
C.夜来风雨声,花落知多少
D.床前明月光,疑是地上霜
蛋白质是由多种氨基酸构成的极为复杂的化合物,甘氨酸是构成人体蛋白质的氨基酸之一,如图是甘氨酸的分子结构模型图,下列对甘氨酸的叙述错误的是
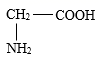
A . 甘氨酸中含有四种原子 B . 甘氨酸由碳、氢、氧、氮四个元素组成
C . 甘氨酸分子中质子与电子的数目相等 D . 甘氨酸中氧元素的质量分数最大
下列根据某些性质区分一些常见物质的方法错误的是
A . 羊毛和涤纶:灼烧闻气味 B . 硫酸铵和氯化铵:加熟石灰研磨
C . 铜片和黄铜片:相互刻画 D . 氧气和二氧化碳:伸入燃着的木条
(2019·云南) 下列有关实验方案设计正确的是 ( )
| 选项 | 实验目的 | 实验方案 |
| A | 配制6%的氯化钠溶液50 g | 称取3 g氯化钾固体溶于47 mL水中 |
| B | 证明氢氧化钠溶液与稀盐酸能反应 | 取氢氧化钠溶液于烧杯中,滴入几滴酚酞溶液,振荡,再滴入稀盐酸至溶液变为无色 |
| C | 除去CaCl2溶液中的少量盐酸 | 加入适量的铁粉 |
| D | 除去CO2中含有的少量CO | 点燃 |
证据推理是化学学科的核心素养,下列证据得出的结论正确的是
| 选项 | 证据 | 结论 |
| A | 单质由同种元素组成 | 只含一种元素的物质一定是单质 |
| B | 水通电得到氢气和氧气 | 水由氢原子和氧原子构成 |
| C | 酒精在空气中燃烧生成二氧化碳和水 | 酒精中一定含有碳元素和氢元素 |
| D | 物质与氧气发生反应都会放出热量 | 放热反应都是氧化反应 |
A . A B . B C . C D . D
已知: 20℃ 时, KCl 和 KNO 3 的溶解度分别为 34 g 和 31.6 g 。配制 20℃ 时的如下四种溶液:
| | 溶液 | ① | ② | ③ | ④ |
| 固体种类 | KCl | KCl | KNO 3 | KNO 3 | |
| 加入固体的质量 /g | 20 | 35 | 20 | 35 | |
| 水的质量 /g | 100 | 100 | 100 | 100 |
下列有关溶液 ① ~ ④ 的说法 不正确 的是 A .属于饱和溶液的是 ②④
B .溶液的质量 ②=④
C .溶液中溶质的质量分数 ①=③
D . ② 中溶质与溶剂的质量比为 17:50
请根据下面常用化学实验装置回答以下问题。
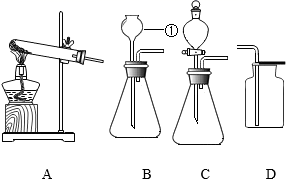
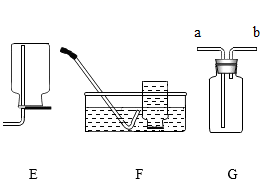
( 1 )写出仪器 ①的名称 ___________ 。
( 2 )实验室选用 B 装置制取氧气的化学方程式为 ___________ 。
( 3 )若用 F 装置收集氧气,当 ___________ 时开始收集,收集完氧气后用玻璃片 ___________ (填 “磨砂”或“光滑”)一面盖住集气瓶口, ___________ (填 “正放”或“倒放”)在桌面上。
( 4 )若用 G 装置通过排空气的方法收集氧气,验满的方法是 ___________ 。
( 5 )实验室制取 CO 2 的化学方程式为 ___________ 。
( 6 )实验室制取 CO 2 时,为了控制反应速率和节约药品,最好选择 ___________ (填字母)作为发生装置。检验生成气体是 CO 2 所选用的试剂为 ___________ 。
2018年5月18日,国际学术期刊《自然·纳米技术》介绍了中国科学家合成了一种新型催化剂,可将二氧化碳这一温室气体高效转化为清洁液体燃料甲醇,该反应的微观示意图如图所示。下列有关说法或化学方程式正确的是
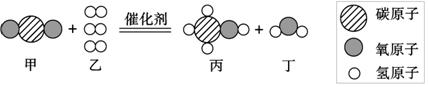
A. 甲、丙是有机化合物,也是氧化物 B. 该反应为复分解反应
C. 该反应前后氢元素的化合价不变 D. CO2 + 3H2  CH3OH + H2O
CH3OH + H2O
氢氧化铝是一种难溶于水的重要化学物质,医学上可用于治疗胃酸过多。
(1)写出用氢氧化铝治疗胃酸过多的化学方程式_____。人体服氯化铝溶液用氢氧化铝后胃液的pH会_____,(填“增大”或“减小”)。
(2)实验小组同学发现将氯化铝溶液逐滴加入氢氧化钠溶液中(如图1),发现刚开始并无氢氧化铝沉淀生成,为了探究刚开始没有沉淀生成的原因,同学们进行如下探究。
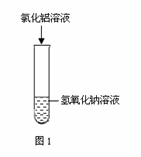
(查阅资料)①氢氧化铝属于两性物质,既可和酸(如盐酸)反应,又可和碱(如氢氧化钠溶液)反应。其中与NaOH反应的化学方程式为![]() 。
。
②NaAlO2(偏铝酸钠)可溶于水,可与少量酸反应生成氢氧化铝,但不与碱发生反应。
(提出猜想)
甲:可能所用的氢氧化钠溶液中含有酸,生成的沉淀与酸反应。
乙:可能生成的氢氧化铝与试管中过量的氢氧化钠反应。
(3)丙同学立刻否认了甲同学的猜想,理由是_____。
(实验验证)
为了验证乙同学的猜想,同学们设计了如下实验:
| 实验操作 | 现象 | 结论 |
| 取一定量氢氧化铝粉末,向其中逐滴加入氢氧化钠溶液至过量 | _____。 | 乙同学猜想正确 |
(思维拓展)上述实验说明反应物相同时,质量比不同会导致生成物不同,除上述化学反应外请你再举一例:_____。
(反思提高)不用其他试剂如何区别氯化铝和氢氧化钠两种无色澄清溶液_____。
该兴趣小组同学将氢氧化钠溶液逐滴加入到氯化铝溶液中,测得反应过程中生成沉淀质量变化如图2:
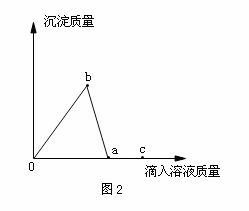
(4)分别写出a点、c点所对应溶液中溶质的成分_____(写化学式,下同),_____。向a点所得溶液中逐滴加入稀盐酸至过量,实验时的现象是_____。
(5)当b点所滴人的氢氧化钠溶液质量为mg时,则a点时所滴入溶液质量为_____。
将3.2g某红棕色粉末与足量的碳充分反应,将产生的二氧化碳气体全部通入足量的澄清石灰水中,得到3g白色沉淀。计算:
(1)生成二氧化碳的质量;
(2)红棕色粉末中氧元素的质量分数。
下列物质间的转化,不能一步实现的是
A.Zn→H2 B.CuO→Cu C.CO2→CO D.CO→CaCO3
构建化学基本观念是学好化学的基础。下列对化学基本观念的认识中,不正确的是
A .微粒观:过氧化氢是由氢分子和氧分子构成的
B .元素观:过氧化氢和水都是由氢元素和氧元素组成的
C .结构观:过氧化氢和水的化学性质不同是因为两者的分子构成不同
D .转化观:过氧化氢在一定条件下可以转化为水
科学技术的进步,证明了宏观物质世界由分子、原子、离子等微观粒子构成。请根据图所示按要求回答问题:
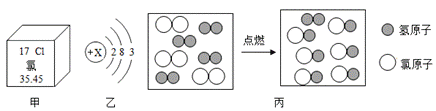
(1)图(甲)是氯元素在元素周期表中的部分信息,氯元素的相对原子质量是______________。
(2)图(乙)是某原子的结构示意图,则X的数值是______________,该原子形成的阳离子符号是____________,该元素与氯元素组成的化合物的化学式是______________。
(3)图(丙)是某化学反应的微观示意图,请写出该反应的化学方程式______________。