中考化学试题
镁是一种常见的金属,请回答下列问题。

(1)组成和结构:
①从宏观看,镁是由__________________组成的。
②从微观看,据图分析,镁位于元素周期表中第___周期,在化学反应中容易___(填“得到”或“失去”)电子形成镁离子。
(2)性质和变化:
①镁具有可燃性,在空气中燃烧的化学方程式是_______________。
②向镁条中滴加稀盐酸,产生大量气泡,此反应是一个____(填“放热”或“吸热”)反应。
③把一定量的镁放入硝酸铜和硝酸银的混合溶液中,充分反应后过滤,滤液为无色,则滤液中的溶质是___________(填化学式,下同),滤渣的组成可能是___________或_____________。
长期埋在地下的金属管线会被腐蚀。常温下,某金属管线的腐蚀速率与土壤含水量的关系如图所示。

(1)分析图示得出的结论是 。
下列对实验现象的描述或实验操作正确的是()
A. 镁条在空气中燃烧,产生大量白雾
B. 高锰酸钾制取氧气后,试管趁热清洗
C. 碘化钾溶液和硝酸银溶液混合,生成黑色沉淀
D. 粗盐提纯实验中,待滤悬浊液静置后过滤
下列实验操作能达到实验目的的是
| 选项 | 实验目的 | 实验操作 |
| A | 除去 NaOH 溶液中混有的 Na 2 CO 3 | 加过量的 Ca ( OH ) 2 溶液,过滤 |
| B | 检验 CH 4 中是否混有 H 2 | 点燃,在火焰上方罩一干冷烧杯 |
| C | 分离 CaCl 2 和 CaCO 3 的固体混合物 | 加足量的水溶解、过滤 |
| D | 比较黄铜片(铜锌合金)和铜片的硬度 | 黄铜片和铜片相互刻划 |
A . A B . B C . C D . D
甲、乙两种固体物质在水中的溶解度曲线如图所示。据图作答:

(1)甲、乙两物质的溶解度受温度影响较大的是________________;在0℃~t1℃之间时,相同温度下甲物质的溶解度______________(填“>”“<”或“=”)乙物质的溶解度。
(2)t2℃时,把20g甲物质加入50g水中充分溶解,所得溶液为______________(填“饱和”或“不饱和”)溶液,把该溶液降温到t1℃时,会析出甲物质__________________g。
为了除去粗盐中的Ca2+、Mg2+、SO42-等离子,可将粗盐溶于水后进行如下操作:①加入适量盐酸,②加过量NaOH溶液,③加过量Na2CO3溶液,④加过量BaCl2溶液,⑤过滤,⑥蒸发结晶。下列操作顺序合理的是
A.②③④⑤①⑥ B.②④③⑤①⑥ C.④②③①⑤⑥ D.④③②①⑤⑥
“低碳生活,绿色出行”。“低碳”指的是较低的 排放,自行车是人们喜爱的“绿色出行”工具,自行车的塑料车把手属于 材料,普通充气橡胶轮胎夏天易爆胎,而采用实体轮胎的自行车可有效防止爆胎,“夏天易爆胎”的微观解释是 。
(2020·成华模拟)钋广泛用于抗静电刷。钋元素的信息如图所示,下列对其说法错误的是( )
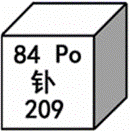
A. 属于金属元素 ![]() B. 原子内质子数为84
B. 原子内质子数为84 ![]() C. 元素符号为PO
C. 元素符号为PO ![]() D. 相对原子质量为209
D. 相对原子质量为209
(2019·孝感)小倩同学将妈妈的智能新手机屏幕解锁图形设置如图甲所示,圆圈内每个数字分别代表初中化学常见的一种物质(“-”表示相连两物质能发生化学反应,反应条件省略)。其中1为炭粉,7可用于工业上玻璃、造纸、纺织、洗涤剂的生产等,1、2、3、5、7分别为不同类别的物质。请回答下列问题。

(1)7代表的物质化学式为 。
(2)1和2发生的化学反应类型 (填“一定”或“不一定”)是置换反应。
(3)5和7发生反应的化学方程式可能为
(任写一个)。
(4)小茹认为小倩设置的解锁图形太简单,给她设置了如图T6-21乙所示的解锁图。若8为氯化钡,则6代表的物质类别为 (填序号)。
A.单质、酸
B.单质、氧化物或酸
C.单质、氧化物、酸或碱
D.单质、氧化物、酸、碱或盐
水在通电条件下会分解,反应的化学方程式为 ___________ 。
构建知识网络,绘制思维导图,是训练科学思维的有效途径。 A~D 是初中化学常见的四种无机化合物,其中,A 是常见的灭火剂,能制汽水、做气体肥料等,它也是造成温室效应加剧的主要物质之一。“—”表示两种物质间可以相互反应,“→”表示一种物质可以生成另一种物质。 分析推理,回答问题:
(1)除 A 外再举一例,分析该物质的利与弊: ▲ 。
(2)B 与 C 反应的实质为 ▲ 。
(3)写 A—C 反应的化学方程式: ▲ 。
(4)写出“D→A”的化学方程式: ▲ 。
某有机物燃烧后生成CO2和H2O两种物质,则此有机物的组成是( )
A.只含有碳、氢元素 B.一定含有碳、氢元素,可能含有氧元素
C.一定含有碳、氢、氧元素 D.肯定含有碳、氧元素
实验室除去粗实验中难溶性杂质的主要实验步骤有:溶解、 ______ 、蒸发;除去粗实验水中的杂质 CaC1 2 、 MgC1 2 、 Na 2 SO 4 ,可依次加入过量的 NaOH 、 ______ 、 Na 2 CO 3 溶液,分离出沉淀后,再加入适量盐酸,其作用是 ______ 。
在除去粗盐中难溶性杂质的实验中,下列操作正确的是

下列图示的实验操作中正确的是:

A.浓硫酸稀释 B.闻气体气味 C.液体的倾倒 D.检查气密性
某件衣服标签的部分内容如图,下列说法错误的是

A.羊毛是天然纤维
B.涤纶是合成纤维
C.涤纶比羊毛耐磨、耐腐蚀
D.合成纤维的吸水性和透气性比天然纤维好
市售 “ 自热米饭 ” 的自加热原理:饭盒夹层中的水与生石灰接触,反应放出大量热。该反应的化学方程式为 __________ 。
央视频道《是真的吗?》栏目中有一段视频:将“锡纸”剪成一段两头宽中间窄的纸条,然后两头分别连接电池的正负极,观察到“锡纸”立即燃烧。据此,小晟同学取某种“锡纸”进行了探究。
(1)“锡纸”燃烧的原因:“锡纸”两端接入电池两极后造成短路致使“锡纸”燃烧,从燃烧的条件分析:开始“锡纸”不燃烧但短路后却能燃烧的原因是________________(填“与氧气接触”或“温度达到着火点”)。
(2)探究“锡纸”中金属的成分:“锡纸”中的金属是锡吗?
【查阅资料】 ①“锡纸”是锡箔或铝箔和纸粘合而成;②锌粉是一种深灰色固体;③锡(Sn)与酸或盐溶液反应生成+2价的锡盐。
【提出猜想】 猜想Ⅰ:“锡纸”中的金属是锡;猜想Ⅱ:“锡纸”中的金属是铝。
【进行实验】 设计方案并进行实验。
| 实验操作 | 实验现象 | 实验分析与结论 |
| 取打磨后的“锡纸”片放入试管中,滴加氯化锌溶液 | “锡纸”表面有深灰色固体析出 | 根据实验现象,结合金属活动性顺序可知猜想______(填“Ⅰ”或“Ⅱ”)成立;反应的化学方程式为_________________________ |
【交流讨论】 ①实验中打磨“锡纸”的目的是___________________________________。
②下列物质的溶液可以替代氯化锌溶液完成上述实验的是________(填序号)。
A.氯化铜 B.硝酸银 C.硫酸钠 D.硫酸亚铁
【拓展应用】 电器短路会引起火灾,我们要严加防范。如果电器着火应该采取的灭火方法是_______________________________________。
我校化学兴趣小组欲将粗盐提纯,再用制取的精盐配制7.5%的氯化钠溶液100g。下列说法不正确的是( )
A. 配制溶液时要称量7.5g氯化钠,量取92.5mL的水
B. 本实验多次使用玻璃棒,有三种作用:搅拌、引流、转移
C. 本实验的主要步骤是溶解、过滤、蒸发和计算、称取、量取、溶解、转移
D. 本实验提纯的氯化钠可能不纯,导致配制的氯化钠溶液质量分数偏大