дёӯиҖғеҢ–еӯҰиҜ•йўҳ
е®һйӘҢжҳҜ科еӯҰжҺўз©¶зҡ„йҮҚиҰҒжүӢж®өпјҢдёӢеҲ—еҢ–еӯҰе®һйӘҢж“ҚдҪңжӯЈзЎ®зҡ„жҳҜпјҲгҖҖгҖҖпјү
AпјҺ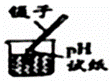 жөӢжә¶ж¶ІpHВ В В В В В В В В В В BпјҺ
жөӢжә¶ж¶ІpHВ В В В В В В В В В В BпјҺ зЁҖйҮҠжө“зЎ«й…ёВ
зЁҖйҮҠжө“зЎ«й…ёВ
CпјҺ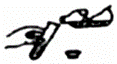 еҖҫеҖ’ж¶ІдҪ“В В В В В В В В В В В DпјҺ
еҖҫеҖ’ж¶ІдҪ“В В В В В В В В В В В DпјҺ В еҸ–з”ЁеӣәдҪ“иҚҜе“Ғ
В еҸ–з”ЁеӣәдҪ“иҚҜе“Ғ
з”Ёж°Ҝй…ёй’ҫеҲ¶еҸ– пјҢдёӢеҲ—еҢ–еӯҰж–№зЁӢејҸжӯЈзЎ®зҡ„жҳҜ
A пјҺ 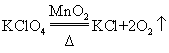
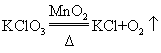
C пјҺ 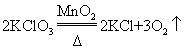
дёӢеҲ—зү©иҙЁдёӯпјҢж—ўеҗ«жңүеҲҶеӯҗеҸҲеҗ«жңүзҰ»еӯҗзҡ„жҳҜпјҲпјү
A.з”ҹй“Ғ
B.жө“зӣҗй…ё
C.е№ІеҶ°
D.еҢ»з”Ёй…’зІҫ
з©әж°”дёӯеҗ«йҮҸиҫғеӨҡдё”еҢ–еӯҰжҖ§иҙЁжҜ”иҫғжҙ»жіјзҡ„ж°”дҪ“жҳҜ
A. ж°®ж°”В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В B. ж°§ж°”
C. зЁҖжңүж°”дҪ“В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В В D. дәҢж°§еҢ–зўі
ж°ҙжҳҜдёҖеҲҮз”ҹзү©з”ҹеӯҳжүҖеҝ…йңҖзҡ„пјҢжҲ‘们еә”иҜҘдәҶи§Јжңүе…іж°ҙзҡ„дёҖдәӣзҹҘиҜҶпјҢеӣһзӯ”дёӢеҲ—й—®йўҳпјҡ
пјҲ1пјүзЎ¬ж°ҙз»ҷз”ҹжҙ»е’Ңз”ҹдә§еёҰжқҘеҫҲеӨҡйә»зғҰпјҢз”ҹжҙ»дёӯеҸҜз”Ё__жқҘеҢәеҲҶзЎ¬ж°ҙе’ҢиҪҜж°ҙгҖӮ
пјҲ2пјүжҲ‘еӣҪжҳҜж·Ўж°ҙиө„жәҗйқһеёёжңүйҷҗзҡ„еӣҪ家пјҢзҲұжҠӨж°ҙиө„жәҗжҳҜжҜҸдёӘе…¬ж°‘зҡ„иҙЈд»»е’Ңд№үеҠЎгҖӮдёӢеҲ—иЎҢдёәеұһдәҺжөӘиҙ№ж°ҙзҡ„жҳҜ__пјҲеЎ«еӯ—жҜҚзј–еҸ·пјүпјӣ
A жҙ—жүӢж“ҰйҰҷзҡӮж—¶дёҚе…ідёҠж°ҙйҫҷеӨҙВ В В В B з”Ёжҙ—иҸңж°ҙжөҮиҠұ
C з”Ёжҙ—иЎЈж°ҙеҶІеҺ•жүҖВ В В В В В В В В В В В В В D з”ЁиҮӘжқҘж°ҙдёҚж–ӯдёәиҘҝз“ңеҶІж°ҙйҷҚжё©
пјҲ3пјүеҰӮеӣҫжҳҜдёҖз§Қ家用зҺҜдҝқеһӢж¶ҲжҜ’ж¶ІеҸ‘з”ҹеҷЁпјҢе…¶дёӯеҸ‘з”ҹзҡ„дё»иҰҒеҸҚеә”жҳҜж°ҜеҢ–й’ е’Ңж°ҙеңЁйҖҡз”өжқЎд»¶дёӢеҸҚеә”з”ҹжҲҗж°ўж°§еҢ–й’ гҖҒж°ўж°”е’Ңж°Ҝж°”пјҲC12пјүпјҢиҜҘеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸдёә__гҖӮ
пјҲ4пјү18дё–зәӘжң«пјҢдәә们е°ұејҖе§ӢдәҶеҜ№ж°ҙзҡ„з»„жҲҗзҡ„з ”з©¶гҖӮиӢұеӣҪ科еӯҰ家жҷ®еҲ©ж–Ҝзү№йҮҢжҠҠвҖңжҳ“зҮғз©әж°”вҖқпјҲж°ўж°”пјүе’Ңз©әж°”ж··еҗҲеҗҺзӣӣеңЁе№ІзҮҘгҖҒжҙҒеҮҖзҡ„зҺ»з’ғ瓶дёӯпјҢеҪ“з”Ёз”өзҒ«иҠұзӮ№зҒ«ж—¶еҸ‘еҮәйңҮиҖізҡ„зҲҶйёЈеЈ°пјҢдё”зҺ»з’ғ瓶еҶ…еЈҒдёҠеҮәзҺ°дәҶж¶Іж»ҙгҖӮдёҚд№…пјҢеҚЎж–ҮиҝӘи®ёз”ЁзәҜж°§д»Јжӣҝз©әж°”иҝӣиЎҢдёҠиҝ°е®һйӘҢпјҢзЎ®и®ӨжүҖеҫ—ж¶Іж»ҙжҳҜж°ҙпјҢиҜҘеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸжҳҜ___________гҖӮеҹәдәҺеҚЎж–ҮиҝӘи®ёе®һйӘҢпјҢеҸҜеҫ—еҮәж°ҙжҳҜз”ұ__________з»„жҲҗзҡ„з»“и®әгҖӮ
дёҖе®ҡиҙЁйҮҸзҡ„жҹҗеҢ–еҗҲзү©е®Ңе…ЁзҮғзғ§пјҢйңҖиҰҒ 3.2g ж°§ж°”пјҢз”ҹжҲҗ 4.4g дәҢж°§еҢ–зўіе’Ң 1.8g ж°ҙгҖӮдёӢеҲ—еҲӨж–ӯй”ҷиҜҜзҡ„жҳҜ
A пјҺиҜҘеҢ–еҗҲзү©зҡ„иҙЁйҮҸдёә 3.0g
B пјҺиҜҘеҢ–еҗҲзү©дёҖе®ҡеҗ«жңүзўігҖҒж°ўгҖҒж°§дёүз§Қе…ғзҙ
C пјҺиҜҘеҢ–еҗҲзү©дёӯзўігҖҒж°ўгҖҒж°§зҡ„еҺҹеӯҗдёӘж•°жҜ”дёә 2 пјҡ 4 пјҡ 1
D пјҺиҜҘеҢ–еҗҲзү©дёӯзўіе…ғзҙ зҡ„иҙЁйҮҸеҲҶж•°жҳҜ 40%
еҢ–еӯҰжҳҜдёҖй—Ёд»Ҙе®һйӘҢдёәеҹәзЎҖзҡ„еӯҰ科пјҺж №жҚ®еҰӮеӣҫпјҢеӣһзӯ”й—®йўҳпјҺ
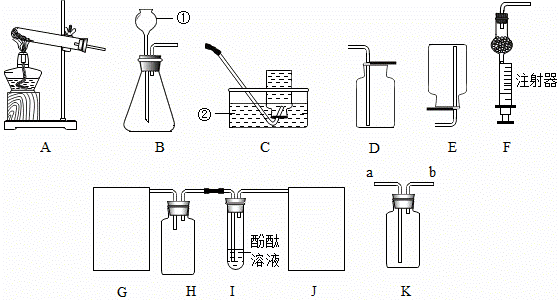
пјҲ1пјүд»ӘеҷЁзҡ„еҗҚз§°в‘ ______пјҢв‘Ў______пјҺ
пјҲ2пјүе®һйӘҢе®Өз”Ёй«ҳй”°й…ёй’ҫеҲ¶еҸ–ж°§ж°”пјҢйҖүз”Ёзҡ„еҸ‘з”ҹиЈ…зҪ®жҳҜ______пјҲеЎ«еӯ—жҜҚеәҸеҸ·пјүпјҢе…¶еҸҚеә”зҡ„ж–№зЁӢејҸдёә______пјҺдҪҶиҜҘиЈ…зҪ®йңҖиҰҒеҒҡйҖӮеҪ“ж”№иҝӣе…¶еҒҡжі•жҳҜ______пјҺ
пјҲ3пјүе®һйӘҢе®ӨеҲ¶еҸ–ж°ўж°”зҡ„еҢ–еӯҰж–№зЁӢејҸдёә______пјҢйҖүз”Ёзҡ„收йӣҶиЈ…зҪ®жҳҜ______пјҲеЎ«еӯ—жҜҚеәҸеҸ·пјүпјҺеҲ¶еҸ–ж°ўж°”ж—¶пјҢз”ЁиЈ…зҪ®Fжӣҝд»ЈиЈ…зҪ®Bзҡ„дјҳзӮ№жҳҜ______пјҺ
пјҲ4пјүж°Ёж°”жҳҜдёҖз§Қж— иүІгҖҒжңүејәзғҲеҲәжҝҖжҖ§иҮӯе‘ізҡ„ж°”дҪ“пјҢжһҒжҳ“жә¶дәҺж°ҙпјҺж°ҙжә¶ж¶ІиғҪдҪҝй…ҡй…һеҸҳзәўпјҺе®һйӘҢе®Өеёёз”ЁеҠ зғӯж°ҜеҢ–й“өе’ҢзҶҹзҹізҒ°дёӨз§ҚеӣәдҪ“ж··еҗҲзү©жқҘеҲ¶еҸ–ж°Ёж°”пјҺжҹҗе…ҙи¶Је°Ҹз»„зҡ„еҗҢеӯҰи®ҫи®ЎеҰӮеӣҫGпҪһJжүҖзӨәиЈ…зҪ®еҜ№ж°Ёж°”зҡ„еҲ¶еҸ–гҖҒжҖ§иҙЁиҝӣиЎҢжҺўз©¶пјҢе…¶дёӯGдёәж°”дҪ“еҸ‘з”ҹиЈ…зҪ®пјҢJдёә收йӣҶиЈ…зҪ®пјҺ
в‘ иЈ…зҪ®Gеә”йҖүжӢ©дёҠиҝ°иЈ…зҪ®дёӯзҡ„______пјҲеЎ«еӯ—жҜҚеәҸеҸ·пјүпјҺ
в‘ЎJиЈ…зҪ®йҖүжӢ©KиЈ…зҪ®ж”¶йӣҶж°Ёж°”пјҢж°Ёж°”еә”д»ҺеҜјз®Ў______иҝӣе…ҘпјҲеЎ«вҖңaвҖқжҲ–вҖңbвҖқпјүпјҺ
в‘ўиЈ…зҪ®Hзҡ„дҪңз”ЁжҳҜ______пјҺ
ж №жҚ®д»ҘдёӢзІ’еӯҗз»“жһ„зӨәж„ҸеӣҫпјҢиҜ·еӣһзӯ”дёӢеҲ—й—®йўҳпјҡ
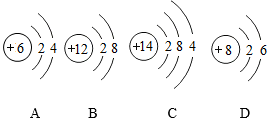
(1) еҶҷеҮә B зІ’еӯҗзҡ„з¬ҰеҸ· ___________ гҖӮ
(2) д»ҘдёҠзІ’еӯҗдёӯеҢ–еӯҰжҖ§иҙЁзӣёдјјзҡ„жҳҜ ___________( еЎ«еӯ—жҜҚ ) гҖӮ
(3) еҶҷеҮә B е’Ң D е…ғзҙ з»„жҲҗеҢ–еҗҲзү©зҡ„еҢ–еӯҰејҸ ___________ гҖӮ
еңЁ pH=10 зҡ„иӮҘзҡӮж°ҙдёӯж»ҙеҠ й…ҡй…һжә¶ж¶ІпјҢжә¶ж¶ІеҸҳ
A пјҺ ж— иүІ
B пјҺ зәўиүІ
C пјҺ и“қиүІ
D пјҺ зҙ«иүІ
дёӢеҲ—е®һйӘҢи®ҫи®ЎпјҢдёҚиғҪиҫҫеҲ°е®һйӘҢзӣ®зҡ„зҡ„жҳҜ
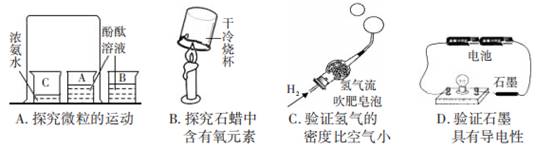
В еңЁдёҖж¬Ўе®һи·өжҙ»еҠЁдёӯпјҢеҢ–еӯҰе…ҙи¶Је°Ҹз»„зҡ„еҗҢеӯҰеңЁе®һйӘҢе®ӨеҲ©з”ЁзЁҖзЎ«й…ёгҖҒBaпјҲNO3пјү2 жә¶ж¶ІгҖҒNa2CO3
жә¶ж¶ІгҖҒNaOH жә¶ж¶ІжЁЎжӢҹеҢ–е·ҘеҺӮе·Ҙдёҡеәҹж°ҙзҡ„еӨ„зҗҶиҝҮзЁӢгҖӮ
гҖҗжҙ»еҠЁдёҖгҖ‘е°Ҷеӣӣз§Қжә¶ж¶ІдёӨдёӨж··еҗҲеҲӨж–ӯиғҪеҗҰеҸ‘з”ҹеҸҚеә”гҖӮ
пјҲ1пјүеӣӣз§Қжә¶ж¶ІдёӯиғҪеҪјжӯӨеҸ‘з”ҹеҸҚеә”зҡ„жңү В В в–ІВ В з»„пјҢеҶҷеҮәе…¶дёӯдёҖдёӘеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸпјҡВ в–І В гҖӮ пјҲ2пјүиғҪеҸ‘з”ҹеҸҚеә”дҪҶжІЎжңүжҳҺжҳҫзҺ°иұЎзҡ„дёҖз»„зү©иҙЁеҸҚеә”зҡ„еҫ®и§Ӯжң¬иҙЁжҳҜ В В в–ІВ В гҖӮ
пјҲ3пјүе®һйӘҢе®ҢжҜ•пјҢеҗҢеӯҰ们е°Ҷеәҹж¶ІеҖ’е…ҘеҗҢдёҖдёӘеӨ§зғ§жқҜдёӯпјҢйқҷзҪ®пјҢи§ӮеҜҹпјҢжқҜеә•жңүзҷҪиүІжІүж·ҖпјҢдёҠеұӮ
жә¶ж¶Ідёәж— иүІгҖӮ 并еҜ№зҷҪиүІжІүж·Җе’ҢдёҠеұӮж— иүІжә¶ж¶Ізҡ„жҲҗеҲҶиҝӣиЎҢдәҶиҝӣдёҖжӯҘзҡ„жҺўз©¶гҖӮ
гҖҗжҙ»еҠЁдәҢгҖ‘жҺўз©¶зҷҪиүІжІүж·Җзҡ„жҲҗеҲҶ
гҖҗиҝӣиЎҢзҢңжғігҖ‘зҢңжғів‘ пјҡзҷҪиүІжІүж·ҖжҳҜ BaSO4пјӣзҢңжғів‘ЎпјҡзҷҪиүІжІүж·ҖжҳҜ BaSO4 е’Ң BaCO3 зҡ„ж··еҗҲзү©
гҖҗе®һйӘҢйӘҢиҜҒгҖ‘
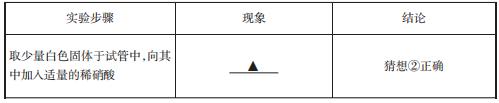
гҖҗжҙ»еҠЁдёүгҖ‘жҺўз©¶еәҹж¶ІжқҜдёӯж— иүІжә¶ж¶Ізҡ„жҲҗеҲҶ
в‘ иҙЁз–‘в… пјҡе°Ҹејәи®ӨдёәеңЁеҸҚеә”зү©дёӯжңүй…ёпјҢеҸҚеә”зҡ„з”ҹжҲҗзү©дёӯд№ҹжңүй…ёпјҢжүҖд»Ҙж— иүІжә¶ж¶Ідёӯе°ұдёҖе®ҡеҗ«жңүй…ёгҖӮ дҪҶе°ҸзәўжҸҗеҮәдәҶдёҚеҗҢзҡ„и§ӮзӮ№пјҢеҘ№и®Өдёә В В в–ІВ В пјҢеҗҢеӯҰ们дёҖиҮҙеҗҢж„Ҹе°Ҹзәўзҡ„и§ӮзӮ№гҖӮ
в‘ЎжЈҖйӘҢжә¶ж¶Ізҡ„й…ёзўұеәҰпјҡжүҖз”Ёе®һйӘҢз”Ёе“Ғжңү В В в–ІВ В гҖӮ з»ҸжөӢе®ҡжә¶ж¶Ізҡ„ pHпјһ7пјҢе‘ҲзўұжҖ§гҖӮ
в‘ў
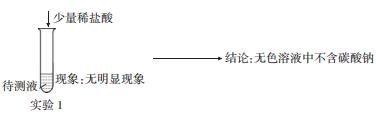
иҙЁз–‘в…Ўпјҡе°Ҹжһ—и®Өдёәе®һйӘҢ 1 дёҚиғҪиҜҒжҳҺж— иүІжә¶ж¶ІдёӯдёҚеҗ«зўій…ёй’ пјҢзҗҶз”ұжҳҜ В В в–ІВ В гҖӮ иҰҒиҜҒжҳҺжә¶ж¶ІдёӯдёҚеҗ«жңүзўій…ёй’ зҡ„е®һйӘҢж–№жЎҲжҳҜ В В в–ІВ В гҖӮ
еҫ—еҮәз»“и®әпјҡж— иүІжә¶ж¶ІдёӯдёҖе®ҡеҗ«жңүзҡ„жә¶иҙЁжҳҜ В В в–ІВ В пјҲеЎ«еҢ–еӯҰејҸпјүгҖӮ
гҖҗеҸҚжҖқдёҺдәӨжөҒгҖ‘е·ҘеҺӮжҺ’ж”ҫеҮәзҡ„еәҹж¶Іеёёе‘Ҳй…ёжҖ§жҲ–зўұжҖ§пјҢжҺ’ж”ҫеүҚжҲ‘们еҝ…йЎ»иҝӣиЎҢеӨ„зҗҶгҖӮ
з”ЁиҜ•з®ЎеӨ№еӨ№жҢҒиҜ•з®ЎеҠ зғӯж—¶пјҢиҜ•з®ЎеӨ№еә”з”ұиҜ•з®ЎВ В В В В В В В В еҫҖВ В В В В В В В еҘ—пјҢжіЁж„ҸжүӢжҢҮдёҚиғҪжҢүеңЁиҜ•з®ЎеӨ№зҡ„жҹ„дёҠгҖӮ
жҹҗеҗҢеӯҰз”ЁpHиҜ•зәёжөӢе®ҡжҹҗй…ёжҖ§жә¶ж¶Ізҡ„pHж—¶пјҢд»–е…Ҳз”Ёи’ёйҰҸж°ҙе°ҶpHиҜ•зәёж№ҝж¶ҰпјҢ然еҗҺеҶҚжөӢе®ҡпјҢеҲҷд»–жүҖжөӢеҫ—зҡ„жә¶ж¶ІpHе°ҶпјҲВ В пјү
AпјҺеҒҸеӨ§В В В В В В В В В В В В BпјҺеҒҸе°ҸВ В В В В В В В В В В В CпјҺж— еҪұе“ҚВ В В В В В В В В В DпјҺж— жі•зЎ®е®ҡ
дёӯеӣҪ科еӯҰйҷўз§‘з ”еӣўйҳҹз ”з©¶жҲҗжһңиЎЁжҳҺпјҢеңЁеёёжё©гҖҒеёёеҺӢе’ҢеҸҜи§Ғе…үжқЎд»¶дёӢпјҢеҹәдәҺ LDH( дёҖз§ҚеӣәдҪ“еӮ¬еҢ–еүӮ ) еҗҲжҲҗж°Ёж°” (NH 3 ) зҡ„еҺҹзҗҶеҰӮеӣҫжүҖзӨәгҖӮдёӢеҲ—иҜҙжі•дёҚжӯЈзЎ®зҡ„жҳҜ
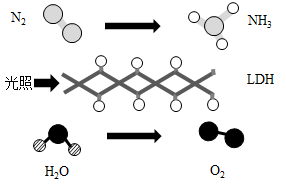
A пјҺеӣӣз§Қзү©иҙЁдёӯжңүдёҖз§ҚеұһдәҺж°§еҢ–зү©
B пјҺеҺҹж–ҷж°” N 2 еҸҜйҖҡиҝҮеҲҶзҰ»ж¶ІжҖҒз©әж°”иҺ·еҫ—
C пјҺеҸӮеҠ еҸҚеә”зҡ„ N 2 дёҺз”ҹжҲҗзҡ„ O 2 иҙЁйҮҸжҜ”дёә 7:8
D пјҺеҸӮеҠ еҸҚеә”зҡ„ N 2 дёҺ H 2 O зҡ„еҲҶеӯҗдёӘж•°жҜ”дёә 1:3
з«ҜеҚҲдҪіиҠӮпјҢзІҪеҸ¶йЈҳйҰҷпјҢиӣӢй»„иӮүзІҪеӣ е…¶иҗҘе…»дё°еҜҢгҖҒзҫҺе‘іеҸҜеҸЈж·ұеҸ—дәә们зҡ„е–ңзҲұгҖӮ
пјҲ1пјүзІҪеҸ¶дёӯеҜҢеҗ«зҡ„зәӨз»ҙзҙ ______________пјҲйҖүеЎ«вҖңеұһдәҺвҖқжҲ–вҖңдёҚеұһдәҺвҖқпјүзі–зұ»зү©иҙЁгҖӮ
пјҲ2пјүиӣӢй»„дёӯеҗ«жңүCгҖҒHгҖҒOгҖҒNгҖҒPзӯү______________пјҲйҖүеЎ«вҖңе…ғзҙ вҖқгҖҒвҖңеҲҶеӯҗвҖқжҲ–вҖңеҚ•иҙЁвҖқпјүгҖӮ
пјҲ3пјүзҳҰиӮүдёӯзҡ„______________еңЁиғғгҖҒиӮ дёӯзҡ„й…¶еҸҠдҪ“еҶ…ж°ҙзҡ„дҪңз”ЁдёӢпјҢйҖҗжӯҘеҲҶи§ЈпјҢз”ҹжҲҗеҸҜд»Ҙиў«еҗёж”¶зҡ„е°ҸеҲҶеӯҗеҢ–еҗҲзү©ж°Ёеҹәй…ёгҖӮ
пјҲ4пјүеӨ§зұізҡ„дё»иҰҒжҲҗеҲҶжҳҜж·ҖзІүпјҢе®ғжҳҜз”ұз»ҝиүІжӨҚзү©йҖҡиҝҮе…үеҗҲдҪңз”ЁеҗҲжҲҗзҡ„и‘Ўиҗ„зі–иҝӣдёҖжӯҘиҪ¬еҢ–иҖҢжҲҗзҡ„гҖӮе…үеҗҲдҪңз”Ёзҡ„еҢ–еӯҰеҸҚеә”ж–№зЁӢејҸдёә____________________гҖӮ
еӣһзӯ”дёӢеҲ—й—®йўҳ
пјҲ 1 пјүжҹҗе…ҙи¶Је°Ҹз»„еҸӮи§ӮзҒ«еҠӣеҸ‘з”өеҺӮпјҢдәҶи§ЈеҲ°еәҹж°”дёӯзҡ„ SO 2 гҖҒ NO 2 гҖҒ CO гҖҒ CO 2 дјҡеҪұе“ҚзҺҜеўғпјҢи®ҫи®ЎеҰӮеӣҫжөҒзЁӢеӨ„зҗҶеәҹж°”гҖӮ
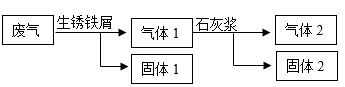
в‘ з”Ёз”ҹй”Ҳй“Ғеұ‘еӨ„зҗҶеәҹж°”дёӯзҡ„ CO пјҢдҪ“зҺ° CO ______ жҖ§гҖӮ
в‘Ўз”ЁзҹізҒ°жөҶдёҚз”ЁзҹізҒ°ж°ҙзҡ„еҺҹеӣ жҳҜ ______ гҖӮ
в‘ўеӣәдҪ“ 2 дёӯжңү ______ пјҲеҶҷдёӨз§Қзү©иҙЁпјүгҖӮ
пјҲ 2 пјү A~D дёәеҲқдёӯеҢ–еӯҰеёёи§Ғзү©иҙЁпјҢиҪ¬еҢ–е…ізі»еҰӮеӣҫгҖӮ A жҳҜз”ұдёӨз§Қе…ғзҙ з»„жҲҗзҡ„й’ҷзӣҗпјҢ C жҳҜзҒ«еҠӣеҸ‘з”өеҺӮжҺ’ж”ҫзҡ„жё©е®Өж°”дҪ“гҖӮ
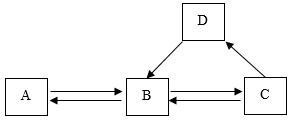
в‘ B иҪ¬еҢ–дёә A зҡ„еҢ–еӯҰж–№зЁӢејҸдёә ______
в‘ЎиӢҘ D е№ҝжіӣз”ЁдәҺзҺ»з’ғгҖҒжҙ—ж¶ӨеүӮзҡ„з”ҹдә§пјҢеҲҷ D иҪ¬еҢ–дёә B зҡ„еҹәжң¬еҸҚеә”зұ»еһӢжҳҜ ______ пјҢжЈҖйӘҢ D дёӯйҳҙзҰ»еӯҗзҡ„ж–№жі•жҳҜ ______ гҖӮ
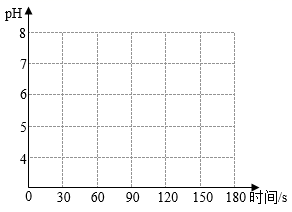
в‘ўе°Ҷи¶ійҮҸ C йҖҡе…Ҙзҹіи•Ҡжә¶ж¶ІдёӯпјҢзҺ°иұЎжҳҜ ______ пјҢиҜҘжә¶ж¶І pH=4 пјҢеҠ зғӯиҮі 90s ж—¶ C е®Ңе…ЁжҺ’еҮәпјҢз”»еҮәеҠ зғӯиҝҮзЁӢ pH еҸҳеҢ–еӣҫеғҸ _____ гҖӮ
в‘ЈзЎқй…ёй’ҫеҸҜдҪңеҢ–иӮҘпјҢиғҪдҫӣз»ҷдҪңзү©дёӨз§Қе…»еҲҶпјҢеұһдәҺ ______ иӮҘж–ҷгҖӮ
еҢ–зҹізҮғж–ҷеңЁдәәзұ»зӨҫдјҡзҡ„еҸ‘еұ•дёӯеҚ жҚ®йҮҚиҰҒең°дҪҚгҖӮ
пјҲ1пјүеҢ–зҹізҮғж–ҷеҢ…жӢ¬з…ӨгҖҒзҹіжІ№е’Ң________пјҢе®ғ们жҳҜ________пјҲеЎ«вҖңеҸҜвҖқжҲ–вҖңдёҚеҸҜвҖқпјүеҶҚз”ҹиғҪжәҗгҖӮ
пјҲ2пјүе°ҶзҹіжІ№еҠ зғӯзӮјеҲ¶пјҢеҸҜеҫ—еҲ°дёҚеҗҢзҡ„дә§е“ҒпјҢе…¶дёӯз”ЁдҪңжұҪиҪҰзҮғж–ҷзҡ„дә§е“Ғд№ӢдёҖжҳҜ__________гҖӮ
пјҲ3пјүз…ӨзҮғзғ§жҺ’ж”ҫзҡ„_________жә¶дәҺйӣЁж°ҙпјҢдјҡеҪўжҲҗй…ёйӣЁгҖӮж–°иғҪжәҗзҡ„еә”з”ЁеҸҜжңүж•Ҳзј“и§ЈиҜҘй—®йўҳпјҢзӣ®еүҚдәәзұ»жӯЈеңЁејҖеҸ‘е’ҢеҲ©з”Ёзҡ„дёҖз§Қж–°иғҪжәҗжҳҜ________гҖӮ
дёӢеҲ—еӣҫеғҸиғҪжӯЈзЎ®еҸҚжҳ еҜ№еә”е…ізі»зҡ„жҳҜ
A пјҺ дёҖе®ҡйҮҸзҡ„ж°§еҢ–й“ңе’ҢзӮӯзІүеңЁз©әж°”дёӯзҒјзғ§ 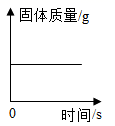
B пјҺ еҗ‘дёҖе®ҡйҮҸзҡ„ж°ҜеҢ–дәҡй“Ғе’Ңж°ҜеҢ–й“ңж··еҗҲжә¶ж¶ІдёӯеҠ е…ҘиҝҮйҮҸй•ҒзІү 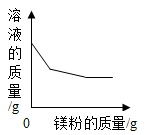
C пјҺ еҫҖ 10g10% зҡ„ж°ўж°§еҢ–й’ жә¶ж¶Ідёӯзј“ж…ўж»ҙеҠ 10g10% зҡ„зЁҖзӣҗй…ё 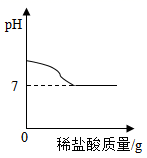
D пјҺ иҙЁйҮҸзӣёзӯүзҡ„й“қзІүе’Ңй”ҢзІүеҲҶеҲ«еҠ е…Ҙи¶ійҮҸзҡ„зЁҖзЎ«й…ё 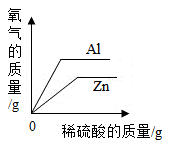
жө“зЎ«й…ёжҳҜдёҖз§Қе…·жңүејәзғҲи…җиҡҖжҖ§зҡ„еҢ–еӯҰиҜ•еүӮпјҢйңҖеј иҙҙзҡ„ж Үеҝ—жҳҜ
A пјҺ  B пјҺ
B пјҺ  C пјҺ
C пјҺ  D пјҺ
D пјҺ 
жҹҗеҢ–еӯҰе…ҙи¶Је°Ҹз»„е°Ҷе…үдә®й“ңзүҮж”ҫеңЁй…’зІҫзҒҜзҒ«з„°дёҠзҒјзғ§пјҢеҸ‘зҺ°иЎЁйқўеҸҳй»‘пјҢ他们еҜ№й»‘иүІзү©иҙЁзҡ„жҲҗеҲҶдә§з”ҹдәҶе…ҙи¶ЈпјҢй“ңзүҮиЎЁйқўзҡ„й»‘иүІзү©иҙЁжҳҜд»Җд№Ҳе‘ўпјҹ
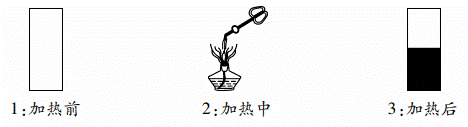
пјҲжҹҘйҳ…иө„ж–ҷпјү
(1)й…’зІҫдёҚе……еҲҶзҮғзғ§дә§з”ҹзӮӯй»‘пјҲеҚій»‘зғҹпјүпјӣ
(2)ж°§ж°”зҡ„еҢ–еӯҰжҖ§иҙЁжҜ”иҫғжҙ»жіјпјҢеҠ зғӯжқЎд»¶дёӢиғҪдёҺйҮ‘еұһй“ңеҸҚеә”з”ҹжҲҗй»‘иүІзҡ„ж°§еҢ–й“ңгҖӮ
(3)ж°§еҢ–й“ңиғҪдёҺзЁҖзЎ«й…ёеҸҚеә”з”ҹжҲҗзЎ«й…ёй“ңе’Ңж°ҙпјӣзӮӯй»‘йҡҫжә¶дәҺж°ҙпјҢдё”дёҺзЁҖзЎ«й…ёдёҚеҸ‘з”ҹеҸҚеә”гҖӮ
пјҲзҢңжғідёҺеҒҮи®ҫпјү
зҢңжғі1пјҡй»‘иүІзү©иҙЁжҳҜзӮӯй»‘гҖӮ
зҢңжғі2пјҡй»‘иүІзү©иҙЁжҳҜз©әж°”дёӯзҡ„ж°§ж°”дёҺй“ңеҸҚеә”з”ҹжҲҗзҡ„ж°§еҢ–й“ңгҖӮ
зҢңжғі3пјҡй»‘иүІзү©иҙЁж—ўжңүзӮӯй»‘еҸҲжңүж°§еҢ–й“ңгҖӮ
пјҲиҝӣиЎҢе®һйӘҢпјү
| е®һйӘҢжӯҘйӘӨ | е®һйӘҢзҺ°иұЎ |
| е®һйӘҢдёҖпјҡеҸ–дёҖе°Ҹж®өе…үдә®й“ңзүҮпјҢж”ҫе…ҘиҜ•з®ЎеҶ…пјҢ然еҗҺз”ЁиҜ•з®ЎеӨ№еӨ№жҢҒиҜ•з®ЎпјҢж”ҫеңЁй…’зІҫзҒҜзҡ„еӨ–з„°йғЁдҪҚеҠ зғӯ | й“ңзүҮеҸҳй»‘ |
| е®һйӘҢдәҢпјҡеҸ–дёҖж”ҜиҜ•з®ЎпјҢе°ҶдёҖе°Ҹж®өе…үдә®й“ңзүҮж”ҫе…ҘиҜ•з®ЎдёӯпјҢеЎһдёҠиғ¶еЎһпјҢ并用注射еҷЁжҠҪеҮәиҜ•з®ЎеҶ…зҡ„з©әж°”пјҢе°ҒеҘҪиғ¶еЎһпјҢ并еҠ зғӯпјҢи¶ҒзғӯеҸ–дёӢиғ¶еЎһпјҢи§ӮеҜҹзҺ°иұЎ | жү“ејҖиғ¶еЎһеүҚй“ңзүҮдёҚеҸҳй»‘пјӣжү“ејҖиғ¶еЎһеҗҺй“ңзүҮеҸҳй»‘ |
| е®һйӘҢдёүпјҡе°ҶеңЁй…’зІҫзҒҜзҒ«з„°дёҠзҒјзғ§еҗҺзҡ„йҷ„зқҖй»‘иүІзү©иҙЁзҡ„й“ңзүҮпјҢжҠ•е…ҘеҲ°зӣӣжңүи¶ійҮҸзЁҖзЎ«й…ёзҡ„иҜ•з®Ўдёӯ | иҜ•з®ЎдёӯжІЎжңүй»‘иүІзү©иҙЁеү©дҪҷпјҢжә¶ж¶Із”ұж— иүІеҸҳдёәи“қиүІ |
пјҲи§ЈйҮҠдёҺз»“и®әпјү
(1)з”ұе®һйӘҢеҸҜзҹҘпјҢзҢңжғі________жҲҗз«ӢгҖӮ
(2)е®һйӘҢдәҢз”ЁжіЁе°„еҷЁжҠҪеҮәиҜ•з®ЎеҶ…з©әж°”зҡ„зӣ®зҡ„жҳҜ_________гҖӮ
(3)йҖҡиҝҮеҜ№й»‘иүІзү©иҙЁжқҘжәҗзҡ„жҺўз©¶пјҢйҮ‘еұһй“ңдёҺж°§ж°”еҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸжҳҜ_________
(4)йҖҡиҝҮе®һйӘҢдёҖе’Ңе®һйӘҢдёүйғҪиғҪеҫ—еҮәзҢңжғі1е’ҢзҢңжғі3дёҚжӯЈзЎ®пјҢдёӨдёӘе®һйӘҢжҳҜд»ҺдёӨдёӘи§’еәҰиҝӣиЎҢи®ҫи®Ўе®һйӘҢж–№жЎҲзҡ„пјҢе®һйӘҢдёҖжҳҜд»Һ____________зҡ„и§’еәҰжҺўз©¶пјӣе®һйӘҢдёүжҳҜд»Һ_____________зҡ„и§’еәҰжҺўз©¶гҖӮ
пјҲеҸҚжҖқжӢ“еұ•пјү
(5)е®һйӘҢдёҖдёәд»Җд№ҲиғҪе°ҶзҢңжғі1е’ҢзҢңжғі3еҗҢж—¶жҺ’йҷӨе‘ўпјҹдҪ и®ӨдёәдҫқжҚ®жҳҜ_____________________гҖӮ



