2019年至2020年高一上册第一次月考化学试卷(江苏省沭阳县修远中学)
| 1. 选择题 | 详细信息 |
|
蛋白质是人类必须的营养物质。下列食物中富含蛋白质的是 A. 面包 B. 米饭 C. 牛肉 D. 蔬菜 |
|
| 2. 选择题 | 详细信息 |
|
下列物质中属于电解质的是( ) A. NH3 B. 乙醇 C. Cu D. NaCl |
|
| 3. 选择题 | 详细信息 |
|
在容量瓶上没有标记的是( ) A.刻度线 B.温度 C.浓度 D.容量 |
|
| 4. 选择题 | 详细信息 |
|
下列能达到实验目的的是 A. 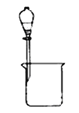 分离水和CCl4 B. 分离水和CCl4 B. 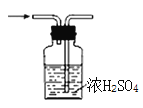 干燥Cl2 干燥Cl2C. 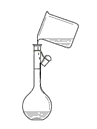 转移溶液 D. 转移溶液 D. 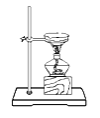 蒸发食盐 蒸发食盐 |
|
| 5. 选择题 | 详细信息 |
|
下列关于 A. C. |
|
| 6. 选择题 | 详细信息 |
|
下列反应属于置换反应的 A. CaH2+2H2O=Ca(OH)2+2H2↑ B. Fe2O3+3CO C. 2Al + Fe2O3 |
|
| 7. 选择题 | 详细信息 |
|
钠与水反应时,观察到的现象是( ) ①钠浮在水面上 ②钠先沉入水中 ③钠熔成光亮的小球 ④四处游动 ⑤发出“嘶嘶”的响声,甚至发生轻微的爆炸 ⑥滴入酚酞溶液变红 A. 全部 B. ①③④⑤⑥ C. ②③⑥ D. ②③④⑤⑥ |
|
| 8. 选择题 | 详细信息 |
|
下列反应属于氧化还原反应的是 A. CaCO3+2HCl=CaCl2+CO2↑+ H2O B. CaO+H2O=Ca(OH)2 C. 2H2O2 D. CaCO3 |
|
| 9. 选择题 | 详细信息 |
|
MgCl2、KCl、K2SO43种盐配成混合液后,若溶液中n(K+)=1.5 mol、n(Mg2+)=0.5 mol、n(Cl-)=1.5 mol,则溶液中n(SO42-)应为 A. 0.5 mol B. 0.25 mol C. 0.15 mol D. 1 mol |
|
| 10. 选择题 | 详细信息 |
|
0.5L 1mol/L FeCl3溶液与0.2L 1mol/L KCl溶液中的Cl-的数目之比为( ) A. 5:2 B. 3:1 C. 15:2 D. 1:3 |
|
| 11. 选择题 | 详细信息 |
|
气体体积的大小,跟下列因素几乎无关的是 A. 分子个数 B. 温度 C. 压强 D. 分子直径 |
|
| 12. 选择题 | 详细信息 |
|
下列有关实验操作正确的是( ) A. 蒸馏实验中温度计的水银球应插入液态混合物中 B. 用酒精萃取碘水中的碘 C. 分液时,下层液体从分液漏斗下口流出,上层液体从上口倒出 D. 开始蒸馏时,应该先加热,再开冷凝水;蒸馏完毕,应先关冷凝水再撤酒精灯 |
|
| 13. 选择题 | 详细信息 |
|
在含有大量H+、Ba2+、Cl-的溶液中,还可能大量存在的离子是( ) A. OH- B. SO42- C. Ag+ D. NH4+ |
|
| 14. 选择题 | 详细信息 |
|
下列反应的离子方程式书写正确的是( ) A. H2SO4溶液与氨水反应:H++OH-=H2O B. CuO与稀盐酸反应:CuO+2H+=Cu2++H2O C. AlCl3溶液与氢氧化钠溶液反应:AlCl3+3OH-=Al(OH)3↓+3Cl- D. 铁粉与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
|
| 15. 选择题 | 详细信息 |
|
相等物质的量的CO和CO2相比较,下列有关叙述中正确的是( )。 ①它们所含的分子数目之比为1∶1; ②它们所含的O原子数目之比为1∶2; ③它们所含的原子总数目之比为2∶3; ④它们所含的C原子数目之比为1∶1;⑤它们所含的电子数目之比为7∶11 A. ①②③④ B. ②和③ C. ④和⑤ D. ①②③④⑤ |
|
| 16. 选择题 | 详细信息 |
|
除去括号内杂质所用试剂和方法不正确的是( ) A. Cu(Fe)----加盐酸,过滤; B. NaCl溶液(碘)----CCl4,萃取、分液; C. KNO3溶液(NaCl)----降温结晶,过滤 D. CO2(HCl)----氢氧化钠溶液,洗气 |
|
| 17. 选择题 | 详细信息 |
|
对于某些离子的检验及结论一定正确的是( ) A. 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,可能有CO32- B. 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- C. 加硝酸银溶液产生白色沉淀,一定有Cl- D. 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+ |
|
| 18. 选择题 | 详细信息 |
|
在无色强酸性溶液中,下列各组离子一定能大量共存的是 A. Na+、K+、Cl-、SO42- B. Cu2+、K+、SO42-、NO3- C. K+ 、NH4+、SO42-、CO32- D. Ba2+、Na+、Cl-、SO42- |
|
| 19. 选择题 | 详细信息 |
|
“脚印”“笑脸”“五环”等焰火让北京奥运会开幕式更加辉煌壮观,这些五彩缤纷的焰火与元素的焰色反应有关。下列说法错误的是( ) A. 观察K2SO4的焰色应透过蓝色的钴玻璃 B. Na与NaCl在灼烧时火焰颜色相同 C. 可以用焰色反应来区别NaCl和KCl D. 焰色反应一定发生化学变化 |
|
| 20. 选择题 | 详细信息 |
|
工业上可利用“3MnO2+4Al A. MnO2被氧化 B. Al2O3是氧化剂 C. Mn失去电子 D. Al是还原剂 |
|
| 21. 选择题 | 详细信息 |
|
设NA表示阿伏加德罗常数的值,下列说法正确的是( ) A. 5.6gFe和足量的盐酸完全反应失去电子数为0.2NA B. 22.4LSO2含有NA个SO2分子 C. 1.6gCH4所含的电子数为NA D. 标况下,4.48L的水中含有H2O分子的数目为0.2NA |
|
| 22. 选择题 | 详细信息 |
|
ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。可通过以下反应制得:2KClO3+H2C2O4+H2SO4 A. H2C2O4是还原剂 B. KClO3在反应中失电子 C. KClO3被还原 D. H2SO4发生氧化反应 |
|
| 23. 选择题 | 详细信息 |
实验室用如图所示的装置蒸馏海水,下列说法正确的是( )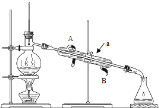 A. 蒸馏烧瓶中加入沸石的作用是防止暴沸 B. 实验时冷却水应从A进入,从B流出 C. 锥形瓶中能收集到高浓度的氯化钠溶液 D. 该装置可用于分离海水中的NaCl和MgCl2 |
|
| 24. 实验题 | 详细信息 |
|
选择下列实验方法分离物质,将分离方法的序号填在横线上。 A.萃取分液 B.过滤 C.分液 D.蒸发结晶 (1)_____分离饱和食盐水和沙子的混合物。 (2)_____将碘从碘水中提取出来。 (3)_____从硫酸钾溶液中得到硫酸钾固体。 (4)_____分离油和水。 |
|
| 25. 计算题 | 详细信息 |
| 3.2gO2和0.2molCO2,物质的量之比是___,同温同压下体积之比是_____。 | |
| 26. 实验题 | 详细信息 |
|
小王同学准备用CuSO4·5H2O配制500mL 1 mol/L的溶液。 (1)小王同学选用的玻璃仪器有:烧杯,玻璃棒,__________;________。 (2)玻璃棒在该实验中有重要的用途,分别是__________和 _________; (3)小王同学通过计算,用托盘天平称取________gCuSO4·5H2O。 (4)物质的量浓度误差(填偏高、偏低、无影响) ①若容量瓶中洗净后未干燥,残留少量水,则所配制的溶液浓度将_________; ②定容时,若眼睛俯视,则所配制的溶液浓度将___________; ③摇匀后以免低于刻度线,再加入少量水________。 |
|
| 27. 实验题 | 详细信息 |
氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按如下图所示步骤进行操作(注意事项:①所加试剂必须过量;②过量试剂必须除去;③不能引入新的杂质)。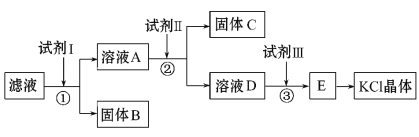 回答下列问题: (1)试剂Ⅰ的化学式为______,①中发生反应的离子方程式为_________。 (2)试剂Ⅱ的化学式为_______,②中加入试剂Ⅱ的目的是____________。 (3)试剂Ⅲ的名称是________,③中发生反应的离子方程式为__________。 |
|
| 28. 计算题 | 详细信息 |
|
取100mL的Na2CO3和Na2SO4混合溶液,加入适量Ba(OH)2溶液100 mL后,恰好完全反应,过滤、干燥后得到14.51g白色沉淀和滤液,再用过量稀硝酸处理沉淀,最后减少到4.66g,并有气体放出。计算: (1)求原混合液中Na2SO4的物质的量?__________________ (2)产生的气体在标准状况下的体积为多少?_________________ |
|
最近更新



