2018届九年级下半期一模考试化学题带答案和解析(江苏省淮安市博里镇初级中学)
| 1. | 详细信息 |
|
学习过程中,遇到的下列现象属于化学变化的是 A. 铅笔折断 B. 废纸撕碎 C. 笔盒生锈 D. 灯泡照明 |
|
| 2. | 详细信息 |
|
我国“化学”一词最早出于《化学鉴原》(1871年)。该书把一种元素翻译为“矽(xi)”。在地壳里,“矽”的含量在所有元素含量中占第二位,现代把这种“矽”元素命名为 A. 锡 B. 硒 C. 氧 D. 硅 |
|
| 3. | 详细信息 |
|
化学实验后我们要有清洗仪器的好习惯,以下清洗方法中,原理与另三种不同的是 A. 内壁有植物油的试管用洗洁精清洗 B. 内壁有碘的试管用酒精清洗 C. 用水清洗蒸发皿中的少量食盐 D. 用汽油除去衣服上的油污 |
|
| 4. | 详细信息 |
|
下列化学用语书写正确的是( ) A. 三个二氧化硫分子:2SO3 B. 两个氧分子:2O C. Co元素的化合价: |
|
| 5. | 详细信息 |
|
下列指定反应的化学方程式正确的是 A. 铝的自我保护: 4Al+3O2=2Al2O3 B. 酸雨形成的原因:CO2+H2O=H2CO3 C. 配制波尔多液:CaO+H2O+CuSO4=CaSO4+Cu(OH)2↓ D. 小苏打治疗胃酸过多:Na2CO3+2HCl=2NaCl+CO2↑+H2O |
|
| 6. | 详细信息 |
|
2018年1月19日,长征十一号固体运载火箭(以下简称长十一火箭)“一箭六星”发射任务圆满成功,固体运载火箭的一种常见的氧化剂是高氯酸铵(NH4ClO4),高氯酸铵分解能提供大量的气体,反应的化学方程式为2NH4ClO4 A. H2 B. H2O C. H2O2 D. HCl |
|
| 7. | 详细信息 |
北京新闻2018年2月22日,在平昌冬奥会短道速滑男子500米决赛中。武大靖勇夺中国体育代表团在本届奥运会上的首金。在剧烈的高强度运动中,人体有些部位会感到酸痛,这是因为体内产生了乳酸(化学式为C3H6O3),下列叙述错误的是 A. 乳酸是由三种元素组成的有机物 B. 乳酸中质量分数最大的是氧元素 C. 乳酸是由3个碳原子、6个氢原子、3个氧原子构成 D. 乳酸中三种元素的质量比和葡萄糖相同 |
|
| 8. | 详细信息 |
利用数字化实验可以形象地比较不同形状的碳酸钙与稀盐酸反应的速率。倾斜锥形瓶使试管内的稀盐酸流入瓶中与固体发生反应,瓶内气压的变化如曲线所示。 有关说法正确的是 A. 曲线①表示块状碳酸钙与稀盐酸反应 B. b点表示碳酸钙与盐酸反应已停止 C. 等质量的碳酸钙,粉末状的产生CO2的质量多 D. 对比分析点c、d可知,相同的气压时,粉状碳酸钙与稀盐酸反应速率更快 |
|
| 9. | 详细信息 |
|
下列图象不能正确反映对应变化关系的是 A.  向等质量的氧化钙、氢氧化钙中分别加入等质量分数的稀盐酸至过量 向等质量的氧化钙、氢氧化钙中分别加入等质量分数的稀盐酸至过量B. 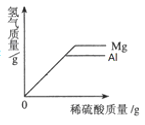 向等质量的镁、铝中分别加入等质量分数的稀硫酸至过量 向等质量的镁、铝中分别加入等质量分数的稀硫酸至过量C.  向一定质量氯化亚铁和氯化铝的混合溶液中加入镁粉至过量 向一定质量氯化亚铁和氯化铝的混合溶液中加入镁粉至过量D. 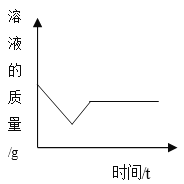 向一定量的饱和石灰水中加入少量氧化钙 向一定量的饱和石灰水中加入少量氧化钙 |
|
| 10. | 详细信息 |
|
“化学就在我们身边”。通过一次全家春游,小昕对这一观点有了更深的体会。 (1)旅游前,妈妈准备了矿泉水、咸鸭蛋、面包、方便面、桔子等食品,桔子中的营养素主要是_____。 (2)开始准备午餐,爸爸用户外便携式煤气炉做饭,小昕发现连接气炉与便携式天然气罐的是一段塑料导气管,它属于_____材料。 (3)做好饭后,小昕将煤气的阀门关闭,其灭火的原理是_____。 |
|
| 11. | 详细信息 |
|
习主席在十九大报告中指出“绿水青山就是金山银山”。中学生要知道: (1)减少污染物排放﹣﹣空气清新 防治大气污染,改善空气质量的根本措施是_____。 A 植树造林 B 控制污染物排放 C 实施人工降雨 D 喷洒空气清新剂 (2)自来水来之不易﹣﹣节约用水 自来水生产流程: 通常加入氯气的作用是杀菌消毒,原理是_____。 (3)清洁高效能源﹣﹣天然气 天然气充分燃烧的化学方程式中,不存在的物质种类是_____。 A 单质 B 氧化物 C 盐 D 有机物 |
|
| 12. | 详细信息 |
化学的发展为人类解决能源危机带来了曙光。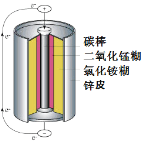 (1)化学电池是一种高效利用能源的装置,电池在使用时的能量转化形式是__。 (2)电池材料中的糊状电解质中含有淀粉,我们可以用___(填试剂名称)来检验。 (3)电解液中的氯化铵,在农业生产中可做___肥。 (4)锌皮的成分为金属锌(含有少量的铁),取少量锌皮放入盛有一定量CuSO4溶液的烧杯中,充分反应后过滤,当滤渣中只含一种物质时,滤液中一定含的溶质有___(写化学式)。 |
|
| 13. | 详细信息 |
|
多角度认识物质的变化,有助于我们更好地理解化学知识。 (1)从微观角度:(图1为某化学反应的微观示意图,据图回答下列问题)  ①微观上看,该化学变化中发生根本改变的微粒是___________(选填“原子”或“分子”)。 ②参加反应的A2与B2两种物质的分子个数比为_______________。 (2)从能量变化角度:(借用图2装置分别进行下列实验,认识物质变化中的能量变化) ①往烧杯中加人一定量生石灰会引起白磷燃烧,从燃烧条件分析,此时生石灰的作用是_______________; ②将一定量的下列某物质溶于烧杯中的冷水,其中能引起白磷燃烧的是______(选填字母序号)。 A.氯化钠 B.硝酸铵 C.浓硫酸 D.氢氧化钠 |
|
| 14. | 详细信息 |
甲、乙两种固体物质的溶解度曲线如下图所示。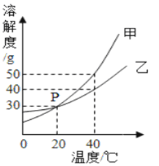 (1)40℃时,甲的饱和溶液中溶质与溶液的质量比为_________(用最简整数比表示) (2)将40℃等质量的甲、乙饱和溶液降温到20℃,所得溶液有关量甲<乙的是_____。 A 溶质质量分数 B 溶液质量 C 溶质质量 D 溶剂质量 (3)50℃时,将等质量甲、乙两种物质加入到等质量的水中,充分振荡后,所得溶液质量的大小关系为:甲_____乙(填“>”、“<”、“=”、“≥”、“≤”)。 |
|
| 15. | 详细信息 |
黄铜矿(主要成分是CuFeS2)经初步处理后,所得溶液甲中溶质为Fe2(SO4)3、CuSO4及H2SO4。某同学通过废铁屑与溶液甲反应,制取补血剂原料碳酸亚铁并回收铜。主要步骤如图所示[Fe2(SO4)3+Fe═3FeSO4]: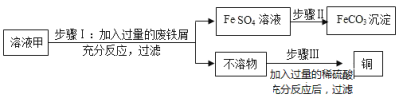 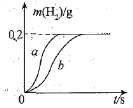 图1 图2 (1)步骤Ⅰ加入的废铁屑中含有少量铁锈,但对产物的成分没有影响,原因是_____. (2)步骤Ⅱ中加入一种可溶性试剂可实现其转化,该试剂可以是_____。 (3)为了测定步骤Ⅲ中所用稀硫酸的溶质质量分数,该同学取两份相同溶质质量分数的稀硫酸各100g,分别加入等质量的铁和锌,相同条件下充分反应,产生氢气的质量随时间变化的曲线如图2所示,则下列说法正确的是_____。 A 表示锌和稀硫酸反应的情况的是曲线a B 稀硫酸的溶质质量分数为9.8% C 加入铁的质量至少有5.6g D 加入锌的质量可能是13g |
|
| 16. | 详细信息 |
如图是实验室制取气体的部分装置,请根据实验装置(部分固定装置已省略)回答问题: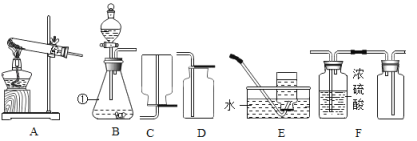 (1)图中标识①仪器的名称是:_____; (2)用A装置制取氧气的化学方程式为:_____; (3)实验室既可以制取CO2,又可以制取O2的发生和收集装置组合为:_____(在A﹣E中选)。 (4)若用F装置收集一瓶干燥的某气体,则该气体可能是_____(填字母代号) A NH3 B H2 C O2 D CH4 E CO2 |
|
| 17. | 详细信息 |
|
味精是常用的调味品,它的鲜味来自于其中的主要成分“谷氨酸钠”(化学式是C5H8NO4Na,易溶于水,与AgNO3不反应),另外还含有NaCl(其他成分不考虑)。某兴趣小组配制味精溶液并测定NaCl质量分数,请回答下列问题: (1)称取5.0g味精配制成50g溶液,量取蒸馏水的量筒规格是_____(填字母)。 A 10mL B 50mL C 100mL (2)如图是配制过程,正确的操作顺序为_____(填序号)。 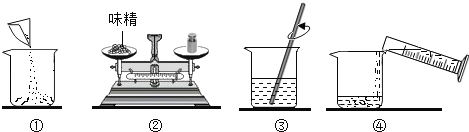 (3)为测定味精中NaCl的质量分数,进行如下实验:向所配制的50g溶液中加入AgNO3溶液充分反应后,过滤、洗涤、干燥、称量沉淀并计算。(提示:NaCl+AgNO3=NaNO3+AgCl↓) 检验过滤所得沉淀已洗涤干净的操作方法是_____。 (4)计算后发现NaCl的质量分数偏低,则可能的原因是_____(填字母)。 A 配溶液时仰视量水 B 过滤时待滤液面高于滤纸边缘 C AgNO3溶液量不足 |
|
| 18. | 详细信息 |
|
小刚、小军、小红对一份久置的NaOH白色粉末的成分进行探究并测定其成分的含量。 (一)成分的确定:小红设计了如图1所示实验方案: 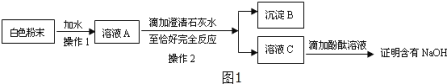 (1)在操作1中要用到玻璃棒,其作用是_____;在操作2中得到沉淀B,写出生成沉淀B的化学方程式_____。 (2)小刚认为小红的这个方案有问题,不能证明含有NaOH,但只要稍加改进,就可以证明粉末中还含有NaOH,则小刚改进的方法是_______。小刚对小红的实验作了正确的改进后进行了实验,实验现象和小红的一致,由此确定固体中含有NaOH。 (二)各成分含量的测定: 小军同学利用电子天平做了如图2所示测定生成CO2的质量实验。 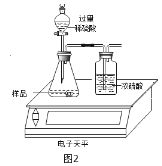 (1)写出锥形瓶中发生反应化学方程式:_____。 (2)有同学提出按上述实验所测得试样中Na2CO3质量分数会偏小,该同学的理由是______(实验操作均正确). (3)根据反应的化学方程式分析,NaOH部分变质或全部变质,与没有变质前的NaOH相比,恰好完全反应时消耗硫酸的量_____(填“相等”、“大于”或“小于”)。 |
|
最近更新



