2020年山东省日照市莒县中考一模化学考试完整版
| 1. 选择题 | 详细信息 |
|
春节是我国最盛大的传统节日。春节活动的内容丰富多彩、形式多样、热闹喜庆。下列活动过程中一定发生化学变化的是( ) A. 打年糕 B. 剪窗花 C. 放烟花 D. 写春联 |
|
| 2. 选择题 | 详细信息 |
下图是甲转化为丁的微观过程。下列说法正确的是( )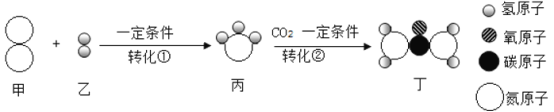 A. 转化①中原子种类不变,个数改变 B. 转化②是化合反应 C. 整个过程中共有2种氧化物 D. 物质丁是复合肥 |
|
| 3. 选择题 | 详细信息 |
|
近年来一些手机厂商纷纷发布自己的可折叠手机。化学物质吡唑啉是生产折叠手机用到的柔性屏幕的重要物质,其化学式为C3H4N2,下列有关吡唑啉C3H4N2 的说法正确的是() A.吡唑啉属于有机高分子化合物 B.吡唑啉是由3个碳原子、6个氢原子和2个氮原子构成的 C.吡唑啉中碳元素质量分数最大 D.吡唑啉的化学式量为70g |
|
| 4. 选择题 | 详细信息 |
|
下列物质在水溶液中能大量共存的是 A. NaCl Na2CO3H2SO4 B. CuSO4KNO3Na2SO4 C. BaCl2NaOH Na2CO3 D. HCl Na2SO4NaOH |
|
| 5. 选择题 | 详细信息 | ||||||||
化学与人类的生活密切相关。下列对化学知识的应用归纳完全正确的一组是
|
|||||||||
| 6. 选择题 | 详细信息 | |||||||||||||||
除去下列物质中的少量杂质,下列实验方案不能达到目的的是( )
|
||||||||||||||||
| 7. 选择题 | 详细信息 | |||||||||||||||
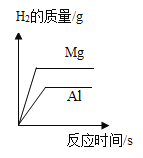
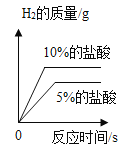
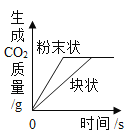
影响化学反应速率的因素很多。下列图像表达的化学反应过程,与实际情况不相符的是( )
|
||||||||||||||||
| 8. 选择题 | 详细信息 |
|
提升“中国芯”的性能是我国信息产业的当务之急。“中国芯”的核心材料是高纯度的单质硅,工业上制取粗硅的化学方程式为:SiO2+2C A. 硅元素在地壳中的含量比氧元素多 B. 该反应的基本类型为置换反应 C. 在此反应中硅元素的化合价升高 D. 该反应体现了碳的氧化性 |
|
| 9. 选择题 | 详细信息 |
|
有一种含CaCO3与CaO的混合物,测得其中钙元素的质量分数为50%,取该混合物16g,经高温煅烧后,将剩余固体投入足量的水中,固体全部溶解生成Ca(OH)2,则生成Ca(OH)2的质量为( ) A.14.8g B.22.2g C.7.4g D.3.7g |
|
| 10. 填空题 | 详细信息 |
如图中A是锡元素在周期表中的信息,B、C分别为两种粒子的结构示意图,D为元素周期表中的部分信息,请根据图中信息回答。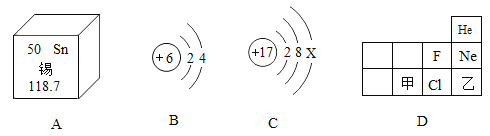 (1)锡元素的相对原子质量是_____。 (2)B表示的原子,其核外电子数是_____。若C表示氯离子,则X=_____。 (3)元素在周期表中的分布是有规律的,D中甲的原子序数_____(填“大于”或“小于”)乙的原子序数。乙所代表的元素,属于_____(填“金属”或“非金属”)元素。 |
|
| 11. 填空题 | 详细信息 |
|
对下面四个常见的化学反应进行对比 分解反应: 置换反应: 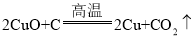 复分解反应: 化合反应:  请从以下各项中选择恰当的内容,用对应的序号填空: ①元素的种类;②原子的种类;③原子的个数;④分子的种类;⑤物质的组成(或结构);⑥物质的总质量;⑦元素的化合价 在化学反应过程中,一定发生变化的是_____;可能发生变化的是_____。 |
|
| 12. 填空题 | 详细信息 |
图是甲、乙两种物质的溶解度曲线,请结合图回答问题: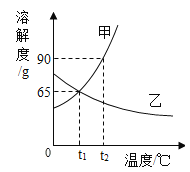 (1)_____℃时,甲、乙两种物质的溶解度相等。 (2)溶解度随温度升高而降低的物质是__________(填“甲”或“乙”)。 (3)可使甲物质从其饱和溶液中结晶析出的方法是_________。 (4)t2℃时,分别将甲、乙两种物质的饱和溶液降温到t1℃,甲溶液的溶质质量分数______(填“大于”、“等于”或“小于”)乙溶液的溶质质量分数。 (5)小明同学用甲物质进行以下实验: 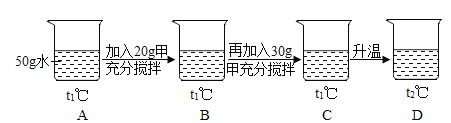 ①实验过程中,B、C、D对应的溶液为不饱和溶液的是____________________。 ②向B对应的溶液中再加入30g甲固体的过程中,发现固体全部溶解,一段时间后又有部分固体析出。你认为“全部溶解”的原因是________________________________________。 |
|
| 13. 推断题 | 详细信息 |
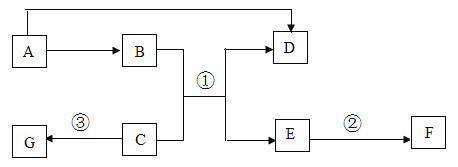 (1)写出物质D的化学式:________。 (2)反应②的现象是:________________。 (3)反应③的化学方程式:________。(只写一种) |
|
| 14. 科学探究题 | 详细信息 | ||||||||||||||||
|
潜水器中可使用过氧化钠(Na2O2)固体做供氧剂,过氧化钠固体与二氧化碳反应原理是:2Na2O2+2CO2═2Na2CO3+O2,为验证该反应产物,某兴趣小组进行如下实验探究。 (查阅资料)过氧化钠与水反应生成氢氧化钠和氧气。 (设计实验)小组同学利用如图装置进行实(忽略稀盐酸的挥发)。 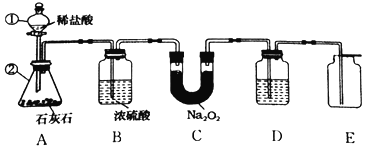 (1)装置A中标号仪器名称:①________,②________。 (2)装置A中反应的化学方程式为________。 (3)装置B的作用是________。 (4)为防止装置E收集的氧气中混有二氧化碳,装置D中盛放的试剂是________溶液。 (5)验证过氧化钠与二氧化碳反应产物
|
|||||||||||||||||
| 15. 计算题 | 详细信息 |
现有含CuSO4和H2SO4的混合溶液,向其中加入一定溶质质量分数的NaOH溶液,实验过程中,生成沉淀的质量与加入NaOH溶液的质量关系如图所示: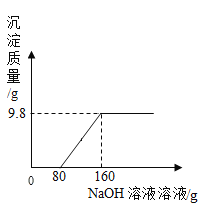 (1)恰好完全反应时,产生沉淀的质量_____g; (2)求混合液中CuSO4的质量;_____ (3)求该NaOH溶液的溶质质量分数。_____ |
|
最近更新