2016辽宁九年级下学期人教版初中化学月考试卷
| 1. | 详细信息 |
|
下列变化中属于化学变化的是( ) A.滴水成冰 B.铁杵成针 C.热胀冷缩 D.百炼成钢
|
|
| 2. | 详细信息 |
|
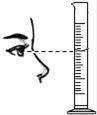
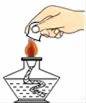
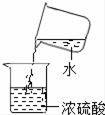
下列实验操作不合理的是( ) A. 读取液体体积 B. 熄灭酒精灯 C. 取用固体粉末 D. 稀释浓硫酸
|
|
| 3. | 详细信息 |
|
如图所示是两种气体发生化学反应的微观示意图,其中相同的球代表同种原子,下列说法正确的是( )
A.化学反应前后原子的种类不变 B.生成物一定是氧化物 C.化学反应前后分子的种类不变 D.该反应属于置换反应
|
|
| 4. | 详细信息 |
|
以下的“水”属于纯净物的是( ) A.雨水 B.矿泉水 C.海水 D.蒸馏水
|
|
| 5. | 详细信息 |
|
下列洗涤方式应用乳化作用的是( ) A.用汽油除去衣服上的油污 B.用水洗去盘子中的水果渣 C.用洗洁精清洗餐具上的油污 D.用盐酸清洗水壶的水垢
|
|
| 6. | 详细信息 |
|
铁及其合金在人类生产、生活中占据着重要的地位.下列说法正确的是( ) A.铁在干燥的空气中容易生锈 B.铁元素是地壳中含量最多的金属元素 C.铁丝在氧气中燃烧生成氧化铁 D.生铁的含碳量比钢的含碳量高
|
|
| 7. | 详细信息 |
|
市售加碘盐是在食盐中加入一定量的碘酸钾(KIO3),KIO3中碘元素的化合价是( ) A.+5 B.﹣1 C.+3 D.+1
|
|
| 8. | 详细信息 |
|
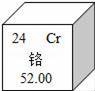
自行车钢圈常常会镀铬,如图是铬在元素周期表中的信息,下列说法不正确的是( )
A.自行车钢圈镀铬可使钢圈更美观 B.自行车钢圈镀铬可防止钢圈锈蚀 C.图中信息说明铬元素在地壳中的含量为52.00% D.图中信息说明铬元素的原子核外有24个电子
|
|
| 9. | 详细信息 |
|
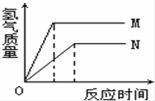
等质量的M、N两种金属片,分别与相同浓度的足量稀盐酸反应(已知M、N在生成物中均为+2价),生成氢气的质量和反应时间的关系如图所示,下列叙述正确的是( )
A.生成H2 的质量M<N B.N消耗的稀盐酸比M消耗的多 C.相对原子质量较大的是N D.产生H2 的快慢程度N>M
|
|
| 10. | 详细信息 |
|
某学生为了验证铁、锌、铜三种金属的活动性顺序,设计了四种方案:①将Zn、Cu分别加入到FeSO4溶液中;②将Zn、Cu分别加入到ZnSO4溶液中;③将Fe分别加入到FeSO4、CuSO4溶液中;④将Fe分别加入到ZnSO4、CuSO4溶液中.其中可行的是( ) A.①④ B.①② C.②③ D.③④
|
|
| 11. | 详细信息 |
|
向含有AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一定量的铁粉,使其充分反应后,过滤,向滤渣中滴加稀盐酸,有气泡产生,则下列结论正确的是( ) A.滤液中一定含Ag+、Cu2+、Zn2+、Fe2+ B.滤液中一定含Fe2+,可能含Zn2+ C.滤液中一定含Fe2+,Zn2+,不含Cu2+,Ag+ D.滤液中一定含Zn2+、Fe2+,可能含Cu2+
|
|
| 12. | 详细信息 |
|
根据化学方程式4NH3+5O2═4X+6H2O,可推断X的化学式是( ) A.NO B.NO2 C.N2O3 D.NH3
|
|
| 13. | 详细信息 |
|
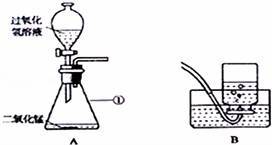
如图是某同学设计的实验室制取氧气的实验装置图,请回答下列问题: (1)分液漏斗的优点: (2)二氧化锰在该化学反应中的作用是 (3)组装好A装置后,该同学先向分液漏斗中加入水,然后将导管另一端浸入水中,并打开分液漏斗的活塞,观察导管口是否有连续的气泡冒出,该操作的目的是 . (4)A装置中发生反应的化学方程式为 ,氧气能用B图收集的原因是 ,应将收集满氧气的集气瓶 放在桌面上.
|
|
| 14. | 详细信息 |
|
用化学用语填空: (1)甲烷 (2)3个亚铁离子 (3)氦原子 (4)氯酸钾 .(5)五个碳酸根离子 ﹣ (6)硫酸中硫元素的化合价 . |
|
| 15. | 详细信息 |
|
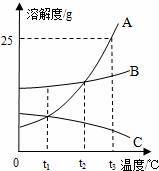
A、B、C三种固体物质在水中的溶解度曲线如图所示,请回答: (1) ℃时,A、B两种物质在100g水中达到饱和状态时溶解的质量相等; (2)若B中混有少量的A,最好采用 的方法提纯B; (3)现有接近饱和的C物质溶液,使其变成饱和溶液的方法有:①加入C物质;②恒温蒸发溶剂;③ ; (4)t3℃时将20g A物质放入50g水中,充分搅拌,所得溶液中溶质的质量分数是 ; (5)将t3℃时等质量的A、B、C三种物质的饱和溶液降温至t1℃时,所得溶液的质量由大到小的顺序是 .
|
|
| 16. | 详细信息 |
|
水是人类宝贵的自然资源,与人类的生产、生活密切相关. (1)水是常见的溶剂,将下列生活中的物质分别放入水中,不能形成溶液的是 . A.蔗糖 B.纯碱 C.食盐 D.花生油 (2)“节约用水,从我做起”.请你写出一种生活中节约用水的做法 . (3)为了保护水质,下列做法合理的是 . A.随意丢弃废旧电池 B.生活污水经处理达标后排放 C.农业上合理使用农药、化肥 D.工业“三废”未经处理任意排放 (4)通过电解水实验,可以知道水是由 组成. (5)生活中降低水的硬度的常用方法是 . (6)净化水的常用方法有:①消毒杀菌 ②过滤 ③蒸馏 ④活性炭吸附 ⑤加明矾吸附沉降.天然水中往往含有许多杂质,要把天然水净化成生活中的自来水,所选用的净化方法按净化过程排序是(填序号) .
|
|
| 17. | 详细信息 |
|
请回答下列各问: (1)登山、潜水、医疗急救时都需要用氧气,是因为氧气 ; 实验室用高锰酸钾制氧气的化学方程式 . (2)用化学方程式回答: 稀硫酸除铁锈: ; 不在溶液中发生的置换反应: . (3)野炊时,人们常把柴草架空,使燃烧更旺,请说明其中的道理: .
|
|
| 18. | 详细信息 |
|
根据金属活动顺序表的有关知识,回答下列问题: (1)用Mg、Zn、Cu三种金属分别于稀盐酸反应,根据金属与稀盐酸反应的 ,可以判断金属活动性强弱的顺序. (2)用Zn分别与MgCl2、CuCl2溶液反应,也能判断金属活动性顺序,其反应的化学方程式为 ,三种金属活动性由强到弱的顺序为 .若将一定质量的Zn放入CuCl2和MgCl2的混合溶液中,充分反应后过滤,所得固体中一定含有的物质是 .
|
|
| 19. | 详细信息 |
|
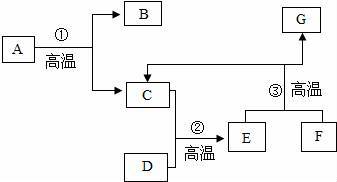
工业上以大理石和赤铁矿为主要原料可以制取B和G,其转化关系如图所示, 已知D、G的主要成分为单质.试回答下列问题: (1)写出工业制取的两种物质的化学式:B 、G . (2)写出下列反应的化学方程式: 反应② ; 反应③: ; 检验气体C:.
|
|
| 20. | 详细信息 |
|
每到冬天,市场上便有一种“热宝”出售,它是一个装有化学药品的小袋.使用时,撕去它的保护膜贴在身体上,不久便会产生热量.已知小袋中装有铁粉、碳粉和少量氯化钠. (1)取小袋内物质,加入稀盐酸中,发生反应的化学方程式为: . (2)将袋内物质放在足量O2中燃烧,写出反应的化学方程式: ① ;② . (3)将袋内物质加入一定量的CuSO4溶液中,充分反应后过滤,滤液中的溶质一定有 (填写名称).
|
|
| 21. | 详细信息 |
|
如图是小明配制100g溶质质量分数为12%的NaCl溶液的有关实验操作示意图.
(1)配制过程中使用的四种玻璃仪器,分别是 、 、 、 . (2)请你指出图中一处错误操作,并分析该操作可能造成的后果. . (3)图②、图③表示的操作步骤分别是 .配制时需称量氯化钠 g,如果氯化钠中含有少量不溶的杂质,溶质的质量分数会 (填“偏大”或“偏小”);量取水最好选择 的量筒(填序号①10mL②50mL③100mL).(水的密度为1g/cm3)
|
|
| 22. | 详细信息 |
|
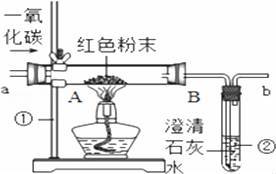
如图是课堂中模拟炼铁的实验装置. (1)写出图中标有序号的仪器名称:① ,② . (2)实验过程中,先要进行的是 .(选填“I”或“II”) I.加热Ⅱ.通一氧化碳 (3)A中反应的化学方程式是 ,A中观察到的现象是 ;B中反应的化学方程式是 , B中观察到的现象是 . (4)该实验的缺点是 .
|
|
| 23. | 详细信息 |
|
某课外小组进行“测定黄铜(铜锌合金)中锌、铜的质量分数”探究.现称取20g块状黄铜样品置于足量的稀盐酸中,待反应完全后,过滤、洗涤、干燥,得固体8.5g.计算: (1)该样品中锌的质量分数; (2)产生氢气的质量.
|
|