2019届九年级下学期中考模拟化学(河北省邢台市第八中学)
| 1. | 详细信息 |
|
下列化学用语与对应表述相符的是( ) A. 2个硫酸根离子——2SO C. 3个氧原子——O3 D. 氧化镁——MgO2 |
|
| 2. | 详细信息 |
|
下列有关实验操作中正确的是( ) A. 称量NaCl  B. 添加酒精 B. 添加酒精 C. 收集氧气 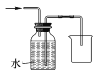 D. 用力塞紧橡皮塞 D. 用力塞紧橡皮塞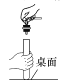 |
|
| 3. | 详细信息 |
|
用微粒的观点解释下列现象,不正确的是( ) A. 1个水分子质量约为3×10-26kg——分子的质量很小 B. 闻到远处饭菜的香味——分子在不断地运动 C. 冰块难于压缩——分子间隔小 D. 夏天室外电线变长——原子受热时体积变大 |
|
| 4. | 详细信息 |
取等质量的A、B金属,分别投入溶质质量分数相同的足量的盐酸中,生成氢气的质量(m)与时间(t)的关系如图。(已知A、B元素在生成物中的化合价相同)下列说法正确的是 A.金属活泼性:A>B B.t1时,产生氢气的质量B<A C.两种金属原子的相对原子质量A>B D.t2时,A、B金属均没有剩余 |
|
| 5. | 详细信息 | |||||||||||||||
在一密闭容器里放入四种物质,使其在一定条件下充分反应,测得数据如下:
|
||||||||||||||||
| 6. | 详细信息 |
|
请沿用科学家认识事物的方式认识“空气”。 (1)从分类角度:空气属于______(填“混合物”或“纯净物”)。 (2)从变化角度:已知:常压下,氮气沸点-196℃,氧气沸点-183℃。常温下将燃着的木条置于盛满液态空气的烧杯口,观察到的现象是_____。将该烧杯放置一段时间后,液态物质剩余约1/10体积,其主要成分是_____。 (3)从应用角度:利用空气制取氮肥的流程如图所示。 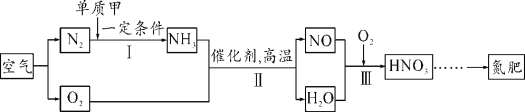 ①Ⅰ中参加反应的单质甲为_____。 ②Ⅱ中反应的化学方程式为______。 |
|
| 7. | 详细信息 |
“黄铜”是铜锌合金,可塑性好,耐腐蚀,许多“金色”饰品就是用它来制作的。现称取20.0g黄铜样品置于烧杯中,慢慢加入稀硫酸使其充分反应,直至没有气泡产生为止,请结合下列图示计算。 (1)该20.0g黄铜样品中含锌的质量为____g。 (2)完全反应时生成硫酸锌的质量是______克。 |
|
最近更新



