2019-2020年高三12月月考化学考试完整版(河北省宣化市第一中学)
| 1. 选择题 | 详细信息 |
由塑化剂引起的食品、药品问题受到广泛关注。下列关于塑化剂DBP(结构如下图)的说法不正确的是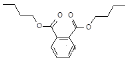 A.属于芳香族化合物,能溶于水 B.其核磁共振氢谱共有6种吸收峰 C.分子中一定有12个原子位于同一平面上 D.水解得到的酸性产物能与乙二醇发生缩聚反应 |
|
| 2. 选择题 | 详细信息 |
|
下列关于物质分类的说法正确的是 A.油脂、糖类、蛋白质均是天然高分子化合物 B.三氯甲烷、氯乙烯、三溴苯酚均是卤代烃 C.CaCl2、烧碱、聚苯乙烯均为化合物 D.稀豆浆、硅酸、雾霾均为胶体 |
|
| 3. 选择题 | 详细信息 |
|
下列离子方程式正确的是 A.向Fe(NO3)3溶液中滴入少量的HI溶液:2Fe3++2I-==2Fe2++I2 B.向苯酚钠溶液中通入少量CO2气体:2C6H5O-+CO2+H2O→2C6H5OH↓+CO32- C.Cu(OH)2沉淀溶于氨水得到深蓝色溶液:Cu(OH)2+4NH3== [Cu(NH3)4]2++2OH- D.澄清石灰水中加入少量NaHCO3溶液:Ca2++2OH-+2HCO3-==CaCO3↓+CO32-+2H2O |
|
| 4. 选择题 | 详细信息 |
短周期主族元素R、T、Q、W在元素周期表中的相对位置如图所示,T元素的最高正价与最低负价的代数和为0。下列判断正确的是 A.原子半径的大小:W>Q>R B.气态氢化物的稳定性:R>Q>T C.对应含氧酸的酸性强弱:W>Q>T D.R分别与T、Q、W形成化合物的晶体均为分子晶体 |
|
| 5. 选择题 | 详细信息 |
|
设NA为阿伏加德罗常数的值,下列说法错误的是( ) A.1 mol B.3.6 g石墨和C60的混合物中,含有的碳原子数为0.3NA C.含有4.6 g钠元素的过氧化钠和氧化钠的混合物中,所含离子总数为0.3NA D.标准状况下,4.48 L戊烷含有的分子数为0.2NA |
|
| 6. 选择题 | 详细信息 |
肼(H2N-NH2)和偏二甲肼 [ H2N-N(CH3)2 ] 均可用作火箭燃料。查阅资料得知,肼是一种良好的极性溶剂,沿肼分子球棍模型的氮、氮键方向观察,看到的平面图如下图所示。下列说法不正确的是 A.肼分子中的氮原子采用sp3杂化 B.肼分子中既有极性键又有非极性键 C.肼分子是非极性分子 D.肼与偏二甲肼互称同系物 |
|
| 7. 推断题 | 详细信息 |
|
已知元素X、Y、Z、W、R为前四周期元素,且原子序数依次增大。X基态原子核外有三个未成对电子,Z、W分别是短周期中电负性最大和最小的元素;R2+离子的3d轨道中有三对成对电子。请回答下列问题: (1)R基态原子的电子排布式为__________,元素X、Y、Z的第一电离能由大到小的顺序为(用元素符号表示)___________________。 (2)化合物XZ3的空间构型为______,R2+与NH3形成的配离子中,提供孤对电子的是_____。 (3)Z的氢化物由固体变为气态所需克服的微粒间的作用力是________。 (4)Z、W、R形成某种化合物的晶胞结构如右图所示,其化学式为___________。 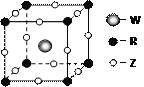 (5)XY2-能被酸性KMnO4溶液氧化,其中MnO4-被还原为Mn2+,反应的离子方程式是________________。 |
|
| 8. 实验题 | 详细信息 | ||||||||||||||||
溴苯是一种化工原料,某兴趣小组用如下装置制备溴苯并证明苯和液溴发生的是取代反应,而不是加成反应。 有关数据如下:
|
|||||||||||||||||
| 9. 推断题 | 详细信息 |
苯佐卡因(E)可用于化妆品紫外线吸收,局部麻醉药等。根据下面的反应路线可以实现苯佐卡因的制备及对糖厂甘蔗渣进行综合利用。 请回答下列问题: (1)反应Ⅰ的化学方程式是_______________。 (2)B的名称是_____________,C中含有的官能团名称是______________。 (3)在反应Ⅰ~Ⅴ中,属于取代反应的是(填序号)________。 (4)写出反应Ⅴ的化学方程式:____________________________。 (5)苯佐卡因有多种同分异构体,其中,氨基直接连在苯环上,苯环上的一氯取代物只有一种的羧酸类同分异构体的结构简式为:_________________。 |
|
| 10. 综合题 | 详细信息 |
|
CuCl是应用广泛的有机合成催化剂,也在染料工业中用作实效型气体吸收剂。利用废旧印刷电路板制氯化亚铜可减少污染、实现资源再生。请回答下列问题: (1)废旧印刷电路板经粉碎分离能得到金属粉末,控制其他条件相同,用10%H2O2和3.0mol·L-1 H2SO4的混合溶液处理印刷电路板的金属粉末,测得不同温度下铜的平均溶解速率如图所示。在H2SO4溶液中,Cu与H2O2反应生成Cu2+和H2O的离子方程式为______。当温度高于40℃时,铜的平均溶解速率随着反应温度升高而下降,其主要原因是______。 (2)工业上常用CuSO4来制备CuCl。在提纯后的CuSO4溶液中加入一定量的Na2SO3和NaCl,加热,生成CuCl沉淀,该反应的离子方程式是__________。 (3)在盐酸中CuCl能吸收CO,发生的反应为 CuCl+CO+H2O (4)工业制备CuCl需要配制质量分数为20.0%的CuSO4溶液(密度为1.2 g·cm-3),配制该溶液所需CuSO4·5H2O与H2O的质量之比为_______,所得溶液的物质的量浓度为______。 (5)工业检测CuCl产品的纯度需要80mL0.5mol/L的FeCl3溶液,配制该溶液所需仪器除托盘天平(含砝码、质量相同的两纸片)、烧杯外,还必需___________________。 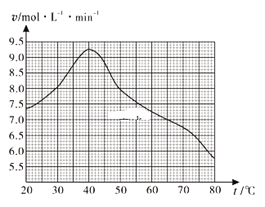 |
|
最近更新



