2019-2020年高二上册期中考试化学免费试卷完整版(安徽省黄山市“八校联盟”)
| 1. 选择题 | 详细信息 |
|
下列电离方程式书写正确的是( ) A.NaHCO3 = Na++H++CO32- B.(NH4)2SO4 C.H2S D.Al(OH)3 |
|
| 2. 选择题 | 详细信息 |
|
下列说法正确的是 A.化学反应除了生成新的物质外,还伴随着能量的变化 B.据能量守恒定律,反应物的总能量一定等于生成物的总能量 C.放热的化学反应不需要加热就能发生 D.吸热反应不加热就不会发生 |
|
| 3. 选择题 | 详细信息 |
把镁条投入到盛有盐酸的敞口容器中,产生H2的速率可由如图2-1-1表示,在下列因素中,①盐酸的浓度,②镁条的表面积,③溶液的温度,④氯离子的浓度,影响反应速率的因素是( )。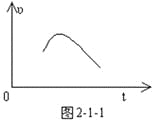 A.①④ B.①②③ C.③④ D.②③ |
|
| 4. 选择题 | 详细信息 |
|
已知 H2(g) + Cl2 (g)===2HCl(g) Δ H =- 184.6 kJ · mol-1则反应:HCl(g)===1/2H2(g)+1/2Cl2(g)的ΔH 为( ) A.+184.6 kJ·mol-1 B.-92.3 kJ·mol-1 C.-369.2 kJ·mol-1 D.+92.3 kJ·mol-1 |
|
| 5. 选择题 | 详细信息 |
|
对于反应A(g)+3B(g)=4C(g)+2D(g),在相同时间内,用不同物质表示的平均反应速率如下,则反应速率最快的是 ( ) A. C. |
|
| 6. 选择题 | 详细信息 |
|
在一定温度下,可逆反应A(g)+3B(g)≒2C(g)达到平衡的标志是( ) A.C的生成速率与C的分解速率相等 B.单位时间生成nmolA,同时生成3nmolB C.A、B、C的浓度不再变化 D.A、B、C的分子数比为1:3:2 |
|
| 7. 选择题 | 详细信息 |
|
下列说法正确的是( ) A. 可逆反应的特征是正反应速率和逆反应速率相等 B. 在其他条件不变时,使用催化剂只能改变反应速率,而不能改变化学平衡状态 C. 在其他条件不变时,升高温度可以使平衡向放热反应方向移动 D. 在其他条件不变时,增大压强一定会破坏气体反应的平衡状态 |
|
| 8. 选择题 | 详细信息 |
|
已知化学反应A2(g)+B2(g)===2AB(g) ΔH= Q kJ·mol-1, 其能量变化如图所示,则Q的值正确的是 ( )  A. a-b B. a C. -b D. b-a |
|
| 9. 选择题 | 详细信息 |
下列图像分别表示有关反应的反应过程与能量变化的关系。 据此判断下列说法中正确的是( ) A.石墨转变为金刚石是吸热反应 B.S(g)+O2(g) C.白磷比红磷稳定 D.CO(g)+H2O(g) |
|
| 10. 选择题 | 详细信息 |
|
对于反应C(s)+H2O(g) A. 平衡常数表达式为 C. 升高体系温度,平衡常数K减小 D. 增加C(s)的量,平衡正向移动 |
|
| 11. 选择题 | 详细信息 |
如图曲线 a 表示放热反应X(g)+Y(g)  A.升高温度 B.加大 X 的投入量 C.加催化剂 D.增大体积 |
|
| 12. 选择题 | 详细信息 |
|
CO2 与 H2 合成(CH3)2O(二甲醚)是煤化工中的重要反应,有关信息如下:2CO2(g)+6H2(g) A. 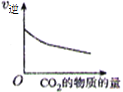 B. B. C.  D. D.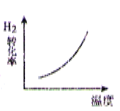 |
|
| 13. 选择题 | 详细信息 |
|
在密闭容器中发生如下反应: aX(g) + bY(g) ⇌cZ(g) +d W(g)。反应达平衡后保持温度不变,将气体体积压缩到原来的1/2,当再次达平衡时,W的浓度为原平衡时的1.8倍。下列叙述中不正确的是 ( ) A. 平衡向逆反应方向移动 B. a + b < c + d C. Z的体积分数增加 D. X的转化率下降 |
|
| 14. 选择题 | 详细信息 |
|
在醋酸的下列性质中,可以证明它是弱电解质的是 ( ) A. 1mol/L的醋酸溶液中H+浓度约为10-3mol/L B. 醋酸能与水以任意比互溶 C. 10mL 1mol/L的醋酸恰好与10mL 1mol/L NaOH溶液完全反应 D. 醋酸的导电性比强酸溶液弱 |
|
| 15. 选择题 | 详细信息 |
|
25℃时将水不断滴入0.1mol/L的氨水中,下列变化的图象合理的是 A.  B. B.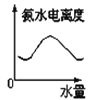 C. C. D. D.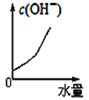 |
|
| 16. 选择题 | 详细信息 |
|
已知下列反应的平衡常数:①H2(g)+S(s) A. K1+K2 B. K1-K2 C. K1×K2 D. K1/K2 |
|
| 17. 填空题 | 详细信息 |
|
已知: ①CO(g)+1/2O2(g)== CO2(g) ΔH=-283.0kJ/mol ②C(s)+O2(g)==CO2(g) ΔH=-393.5kJ/mol 请写出 C 与 O2 反应生成 CO 气体反应的热化学方程式: _______________。 |
|
| 18. 填空题 | 详细信息 |
| 现有:①硫酸铜溶液②CO2③石墨④KOH⑤CH3COOH⑥NH3⑦NH3·H2O⑧NaHCO3其中属于强电解质的是_______(填序号,下同),属于弱电解质的是_____, 属于非电解质的是_________,既不是电解质,又不是非电解质的是_____。 | |
| 19. 填空题 | 详细信息 |
|
在恒容的密闭容器内,使 1molN2和3molH2 混合发生下列反应: 3H2+N2 (1) 升高温度时,混合气体的密度_____。(填:“变大”或“变小”或“不变”) (2)当达到平衡时,充入 N2,平衡将_____移动。(填:“正向”或“逆向”或“不”, 下同) (3)当达到平衡时,充入Ar气,平衡将_____移动。 (4)当达到平衡时,将 c(N2)、c(H2)、c(NH3)同时增大 1 倍,平衡将_____移动。 |
|
| 20. 填空题 | 详细信息 |
|
在一定温度下,现有三种酸:a.盐酸 b.硫酸 c.醋酸,现回答下面问题(注:填对应的字母) (1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是_____________。 (2) 若三者 c(H+ )相同时,物质的量浓度由大到小的顺序是________________。 (3)当三者 c(H+)相同且溶液体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序_______________ 。 (4)当 c(H+)相同、溶液体积相同时,同时加入形状、密度、质量完全相同的锌,则开始时反应速率的大小关系为_______________ 。 (5)将 c(H+)相同的三种酸均加水稀释至原来的 100 倍后,c(H+)由大到小的顺序是_____。 |
|
| 21. 实验题 | 详细信息 | ||||||||||||||||||||||
|
兴趣小组探究锌片与盐酸、醋酸反应时,浓度或温度对反应速率的影响,他们准备了以下化学用品:0.20mol/L与0.40mol/L的HCl溶液、0.2mol/L与0.40mol/L的CH3COOH溶液、0.10mol/LCuCl2、锌片(形状、大小、质量相同)、秒表、碳棒、导线、烧杯、几支试管和胶头滴管,酸液温度控制为298K和308K。 酸液都取足量、相同体积,请你帮助完成下面实验设计表(表中不留空格):
|
|||||||||||||||||||||||
| 22. 综合题 | 详细信息 |
在一恒容密闭容器中发生某化学反应2A(g) (1)在800℃时该反应的化学平衡常数K=_____。 (2)在实验Ⅰ中,反应在20min至40min内A的化学反应速率为_________。 (3)实验Ⅱ和实验Ⅰ相比,可能隐含的反应条件是_____。 (4)根据实验Ⅲ和实验Ⅰ的比较,可推测该反应降低温度,平衡向_____(填“正”或“逆”)反应方向移动,该正反应是__________(填“放热”或“吸热”)反应。 (5)与实验Ⅰ相比,若实验Ⅰ中的A的初始浓度改为0.8mol·L-1,其他条件不变,则达到平衡时所需用的时间_____实验Ⅰ(填“等于”、“大于”或“小于”)。 |
|
| 23. 综合题 | 详细信息 |
|
研究氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反 应: 2NO2(g)+NaCl(s) 2NO(g)+Cl2(g) (1)4NO2(g)+2NaCl(s) (2)为研究不同条件对反应(Ⅱ)的影响,在恒温条件下,向2L恒容密闭容器中加入0.2molNO和0.1molCl2,10min时反应(Ⅱ)达到平衡。测得10min内v(ClNO)=7.5×10-3mol·L-1·min-1,则平衡后n(Cl2)=________mol,NO的转化率α1=___________。其他条件保持不变,反应(Ⅱ)在恒压条件下进行,平衡时NO的转化率α2_____α1(填“>”“<”或“=”),平衡常数K2_____(填“增大”“减小”或“不变”)。若要使K2减小,可采用的措施是_________。 A.增大压强 B.减小压强 C.升高温度 D.降低温度 E.加催化剂 F.增加反应物的浓度 G.减少生成物的浓度 |
|
最近更新




