陕西2019年高三化学上册月考测验在线答题
| 1. 选择题 | 详细信息 |
|
下列我国古代的技术应用中,不涉及氧化还原反应的是 A. 煅烧贝壳  B. 粮食酿醋 B. 粮食酿醋 C. 古法炼铁  D. 火药爆炸 D. 火药爆炸 |
|
| 2. 选择题 | 详细信息 |
|
化学与人类生产、生活、社会可持续发展密切相关,下列说法正确的是( ) A. 凡含有添加剂的食物对人体健康均有害,不宜食用 B. “霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应 C. 人体缺乏铁元素,可以补充硫酸亚铁,且多多益善 D. “青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化 |
|
| 3. 选择题 | 详细信息 |
|
取一小块金属钠,放在燃烧匙里加热,下列实验现象描述不正确的是( ) A. 燃烧后得白色固体 B. 燃烧时火焰为黄色 C. 燃烧后生成淡黄色固体物质 D. 金属先熔化 |
|
| 4. 选择题 | 详细信息 |
|
将下列各组物质按酸、碱、盐分类顺次排列,其中正确的是( ) A.硫酸 纯碱 孔雀石[Cu2(OH)2CO3] B.硝酸 烧碱 绿矾[FeSO4•7H2O] C.醋酸 乙醇 碳酸钙 D.盐酸 熟石灰 苛性钠 |
|
| 5. 选择题 | 详细信息 |
|
下列变化必须加入还原剂才能实现的是( ) A. Na→Na2O2 B. Na→NaOH C. Zn→ZnCl2 D. CuO→Cu |
|
| 6. 选择题 | 详细信息 |
|
下列物质能使干燥的蓝色石蕊试纸先变红后褪色的是( ) ①氯气 ②液氯 ③新制的氯水 ④氯气的酒精溶液 ⑤盐酸 ⑥盐酸酸化的漂白粉溶液 A. ①②③ B. ①②③⑥ C. ③⑥ D. ②④⑤⑥ |
|
| 7. 选择题 | 详细信息 |
|
A. 称量时,将固体NaOH直接放在天平左盘上 B. 将称量好的固体NaOH放入容量瓶中,加蒸馏水溶解 C. 定容时如果加水超过了刻度线,用胶头滴管直接吸出多余部分 D. 将烧杯中溶解固体NaOH所得溶液,冷却到室温后转移至容量瓶中 |
|
| 8. 选择题 | 详细信息 |
|
设NA表示阿伏加德罗常数的值,下列说法正确的是 ( ) A. 物质的量浓度为0.5mol/L的MgCl2溶液中,含Cl-个数为NA B. 0.1molNa2O2固体与足量的H2O充分反应,转移0.2NA个电子 C. 3g 3He含有的中子数为1NA D. 标况下,4.48L的水中含有H2O分子的数目为0.2NA |
|
| 9. 选择题 | 详细信息 |
|
下列对过氧化钠的叙述中,正确的是( ) A. 过氧化钠能与酸反应生成盐和水,所以过氧化钠是碱性氧化物 B. 过氧化钠能与水反应,所以过氧化钠可以作气体的干燥剂 C. 过氧化钠与二氧化碳反应产生氧气,故可用于呼吸面具中 D. 过氧化钠与二氧化碳反应时,过氧化钠只作氧化剂 |
|
| 10. 选择题 | 详细信息 |
|
宋代著名法医学家宋慈的《洗冤集录》中有关于银针验毒的记载,“银针验毒”的原理是4Ag+2H2S+O2===2X+2H2O,下列说法不正确的是( ) A. X的化学式为Ag2S B. 银针验毒时,空气中氧气得到电子 C. 反应中Ag和H2S均是还原剂 D. 每生成1 mol X,反应转移2 mol e- |
|
| 11. 选择题 | 详细信息 |
|
下列离子方程式中,正确的是 ( ) A. 稀硫酸滴在铁片上:2Fe+6H+===2Fe3++3H2↑ B. 碳酸氢钠溶液与稀盐酸混合:HCO3-+H+=H2O+CO2↑ C. 硫酸铜溶液与氢氧化钠溶液混合:CuSO4+2OH-===Cu(OH)2↓+ D. 硝酸银溶液与氯化钠溶液混合:AgNO3+Cl-===AgCl↓+ |
|
| 12. 选择题 | 详细信息 |
|
已知在相同条件下进行下列反应:①Cl2+2KBr=2KCl+Br2;②KClO3 +6HCl=3Cl2+KCl +3H2O;③2KBrO3 +Cl2=Br2 + 2KClO3。下列说法正确的是: A.上述三个反应都有单质生成,所以都是置换反应 B.反应①和反应③中均生成Br2,溴元素发生的变化相同 C.反应②中被氧化与被还原物质的物质的量之比为6:1 D.③中lmol还原剂反应则氧化剂得到电子的物质的量为10mol |
|
| 13. 选择题 | 详细信息 |
|
设NA为阿伏加德罗常数的值,下列说法正确的是( ) A. 标准状况下,22.4LCl2通入足量的NaOH溶液充分反应,有NA个电子转移 B. 100 mL 1 mol·L−1FeCl3溶液中所含Fe3+的数目为0.1NA C. lmolSO2与足量O2在一定条件下反应生成SO3,共转移2NA个电子 D. 84gNaHCO3固体含有CO32-离子的数目为NA |
|
| 14. 选择题 | 详细信息 |
|
下列各组离子可能大量共存的是( ) A. 在含大量Fe3+的溶液中:NH4+、Na+、Cl﹣、SCN﹣ B. 在含有Al3+、Cl﹣的溶液中:HCO3﹣、I﹣、NH4+、Mg2+ C. 在c(H+)=1×10﹣13 mol·L﹣1的溶液中:Na+、S2﹣、SO32﹣、NO3﹣ D. 在溶质为KNO3和NaHSO4的溶液中:Fe2+、Ca2+、Al3+、Cl﹣ |
|
| 15. 选择题 | 详细信息 | ||||||||||||
下列指定反应的化学用语表达正确的是( )
|
|||||||||||||
| 16. 选择题 | 详细信息 |
某氯化钾样品中含有少量碳酸钾、硫酸钾和不溶于水的杂质。为了提纯氯化钾,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按如图所示步骤进行操作。下列说法中正确的是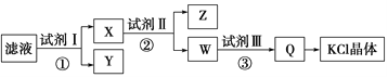 A. 起始滤液的pH=7 B. 试剂Ⅰ为Ba(NO3)2溶液 C. 步骤②中加入试剂Ⅱ的目的是除去Ba2+ D. 图示的步骤中必须要经过2次过滤操作 |
|
| 17. 选择题 | 详细信息 |
向Na2CO3、NaHCO3,混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示。则下列离子组在对应的溶液中一定能大量共存的是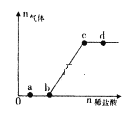 A. a点对应的溶液中:Na+、OH-、SO42-、NO3- B. b点对应的溶液中:Al3+、Fe3+、MnO4-、Cl- C. c点对应的溶液中:Na+、Ca2+、NO3-、Cl- D. d点对应的溶液中:F-、NO3-、Fe2+、Ag+ |
|
| 18. 填空题 | 详细信息 |
|
有一瓶澄清的溶液,其中可能含有H+,Mg2+,Na+,Ba2+,Fe3+,Cl﹣,CO32﹣,SO42﹣等离子,取该溶液进行以下实验 a.用PH试纸检验,表明溶液呈强酸性。 b.取部分溶液逐渐滴加入NaOH溶液,使溶液从酸性逐渐变成碱性,整个滴加过程中,溶液均无沉淀生成。 c.取部分上述碱性溶液加Na2CO3溶液,有白色沉淀生成。 (1)根据上述事实确定:该溶液中肯定存在的离子有____________;肯定不存在的离子有____________;可能存在的离子有____________。 (2)写出以下反应的离子方程式: ①氧化镁溶于盐酸____________。 ②碳酸氢钠溶液与氢氧化钠溶液混合____________。 ③氢氧化钡与稀硫酸混合____________。 |
|
| 19. 实验题 | 详细信息 |
实验室用如下装置制取氯气,并用氯气进行实验。回答下列问题: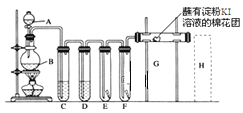 (1)A中盛有浓盐酸,B中盛有MnO2,写出反应的化学方程式_______。 (2)D中放入浓H2SO4,其目的是_____________________________。 (3)E中为红色干布条,F中为红色湿布条,可观察到的现象是___________,对比E和F中现象的差异可得出的结论及解释是____________________。 (4)G处的现象是____________________________________。 (5)画出H处尾气吸收装置图并注明试剂____________。 (6)家庭中常用消毒液(主要成分NaClO)与洁厕灵(主要成分盐酸)清洁卫生。某品牌消毒液包装上说明如图。 注意事项: 1、本品对棉织品有漂白脱色作用,对金属制品有腐蚀作用。 2、密封保存,请勿与洁厕灵同时使用。 3、保质期为一年。 “与洁厕灵同时使用”会产生有毒的氯气,写出反应的离子方程式________。 (7)现在有一种名为“净水丸”的产品也能对饮用水进行快速的杀菌消毒,药丸通常分内外两层。外层的优氯净Cl2Na(NCO)3先与水反应,生成次氯酸起杀菌消毒作用;几分钟后,内层的亚硫酸钠(Na2SO3)溶出,可将水中的余氯(次氯酸等)除去。亚硫酸钠将水中多余次氯酸除去的离子反应方程式为____________。 |
|
| 20. 填空题 | 详细信息 |
如图在衬白纸的玻璃片中央放置适量的KMnO4颗粒,在周围分别滴加一滴含有酚酞的澄清石灰水、FeCl2溶液,然后在KMnO4晶体上滴加适量的浓盐酸,迅速盖好表面皿。提示:实验室中所用的少量氯气可以用下述原理制取:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,此反应在常温下即能进行。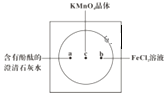 (1)浓盐酸在反应中表现出来的性质是______ (填写编号),氧化剂与还原剂物质的量之比为______ ,氧化产物为______ 。 ①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性 (2)产生0.1 mol Cl2,则转移电子的物质的量为 ______ mol。 (3)a处反应的化学方程式是___________________________,工业上用此原理制取漂白粉。 (4)b处离子方程式是________________________。 (5)高锰酸钾标准溶液经常用来滴定测量物质的含量。用高锰酸钾法间接测定石灰石中CaCO3的含量的方法为: 称取试样0.1250g,用稀盐酸溶解后加入(NH4)2C2O4得CaC2O4沉淀。沉淀经过滤洗涤后溶于稀硫酸中。滴定生成的H2C2O4 用去浓度为0.0 16mo/LKMnO4 溶液25.00mL。 ①写出CaC2O4沉淀溶解的离子方程式:___________________ ②配平并完成下列高锰酸钾滴定草酸反应的离子方程式: ____MnO4-+___H2C2O4+____=___Mn2++___CO2↑+____ ③石灰石中CaCO3的百分含量:_______ |
|
最近更新



