2019届高三第一学期学业质量监测理科综合化学考试(广东省珠海市)
| 1. 选择题 | 详细信息 |
|
化学与工业生产有着密切的联系,下列说法中正确的是( ) A. 与12C互为同素异形体的14C可用作文物鉴定 B. 因铝的化学性质活泼,故不能用铝槽车储运浓H2SO4 C. 海水淡化的方法有蒸馏法、电渗析法、明矾净水等方法 D. 石油裂解、煤的气化等过程中都包含化学变化 |
|
| 2. 选择题 | 详细信息 |
海藻中含有丰富的碘元素(以I-形式存在)。实验室中提取碘的流程如下图所示:  上述流程中步骤A~D对应的装置图正确的是( ) A. A B. B C. C D. D |
|
| 3. 选择题 | 详细信息 |
某有机化合物M的结构简式如下图所示,有关该化合物的叙述正确的是( ) A. 属于芳香烃 B. 分子式为:C11H14O2 C. 最多有11个碳原子共面 D. 能发生化学反应的类型只有2种 |
|
| 4. 选择题 | 详细信息 |
|
设NA为阿伏伽德罗常数的值,下列说法正确的是( ) A. 32克188O2,中含有的中子数为10NA B. 25℃时,1L pH=12的Ba(OH)2溶液中OH-数目为0.02NA C. 标况下,224L Cl2与足量H2O反应转移的电子数为0.1NA D. 4.6gNa与足量O2充分反应后的产物中含离子数目为0.3NA |
|
| 5. 选择题 | 详细信息 |
|
W、X、Y、Z为原子序数依次递增的前20号主族元素。W、Y均为非金属元素,而W、Z的最外层电子数之比为2:1,X是地壳中含量最高的金属元素,X、Y形成的二元化合物溶水后同时生成沉淀和臭鸡蛋气味的气体,下列说法正确的是( ) A. Z对应的金属氢化物只存在离子键 B. X、Z分别对应的金属氯化物的水溶液均呈酸性 C. H2YO3的酸性比H2WO3强,则证明非金属性:Y>W D. Y的两种气态氧化物分别通入BaCl2溶液中均产生白色沉淀 |
|
| 6. 选择题 | 详细信息 |
一种三室微生物燃料电池污水净化系统原理如下图所示,图中含酚废水中有机物可用C6H6O表示,左、中、右室间分别以离子交换膜分隔。下列说法不正确的是( ) A. 左池的pH值降低 B. 右边为阴离子交换膜 C. 右池电极的反应式:2NO3-+10e-+12H+= N2↑+ 6H2O D. 当消耗0.1molC6H6O,在标准状况下将产生0.28mol氮气 |
|
| 7. 选择题 | 详细信息 |
纯的叠氮酸(HN3)是一种弱酸,常温下向25mL 0.1 mol/L NaOH溶液中加入0.2 mol/L HN3溶液,滴加过程中的pH值的变化曲线(溶液混合时的体积变化忽略不计)如下图。下列说法正确的是( ) A. 该滴定过程中应用甲基橙作指示剂 B. 若B点pH=8,则c(HN3)=(10-6~10-8 )mol/L C. 点D对应溶液中存在关系:c(HN3)>c(Na+)>c(N3-) D. 沿曲线A→B→C的过程中,由水电离产生的c(OH-)逐渐减少 |
|
| 8. 实验题 | 详细信息 |
氨基甲酸铵(H2NCOONH4)是一种易水解、受热易分解的白色固体,某研究小组用下图所示的实验装置制备氨基甲酸铵,反应原理为:2NH3(g)+CO2(g)=H2NCOONH4(s) △H<0。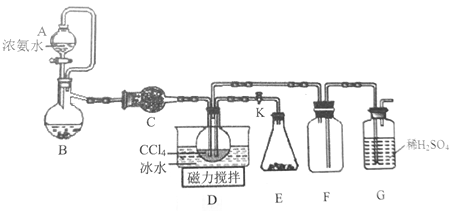 (1)仪器B的名称是________________。 (2)打开阀门K,装置E中由固体药品所产生的气体就立即进入装置D,则该固体药品的名称为________________。 (3)装置D为制备氨基甲酸铵的反应器(CCl4充当惰性介质),在合适催化剂下搅拌一段时间。 ①反应在冰水浴中进行的原因为_______________________________________。 ②当CCl4液体中产生较多晶体悬浮物时,即停止反应,__________(填操作名称)分离得到粗产品。 (4)仪器G的作用有:_______________________________________。 (5)该实验装置中有一处不足,改进方法是______________________________________。 (6)已知氨基甲酸铵可完全水解为碳酸氢铵,则该反应的化学方程式_________________。 (7)为测定某样品中氨基甲酸铵的质量分数,某研究小组用该样品进行实验,已知杂质不参与反应,请补充完整测定某样品中氨基甲酸铵质量分数的实验方案(限选试剂:蒸馏水、澄清石灰水、Ba(OH)2溶液):用天平称取一定质量的样品,加水溶解,____________________,测量的数据取平均值进行计算。 |
|
| 9. 综合题 | 详细信息 |
从某化工厂提供的硒酸泥(主要含S、Se、Fe2O3及SiO2)中提取粗硒的工艺流程如下图所示: 备注:氧化浸出液中Se的含量为43.45g/L 根据以上信息回答下列问题: (1)把煤油加热后再进行浸泡的目的是:__________________________。 (2)将含硫的滤液进行“冷却、结晶、过滤”操作可以除去煤油中的硫,由这一操作可推测硫的物理性质是:__________________________。 (3)“氧化浸硒”过程中: ①需要控制H2SO4的浓度至少为3mol/L,理由是:__________________________。 ②硒转化为H2SeO3并生成一种黄绿色的气体,此过程的化学方程式为_______________。 (4)要将1L氧化浸出液中的硒元素全部还原,需要至少加入Na2SO3_____mol; (5)滤渣A的主要成分有___________;滤液B的金属阳离子有___________; (6)处理硒酸泥的另一种方法是往硒酸泥中加入等体积的浓硫酸进行焙烧,本工艺流程与此方法相比主要的优点是(写两点):__________________________。 |
|
| 10. 综合题 | 详细信息 |
|
工业上制备丙烯的方法有多种,具体如下(本题丙烯用C3H6表示): (1)丙烷(C3H8)脱氢制备丙烯(C3H6) 由下图可得,C3H8(g)  (2)用惰性电极电解CO2的酸性溶液可得丙烯(C3H6),其原理如下图所示。则b的电极反应式为__________。  (3)以丁烯(C4H8)和乙烯(C2H4)为原料反应生成丙烯(C3H6)的方法被称为“烯歧化法”,反应为:C4H8(g)+C2H4(g) 一定温度下,在一体积恒为VL的密闭容器中充入一定量的C4H8和C2H4,发生烯烃歧化反应。 I.该反应达到平衡的标志是______________ a.反应速率满足:2v生成(C4H8)=v生成(C3H6) b.C4H8、C2H4、C3H6的物质的量之比为1:1:2 c.混合气体的平均相对分子质量不再改变 d.C4H8、C2H4、C3H6的浓度均不再变化 Ⅱ.已知t1min时达到平衡状态,测得此时容器中n(C4H8)=mmol,n(C2H4)=2mmol,n(C3H6)=nmol,且平衡时C3H6的体积分数为 ①该时间段内的反应速率v(C4H8)= _______mol/(L·min)。(用只含m、V、t1的式子表示)。 ②此反应的平衡常数K=______________。 ③t1min时再往容器内通入等物质的量的C4H8和C2H4,在新平衡中C3H6的体积分数_______ (4)“丁烯裂解法”是另一种生产丙烯的方法,但生产过程中伴有生成乙烯的副反应发生,具体反应如下:主反应:3C4H8 ①从产物的纯度考虑,丙烯和乙烯的质量比越高越好。则从下表现的趋势来看,下列反应条件最适宜的是__________(填字母序号)。 a.300℃0.1MPa b.700℃0.1MPa c.300℃0.5MPa d.700℃0.5MPa ②下图中,平衡体系中丙烯的百分含量随压强增大呈上升趋势,从平衡角度解释其可能的原因是_____。  |
|
| 11. 综合题 | 详细信息 | ||||||||
|
锰元素在多个领域中均有重要应用,回答下列问题。 (1)Mn在元素周期表中位于_____区;MnSO4中阳离子的价电子排布式为__________; (2)Mn3+在水溶液中容易歧化为MnO2和Mn2+下列说法合理的是_______ A.Mn3+的价电子构型为3d4,不属于较稳定的电子构型 B.根据Mn2+的电子构型可知,Mn4+中不含成对电子 C.Mn2+易被氧化,可能是因为Mn2+产内有大量自旋方向相同的电子 D.Mn2+与Fe3+具有相同的价电子构型,所以它们的化学性质相似 (3)在K2MnF6中,MnF62-的空间构型是正八面体,则中心原子的价层电子对数为_____。该化合物中含有的共价键在形成过程中原子轨道的重叠方式为__________ (4)二价锰的化合物的性质如下表所示:
|
|||||||||
| 12. 综合题 | 详细信息 |
工业上以乙酸为原料经一系列反应可得到香豆素-3-羧酸,合成路线如下图所示: (1)反应1的反应类型是________,A的官能团名称是________,B的名称是________。 (2)D→E的变化过程中, 另一有机产物的结构简式为________________。 (3)F的结构简式为________________。 (4)写出满足下列条件的C的两种同分异构体的结构简式________________________。 a.只含有羧基 b.核磁共振氢谱有3个吸收峰,且峰面积之比为3:2:1 (5)香豆素-3-羧酸在NaOH溶液中完全反应的化学方程式为_______________________。 (6)已知:R-CH(COOH)2 →R-CH-COOH,参照上述合成路线和信息,写出以苯甲醛和B为基本原料合成C6H5-CH=CH-COOH的路线。__________________________。 |
|
最近更新




