西藏山南第二高级中学2020-2021年高一上期期中考试化学免费试卷带答案和解析
| 1. 选择题 | 详细信息 | |||||||||||||||
许多装有化学物质的瓶子上贴有危险警告标志,下面是一些危险警告标志,其中标志贴错的是( )
A.A B.B C.C D.D |
||||||||||||||||
| 2. 选择题 | 详细信息 |
|
胶体能产生丁达尔效应,下列物质中能产生丁达尔效应的是 A.食醋 B.云雾 C.食盐水 D.白糖水 |
|
| 3. 选择题 | 详细信息 |
|
用下列方法来制备Fe(OH)3胶体,可行的是( ) A.把1mL饱和三氯化铁溶液逐滴加入到20mLNaOH溶液中 B.把1mL饱和三氯化铁溶液逐滴加入到20mL冷水中,边加边振荡 C.把1mL饱和三氯化铁溶液一次性加入到20mL沸水中,并加以搅拌 D.把1mL饱和三氯化铁溶液逐滴加入20mL到沸水中 |
|
| 4. 选择题 | 详细信息 |
|
下列电解质在水溶液中的电离方程式书写正确的是( ) A.HClO=H++ClO- B.KHCO3=K++ C.H2CO3 |
|
| 5. 选择题 | 详细信息 |
|
下列物质的水溶液能导电,但属于非电解质的是( ) A.CO2 B.CH3COOH C.CuSO4 D.NaOH |
|
| 6. 选择题 | 详细信息 |
|
在无色透明的溶液中,下列各组离子能大量共存的是( ) A.Cu2+、NO C. K+、Cl-、HCO |
|
| 7. 选择题 | 详细信息 |
|
下列各溶液中n(Na+)与100 mL 0.1 mol/L Na2SO4溶液中n(Na+)相同的是( ) A.100 mL 0.1 mol/L NaCl 溶液 B.50 mL 0.2 mol/L NaNO3溶液 C.100 mL 0.1 mol/L NaHSO4溶液 D.200mL 0.2mol/L HCl溶液与100 mL 0.2 mol/L NaHCO3溶液混合 |
|
| 8. 选择题 | 详细信息 |
|
下列实验操作中错误的是 A.萃取操作时,一般选择有机萃取剂,且萃取剂的密度与水的密度无关 B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 C.分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 D.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 |
|
| 9. 选择题 | 详细信息 |
|
用NA表示阿伏德罗常数的值,下列叙述正确的是 A.NA 个CO2分子占有的体积约为22.4L B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.02 NA C.标准状况下,22.4LH2O含有的分子数为 NA D.物质的量浓度为0.5mol·L-1的MgCl2溶液中,含有Cl-个数为NA |
|
| 10. 选择题 | 详细信息 | ||||||||||||
下列用于分离提纯物质的装置正确的是( )
|
|||||||||||||
| 11. 选择题 | 详细信息 |
符合下图中阴影部分的物质是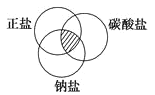 A.Na2CO3 B.NaHCO3 C.K2CO3 D.Na2SO4 |
|
| 12. 选择题 | 详细信息 |
|
下列叙述正确的是( ) A.lmo1 O2的质量为32g/mo1 B. C.H2SO4的相对分子质量为98g D.lmol任何物质的质量等于该物质的相对分子质量 |
|
| 13. 填空题 | 详细信息 |
填写物质的量与质量、微粒数、气体体积、物质的量浓度的关系。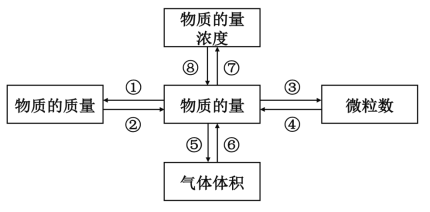 ①___________; ②___________; ③___________; ④___________; ⑤___________; ⑥___________; ⑦___________; ⑧___________。 |
|
| 14. 填空题 | 详细信息 |
实验室需要0.1mol/L NaOH溶液450mL和0.5mol/L硫酸溶液450mL.根据这两种溶液的配制情况回答下列问题: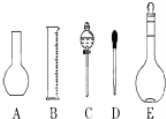 (1)如图所示的仪器中配制溶液肯定不需要的是__________(填序号),仪器C的名称是__________,本实验所需玻璃仪器E规格为__________mL. (2)下列操作中,容量瓶所不具备的功能有__________(填序号). A.配制一定体积准确浓度的标准溶液 B.长期贮存溶液 C.用来加热溶解固体溶质 D.量取一定体积的液体 (3)在配制NaOH溶液实验中,其他操作均正确.若定容时仰视刻度线,则所配制溶液浓度__________0.1mol/L(填“大于”“等于”或“小于”,下同).若NaOH溶液未冷却即转移至容量瓶定容,则所配制溶液浓度__________0.1mol/L. (4)根据计算得知,所需质量分数为98%、密度为1.84g/cm3的浓硫酸的体积为______mL(计算结果保留一位小数).如果实验室有10mL、25mL、50mL量筒,应选用__________mL规格的量筒最好. |
|
| 15. 填空题 | 详细信息 |
|
NaHCO3是生活中常见的物质,请回答下列问题: (1)写出NaHCO3在水溶液中的电离方程式:_____________。 (2)NaHCO3属于“酸”“碱”“盐”中的___________。 (3)制备Fe(OH)3胶体:用洁净的烧杯取一定量蒸馏水,用酒精灯加热至沸腾,向烧杯中加入几滴饱和FeCl3溶液继续加热至液体呈透明的红褐色。 ①写出制备Fe(OH)3胶体反应的离子方程式:_____________。 ②验证制得的分散系是胶体的方法为____________。 |
|
| 16. 计算题 | 详细信息 |
|
(1)配制500mL0.2mol/LNa2CO3 溶液需要的Na2CO3 质量是多少?_____________。 (2)取上述溶液20mL稀释成100mL后其物质的量浓度是多少?_____________。 |
|
最近更新