珠海市带答案与解析
| 1. 选择题 | 详细信息 |
|
近年来发现,在金星大气层中存在三氧化二碳。下列物质与它属于同类的是 A.H2、O3 B.H2SO4、H2CO3 C.SO2、NO D.Na2SO3、KClO3 |
|
| 2. 选择题 | 详细信息 |
|
古诗词是我们宝贵的精神财富。下列诗句中不涉及氧化还原反应的是( ) A.泉眼无声惜细流,树阴照水爱晴柔 B.春蚕到死丝方尽,蜡炬成灰泪始干 C.野火烧不尽,春风吹又生 D.爆竹声中一岁除,春风送暖入屠苏 |
|
| 3. 选择题 | 详细信息 |
|
区别溶液和胶体最简单的方法是 A. 丁达尔现象 B. 闻气味 C. 过滤 D. 根据分散质微粒直径 |
|
| 4. 选择题 | 详细信息 |
|
将下列各组物质,按单质、氧化物、酸、碱、盐分类顺序排列正确的是 A.银、二氧化硫、硫酸、纯碱、食盐 B.碘酒、冰、硫酸氢钠、烧碱、碳酸钙 C.氢气、干冰、硝酸、烧碱、硝酸钾 D.铜、氧化铜、醋酸、石灰水、碳酸氢钠 |
|
| 5. 选择题 | 详细信息 |
|
下列叙述正确的是 A.向氢氧化钠溶液中边滴加饱和FeCl3溶液边振荡制备Fe(OH)3胶体 B.分散系中分散质粒子直径由小到大的正确顺序是:溶液<胶体<浊液 C.Fe(OH)3胶体的电泳现象证明此胶体带正电荷 D.胶体区别于其他分散系的根本原因是胶体有丁达尔效应 |
|
| 6. 选择题 | 详细信息 |
|
下列有关胶体制备和性质,正确的是 A.胶体与其他分散系的本质区别是有丁达尔效应,而其他分散系没有 B.将饱和 C.胶体粒子的直径小于 D.将一束强光通过 |
|
| 7. 选择题 | 详细信息 |
|
下列物质属于电解质的是 A.食盐水 B.铜 C.二氧化硫 D.氢氧化钠 |
|
| 8. 选择题 | 详细信息 |
|
下列电离方程式中,正确的是 A.Na2SO4=2Na++ C.Al2(SO4)3=2Al3++3 |
|
| 9. 选择题 | 详细信息 |
|
下列离子方程式中正确的是( ) A.氢氧化钠溶液与碳酸氢钠溶液反应:OH-+HCO B.氢氧化铜与稀硫酸反应:H++OH-=H2O C.铝与硝酸汞溶液反应:Al+Hg2+=Al3++Hg D.金属铜与稀盐酸反应:Cu+2H+=Cu2++H2↑ |
|
| 10. 选择题 | 详细信息 |
|
下列反应的离子方程式书写正确的是( ) A.往碳酸镁中滴加稀盐酸:CO B.氢氧化钡溶液与稀H2SO4反应:Ba2++SO C.CuO与稀盐酸反应:CuO+2H+=Cu2++H2O D.铁粉与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
|
| 11. 选择题 | 详细信息 |
|
下列各组中的离子,能在溶液中大量共存的是 A.K+、H+、 C.Na+、H+、Cl-、 |
|
| 12. 选择题 | 详细信息 |
|
下列各组离子在指定溶液中能大量共存的是( ) A.无色溶液中: K+、 Na+、 B.强碱性溶液: C.强酸性溶液: Fe2+、 K+、ClO-、 D.在碳酸钠溶液中: K+、 |
|
| 13. 选择题 | 详细信息 |
某兴趣小组的同学向一定体积的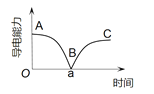 A.AB段溶液的导电能力不断减弱,说明生成的 B.B处溶液的导电能力约为0,说明溶液中几乎没有自由移动的离子 C.a时刻 D.BC段溶液的导电能力不断增大,主要是由于过量的 |
|
| 14. 选择题 | 详细信息 |
|
下列说法正确的( ) A.氧化还原反应的本质是元素化合价的升降 B.发生氧化反应的物质也可能同时发生还原反应 C.有单质参与的反应一定是氧化还原反应 D.氧化还原反应一定有氧元素参加 |
|
| 15. 选择题 | 详细信息 |
|
下列变化过程中,属于氧化反应的是 A.MnO2→Mn2+ B.Sn2+→Sn4+ C.Ag+→Ag D.CuO→CuCl2 |
|
| 16. 选择题 | 详细信息 |
|
下列反应属于氧化还原反应的是 A.CaCO3+2HCl=CaCl2+CO2↑ + H2O B.CaO+H2O=Ca(OH)2 C.2H2O2  2H2O+O2↑ D.CaCO3 2H2O+O2↑ D.CaCO3 |
|
| 17. 选择题 | 详细信息 |
|
氧化还原反应的实质是( ) A.氧元素的得与失 B.化合价的升降 C.电子的转移 D.分子中原子重新组合 |
|
| 18. 选择题 | 详细信息 |
|
以下表示的是碳及其化合物的转化关系,其中涉及的基本反应类型依次是( ) C A.化合、置换、分解、复分解 B.置换、复分解、化合、分解 C.置换、化合、分解、复分解 D.置换、化合、复分解、分解 |
|
| 19. 选择题 | 详细信息 |
|
已知5KCl+KClO3+3H2SO4=3Cl2↑+3K2SO4+3H2O,下列说法不正确的是( ) A.H2SO4既不是氧化剂又不是还原剂 B.1个KClO3参加反应时有5个电子转移 C.KClO3 是氧化剂 D.被氧化与被还原的氯元素的质量比为1:5 |
|
| 20. 实验题 | 详细信息 |
|
某课外活动小组进行Fe(OH)3胶体的制备实验并检验其相关性质。 (1)若将饱和FeCl3溶液分别滴入下列物质中,能形成胶体的是_______; A.冷水 B.沸水 C.NaOH浓溶液 D.NaCl浓溶液 (2)写出制备Fe(OH)3胶体的化学反应方程式_______; (3)取少量制得的胶体加入试管中,再加入少量H2SO4溶液,观察到的现象________; (4)Fe(OH)3胶体区别于FeCl3溶液最本质的特征是________; A.Fe(OH)3胶体粒子的直径在1~100nm之间 B.Fe(OH)3胶体具有丁达尔效应 C.Fe(OH)3胶体是均一的分散系 D.Fe(OH)3胶体的分散质粒子能透过滤纸 (5)将制得的胶体放入半透膜制成的袋内,如图所示,放置2min后,取少量半透膜外的液体于试管中,置于暗处,用一束强光从侧面照射,观察_____ (填“有”或“无”)丁达尔现象,再向试管中加入用稀硝酸酸化的硝酸银溶液,可观察到的现象为_______。  |
|
| 21. 填空题 | 详细信息 |
|
分类法是一种重要的学习方法。下列4组物质中均有一种物质的类别与其他三种不同,请分别填出其化学式。 甲:Ca、H2、O2、Cl2; 乙:CO、CaO、CO2、SO2; 丙:Ca(OH)2、K2CO3、KHCO3、K2SO4; 丁:NaOH、Ca(OH)2、KOH、CaCl2。 (1)甲________,乙________,丙________,丁________。 (2)根据图示,写出序号所示反应的化学方程式: Ca ①______________________________________。 ②______________________________________。 ③______________________________________。 |
|
| 22. 填空题 | 详细信息 |
|
I.化学反应按照不同的分类方法,可以分为化合反应,分解反应、置换反应、复分解反应,也可分为氧化还原反应和非氧化还原反应。有下列反应: ①CO2+C (1)其中属于化合反应的是_______(填序号,下同),属于置换反应的是_______。 (2)属于氧化还原反应的是________。 Ⅱ.(1)反应Fe2O3+2Al=Al2O3+2Fe在化学上被称为“铝热反应",人们可利用该反应来焊接铁轨,该反应所属基本反应类型是______。在该反应中______元素的化合价升高,该元素的原子______电子,被______;而______元素的化合价降低,该元素的原子______电子,被______。该反应中,Fe2O3发生了______反应,Al发生了______反应,______是氧化剂,______是氧化产物,______是还原剂,______是还原产物。 (2)写出CuO与CO在高温下反应的化学方程式,并用双线桥标出电子转移的方向和数目:________。 (3)写出Cu和AgNO3溶液反应的化学方程式,并用单线桥标出电子转移的方向和数目:________。 |
|
| 23. 填空题 | 详细信息 |
|
I.下列物质是生活生产中常见的物质:①NaHSO4晶体,②液态O2,③冰醋酸(固态醋酸),④汞,⑤Ba(OH)2固体,⑥Fe(OH)3胶体,⑦酒精(C2H5OH),⑧熔化Na2CO3,⑨盐酸,⑩金属钠,请回答下列问题(用序号): (1)以上物质属于电解质的是________ (2)以上物质中属于非电解质的是________ (3)以上物质中能导电的是________ II.按要求写方程式 (1)写出下列物质在水溶液中的电离方程式: ①NaHSO4_________ ②K2SO4 __________ ③NH4HCO3_______ (2)书写下列反应的离子方程式 ①氢氧化钠与硫酸反应__________。 ②实验室制取CO2气体_________。 ③少量CO2气体通入澄清石灰水________。 ④硫酸铜溶液与氢氧化钠反应______。 ⑤铁与稀硫酸____________。 ⑥氧化铜与稀盐酸__________。 |
|
最近更新



