2019届高三上半期第二次月考化学考试完整版(福建省华安县第一中学)
| 1. 选择题 | 详细信息 |
|
下列说法正确的是 A. 足量的Fe在Cl2中燃烧只生成FeCl3 B. 铁的化学性质比较活泼,它能和水蒸气反应生成H2和Fe(OH)3 C. 用酸性KMnO4溶液检验FeCl3溶液中是否含有FeCl2 D. 向某溶液中加NaOH溶液得白色沉淀,且颜色逐渐变为红褐色,说明该溶液中只含有Fe2+ |
|
| 2. 选择题 | 详细信息 |
|
下列说法中正确的是 A. 第ⅦA族单质从上往下熔沸点逐渐升高,第ⅠA族单质从上往下熔沸点逐渐降低 B. Na2SiO3溶液可用作矿物胶、木材防火剂,还可用作制备硅胶的原料 C. 品红溶液和滴有酚酞的NaOH溶液均能与SO2气体作用而褪色,且其实质相同 D. 镁和铝性质稳定且都有很强的抗腐蚀能力,所以镁铝合金可用于飞机、轮船制造 |
|
| 3. 选择题 | 详细信息 |
|
下列反应的离子方程式正确的是 A. NaHS溶液中滴加少量的硫酸铜溶液:2HS-+Cu2+═CuS ↓+H2S↑ B. 将NO2气体通入H2O中:3NO2+H2O═2H++NO3-+O2↑ C. ICl和Cl2的化学性质相似,将ICl通入KOH溶液中:ICl+2OH-═I-+ClO-+H2O D. 1.5 mol·L-1 100 mL的FeBr2溶液中通入3.36 L(标准状况)Cl2:2Br-+Cl2═Br2+2Cl- |
|
| 4. 选择题 | 详细信息 |
|
W、Q、X、Y、Z是五种短周期主族元素,其中X原子K、L层电子数之比为1∶2,Y元素最外层电子数是次外层的3倍,Z是短周期主族元素中原子半径最大的元素,W是地壳中含量最高的金属元素, Q元素最高化合价与最低化合价之和为6。下列判断正确的是 A. W、Q、X、Y、Z的原子序数依次递增 B. Y的简单氢化物比X的稳定性高 C. 常温下,W元素的单质与浓硝酸反应生成NO2 D. Z、W的单质分别与Q的单质化合后的产物中所含化学键类型相同 |
|
| 5. 选择题 | 详细信息 |
根据下列装置完成系列实验,下列说法正确的是( )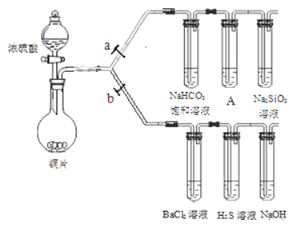 A. 铜和浓硝酸的反应与铜和浓硫酸的反应一样需要加热条件下才能进行 B. BaCl2溶液中会出现白色沉淀BaSO3 C. H2S溶液中会出现黄色沉淀,体现了SO2的还原性 D. 为验证碳、硅非金属性的相对强弱,A试管中的试剂可以是KMnO4溶液 |
|
| 6. 选择题 | 详细信息 |
|
下列化学用语表述正确的是( ) A. 核内质子数为117、中子数为174的核素Ts可表示为: B. 氯离子的结构示意图: 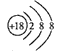 C. COCl2的结构式为: 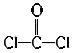 D. CaO2的电子式为: |
|
| 7. 选择题 | 详细信息 |
|
NA表示阿伏加德罗常数的值,下列说法正确的是( ) A. 标准状况下,11.2L三氧化硫中含有分子的数目为0.5NA B. 用含有0.1mo1FeCl3的饱和溶液配制的氢氧化铁胶体中,胶体粒子数等于0.1NA C. 1 mol过氧化钠与足量水反应,转移的电子数为NA D. 1.8g D2O中所含中子数为9NA |
|
| 8. 选择题 | 详细信息 |
|
丰富多彩的颜色变化增添了化学实验的魅力,下列反应颜色变化正确的是( ) ①新制氯水久置后→浅黄绿色消失 ②Cl2通入石蕊试液中→先变红后褪色 ③SO2通入溴水中→橙色褪去 ④浓硫酸滴入蔗糖晶体中→先变黄后变黑色 ⑤氨气通入酚酞溶液中→变红色 A. ①②④⑤ B. ②③④⑤ C. ①②③④ D. 全部 |
|
| 9. 选择题 | 详细信息 | ||||||||||||||||||||
下表所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是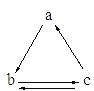
|
|||||||||||||||||||||
| 10. 选择题 | 详细信息 |
|
汽车剧烈碰撞时,安全气囊中发生反应:10NaN3+2KNO3=K2O+xNa2O+16N2↑,下列说法错误的是 A.x=5 B.每生成16 mol N2转移10 mol电子 C.N2既是氧化产物又是还原产物 D.反应中氧化产物与还原产物的质量之比为15:1 |
|
| 11. 选择题 | 详细信息 |
|
下列反应中,反应后固体物质质量不变的是 A. 在试管中加热小苏打粉末 B. 铝丝插入Cu(NO3)2溶液中 C. 在O2中灼烧Cu2S使之转化为CuO D. 水蒸气通过高温炽热的铁粉 |
|
| 12. 选择题 | 详细信息 |
|
常温下,下列各组离子一定能在指定溶液中大量共存的是 A. 能溶解Al2O3的溶液中:Na+、Fe2+、ClO-、SO42- B. 使甲基橙变红色的溶液中:K+、NH4+、HCO3-、Cl- C. 含有Na2SO3的溶液中:K+、H+、Cl-、NO3- D. 由水电离产生的c(OH-)=l×10-10mol·L-1的溶液中:Ba2+、K+、NO3-、Br- |
|
| 13. 选择题 | 详细信息 |
|
下列说法正确的是 ①合金的硬度可以大于它的纯金属成分,合金的熔点可以低于它的成分金属 ②碘酒、豆浆、牛奶、淀粉溶液都是胶体 ③FeO不稳定,在空气里受热就迅速被氧化成Fe2O3 ④新型陶瓷、玛瑙、玻璃都不是硅酸盐产品 ⑤漂粉精等可用于游泳池的消毒,而有些高级的游泳池则用臭氧等进行消毒 ⑥水玻璃、纯碱、氧化钙都是电解质 ⑦Ca(HCO3)2、Fe(OH)3、FeCl2都可以用化合反应制得 ⑧浓硝酸和浓盐酸按体积比1∶3混合叫做王水,能使一些不溶于硝酸的金属溶解 A. ①⑤⑦⑧ B. ①③⑦⑧ C. ②⑤⑦⑧ D. ③⑥⑦⑧ |
|
| 14. 选择题 | 详细信息 |
|
X、Y、Z、W、M五种元素的原子序数依次增大。已知X、Y、Z、W是短周期元素中的四种非金属元素,X元素的原子形成的离子就是一个质子;Y原子的最外层电子数是内层电子数的2倍;Z、W在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体;M元素的原子是短周期中原子半径最大的。下列说法正确的是 A. X、Z、W三元素形成的化合物都是共价化合物 B. 简单离子的半径从大到小的顺序是:M>Y>Z>W C. 氢化物的稳定性强弱顺序为:Y>Z>W D. M2W2既含有离子键,也含有非极性键 |
|
| 15. 选择题 | 详细信息 |
下列图象能正确表示相关反应中产物物质的量的变化的是(横、纵坐标单位:mol)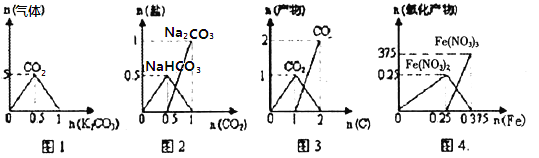 A. 图l:n(HCl)=lmol,K2CO3逐步加入到HCl溶液中,在敞口容器中生成的气体 B. 图2:n(NaOH)="1" mol,CO2逐步通人到NaOH溶液中反应生成的盐 C. 图3:n(O2)=1mol,高温下C和O2在密闭容器中的反应产物 D. 图4:n(HNO3,)=lmol,Fe和稀HNO3反应生成的氧化产物(还原产物为NO) |
|
| 16. 综合题 | 详细信息 | ||||
某强酸性无色溶液中可能含下表离子中的若干种离子。
|
|||||
| 17. 综合题 | 详细信息 |
铬是人体必需元素,如含量不足会影响糖类和脂类的代谢,过高则会引起急性中毒。工业上往往采取下列循环工艺防止铬的污染: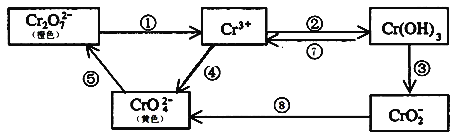 完成下列填空: (1)①步中含Cr2O (2)反应⑤是可逆反应,在Na2CrO4溶液中加入稀硫酸,溶液由黄色逐渐变成橙色,写出该反应的离子方程式:___________________________________; (3)向上述反应后的溶液中加入碱溶液,让废水的pH升至8~10,控制适当的温度,使产物中的金属阳离子全部转变为沉淀。回收所得的Cr(OH)3,经处理后又可转变成K2Cr2O7。纯净的K2Cr2O7常用于准确测定Na2S2O3溶液的物质的量浓度,方法如下: ①Cr2O72-+6I-+14H+ =3I2+2Cr3++7H2O ②2S2O32-+ I2 =S4O62-+2I-,准确称取纯净的K2Cr2O7 0.294g配成溶液,加足量KI,用Na2S2O3溶液滴定,消耗Na2S2O3溶液25.00mL。 ①回收所得的Cr(OH)3在处理之前需要先进行洗涤,洗涤沉淀的方法为________________________; ②滴定时加入的指示剂通常为_________,滴定至终点的现象是_______________________________; ③Na2S2O3溶液的物质的量浓度为__________。 |
|
| 18. 综合题 | 详细信息 |
实验室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4的主要流程如下: (1)制备MgAl2O4过程中,高温焙烧时发生反应的化学方程式为_____________。 (2)判断流程中沉淀是否洗净所用的试剂是__________________。 (3)在25 ℃下,向浓度均为0.01 mol·L-1的MgCl2和AlCl3混合溶液中逐滴加入氨水,先生成______沉淀(填化学式),生成该沉淀的离子方程式:_____________。{已知25 ℃时Ksp[Mg(OH)2]=1.8×10-11,Ksp[Al(OH)3]=3×10-34}。 (4)无水AlCl3(183 ℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。 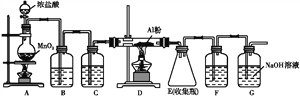 装置B中盛放饱和NaCl溶液,该装置的主要作用是______;F中试剂的作用是__________________________________________。 (5)将Mg、Cu组成的3.92 g混合物投入过量稀硝酸中,充分反应后,固体完全溶解时收集到还原产物NO气体1.792 L(标准状况),向反应后的溶液中加入4 mol·L-1的NaOH溶液80 mL时金属离子恰好完全沉淀。则形成沉淀的质量为____g。 |
|
| 19. 综合题 | 详细信息 |
|
联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料.回答下列问题: (1)联氨分子的电子式为___________, 其中氮的化合价为___________. (2)实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为____________. (3)①2O2(g)+N2(g)═N2O4(l) △H1 ②N2(g)+2H2(g)═N2H4(l) △H2 ③O2(g)+2H2(g)═2H2O(g) △H3 ④2N2H4(l)+N2O4(l)═3N2(g)+4H2O(g) △H4=﹣1048.9kJ•mol﹣1 上述反应热效应之间的关系式为△H4=______________, 联氨和N2O4可作为火箭推进剂的主要原因为______________________. (4)联氨为二元弱碱,在水中的电离方式与氨相似.联氨第一步电离反应的平衡常数值为_____ (已知:N2H4+H+⇌N2H5+的K=8.7×107;Kw=1.0×10﹣14).联氨与硫酸形成的酸式盐的化学式为_______________. (5)联氨是一种常用的还原剂.向装有少量AgBr的试管中加入联氨溶液,观察到的现象是_______________. 联氨可用于处理高压锅炉水中的氧,防止锅炉被腐蚀.理论上1kg的联氨可除去水中溶解的O2__________kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是________________________. |
|
最近更新