莆田市高一化学2018年上学期期中考试网上考试练习
| 1. 选择题 | 详细信息 |
如果你家里的食盐不小心混入了大量的泥沙,利用你所学的知识,最简便的分离方法是( ) A. A B. B C. C D. D |
|
| 2. 选择题 | 详细信息 |
|
在自来水的生产中,常通入适量氯气进行杀菌消毒,氯气与水反应的产物之一是盐酸。市场上有些不法商贩为牟取暴利,利用自来水冒充纯净水桶装出售。为辨别真伪,可用下列哪一种试剂来鉴别 A. 酚酞试液 B. 氯化钡溶液 C. 氢氧化钠溶液 D. 硝酸银溶液 |
|
| 3. 选择题 | 详细信息 |
|
下列关于Na和Na+的叙述中,错误的是 A. 它们相差一个电子层 B. 它们的化学性质相似 C. 钠原子,钠离子均为同一元素 D. 灼烧时,它们的焰色反应都呈黄色 |
|
| 4. 选择题 | 详细信息 |
|
核内中子数为N的R2+,其质量数为A,则该离子的核外电子数为( ) A.N-2 B.N+2 C.A-N-2 D.A-N+2 |
|
| 5. 选择题 | 详细信息 |
|
下列反应既是氧化还原反应,又是化合反应的是( ) A. Na2CO3+CO2+H2O=2NaHCO3 B. SO2+H2O2=H2SO4 C. CaO+H2O=Ca(OH)2 D. Cl2+2NaOH=NaClO+NaCl+H2O |
|
| 6. 选择题 | 详细信息 |
|
下列物质的分离方法中,主要是利用密度不同达到分离目的的是 A. 把石油蒸馏分离成汽油、煤油和柴油等 B. 煎中药时用水在煮沸条件下提取中药的有效成分 C. 把大豆磨碎后,用水溶解其中可溶性成分,经过滤后,分成豆浆和豆渣 D. 做饭洗米时淘去米中的沙 |
|
| 7. 选择题 | 详细信息 |
|
判断下列物质中属于电解质的是( ) A.硝酸钾溶液 B.蔗糖 C.金属铜 D.氢氧化钡 |
|
| 8. 选择题 | 详细信息 |
|
在2H2S+SO2=2H2O+3S中,氧化剂与还原剂的分子个数比为( ) A. 2∶1 B. 1∶2 C. 1∶1 D. 16∶17 |
|
| 9. 选择题 | 详细信息 |
|
久置的氯水和新制的氯水相比较,下列结论正确的是 A. 颜色相同 B. 都能使有色布条褪色 C. pH相同 D. 加AgNO3溶液都能生成白色沉淀 |
|
| 10. 选择题 | 详细信息 |
|
下列溶液中c(Cl-)最大的是 A. 400 mL0.5 mol/L BaCl2溶液 B. 200 mL 0.5 mol/L MgCl2溶液 C. 300 mL1 mol/L NaCl溶液 D. 100 mL 0.5 mol/L AlCl3溶液 |
|
| 11. 选择题 | 详细信息 |
|
下列有关胶体的叙述中不正确的是 A. 实验室可用丁达尔效应鉴别胶体与溶液 B. “雨后彩虹”既是一种自然现象又是光学现象,同时也与胶体有关 C. 1 mol Fe3+完全反应生成氢氧化铁胶体粒子的数目为NA D. 分散质粒子大小介于1 nm~100 nm之间的分散系称为胶体 |
|
| 12. 选择题 | 详细信息 |
|
对下列未知盐的稀溶液所含离子的检验中,作出的判断一定正确的是 A. 先加入氯化钡溶液时不产生沉淀,继续加入硝酸银溶液时,有不溶于稀硝酸的白色沉淀生成,可判定含有Cl— B. 先加稀盐酸酸化时没有现象,再加入氯化钡溶液有白色沉淀生成,可判定含有SO42- C. 加入NaOH溶液,有白色沉淀产生,可判定含有Mg2+ D. 加入盐酸后有无色无味气体逸出,此气体能使澄清石灰水变浑浊,判定一定含有CO32- |
|
| 13. 选择题 | 详细信息 |
|
现有①MgSO4 ②Ba(NO3)2 ③NaOH ④CuCl2四种溶液,不加其他试剂就可鉴别出来,鉴别的先后顺序是( ) A. ④③①② B. ③④①② C. ②①③④ D. ③④②① |
|
| 14. 选择题 | 详细信息 |
|
将2.3g钠放入97.7g水中,下列说法正确的是 A. 电子转移的数目为2NA B. 所得溶液的质量分数是等于4% C. 产生气体的体积为1.12L D. 产生的气体含有0.1mol的电子 |
|
| 15. 选择题 | 详细信息 |
|
下列说法中错误的是 A. 从1L1mol·L-1的NaCl溶液中取出10mL,其浓度仍是1mol·L-1 B. 制备0.5L 10mol·L-1的盐酸,需要氯化氢气体112L(标准状况) C. 0.5L 2mol·L-1BaCl2溶液中,Ba2+和Cl-总数为3×6.02×1023 D. 10mL质量分数为98%的H2SO4,用水稀释至100mL,H2SO4的质量分数为9.8% |
|
| 16. 选择题 | 详细信息 |
|
海带中含有丰富的碘,有人设计如下步骤:①将海带灼烧成灰,在灰中加水搅拌;②加四氯化碳充分振荡静置;③通入氯气;④过滤;⑤用分液法分离液体混合物。合理操作的先后顺序是 A. ①②③④⑤ B. ①④②③⑤ C. ①②④③⑤ D. ①④③②⑤ |
|
| 17. 选择题 | 详细信息 |
|
下列关于钠的说法中错误的是 A. 金属钠有强的还原性 B. 钠可以从硫酸铜溶液中还原出铜单质 C. 钠在氯气中燃烧产生大量的白烟 D. 钠元素在自然界中都是以化合态存在 |
|
| 18. 选择题 | 详细信息 |
|
通过溶解、过滤、蒸发等操作,可将下列各组固体混合物分离的是( ) A. 硝酸钠和氢氧化钠 B. 二氧化锰和氧化铜 C. 氯化钾和二氧化锰 D. 碳酸钾和氯化钙 |
|
| 19. 选择题 | 详细信息 |
|
已知:①2K2CrO4+H2SO4 ②K2Cr2O7+6FeSO4+7H2SO4 ③Fe2(SO4)3+2HI 下列结论正确的是 A. ①②③均是氧化还原反应 B. 氧化性强弱顺序是K2Cr2O7>Fe2(SO4)3>I2 C. 反应②中氧化剂与还原剂的物质的量之比为6∶1 D. 反应③中0.1 mol还原剂共失去电子数为6.02×1023 |
|
| 20. 计算题 | 详细信息 |
|
(1) 3.01×1023个OH−的物质的量为________mol,含有质子的物质的量为_____mol,含有电子的物质的量为________mol,这些OH−和________g Na+含有的电子数相同。 (2)标准状况下,1.92g某气体的体积为672mL,则该气体的摩尔质量为______; (3)等质量的SO2和SO3的物质的量之比_______;氧原子个数比为_________; (4)11.1gCaCl2固体溶于水配成500mL溶液,其浓度为_____ mol·L-1,从中取出100 mL溶液,其中Cl-的物质的量为_____mol。 |
|
| 21. 填空题 | 详细信息 |
|
已知铜和浓硫酸可以在加热条件下发生如下反应(反应方程式已配平): 试完成下面的问题: (1)A物质可以导致酸雨的形成。则A应该属于______(用字母代号填写) a.酸 b. 碱 c.盐 d.酸性氧化物 e.碱性氧化物 (2)该反应中被氧化的元素是_________________,参加反应的氧化剂与还原剂的物质的量之比为______。 (3)写出该反应的化学方程式并用双线桥标出电子转移的方向和数目:____________。 (4)一定量的铜片与100mL 18 mol/L的浓 |
|
| 22. 实验题 | 详细信息 |
|
现欲用98%的浓硫酸(密度为1.84g·cm-3)配制浓度为1mol·L-1的稀硫酸480mL。 (1)从下列用品中 选出实验所需要的仪器________________(填写序号) A.1000mL烧杯 B.100mL烧杯 C.10mL量筒 D.50mL量筒 E.500mL容量瓶 F.1000mL容量瓶 G.广口瓶 H.托盘天平 (2)除选用上述仪器外,还缺少的必要仪器或用品是_______________________ (3)需取用浓硫酸的体积为________mL (结果保留一位小数) (4)配制时,一般可分为以下几个步骤,请在下列横线填写所缺步骤的名称: 计算、称量、溶解、冷却、转移、洗涤、转移、_______、摇匀。 (5)下列情况中,会使所配溶液的浓度偏低的是________ A.将量筒中的浓硫酸转入烧杯后,用水洗涤量筒,将洗液也转入在烧杯中 B.稀释浓硫酸后立即转入容量瓶 C.定容时加水不慎超过刻度线 D.定容时仰视刻度线 |
|
| 23. 实验题 | 详细信息 |
某校化学兴趣小组为研究Cl2的性质,设计如图所示装置进行实验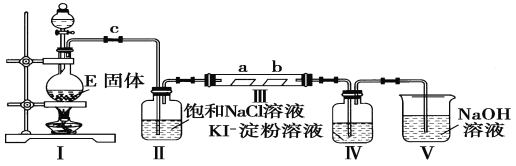 (1)实验室以二氧化锰和浓盐酸制备氯气的化学方程式为_______________。 (2)装置Ⅱ的作用是____________________________________。 (3)实验过程中,装置Ⅳ中的实验现象为_________________________;发生反应的化学方程式为_______________________________。 (4)实验结束后,该组同学在装置Ⅲ中(a是干燥的品红试纸,b是潮湿的品红试纸)观察到b的红色褪去,但是并未观察到“a无明显变化”这一预期现象。为了达到这一实验目的,你认为还需在上图装置_______与_____________之间添加下图中的_____________装置(填序号),该装置的作用是____________。  (5)装置V的目的是防止尾气污染空气,写出装置V中发生反应的化学方程式:_________________。 (6)将8.7 g MnO2与含HCl 14.6 g的浓盐酸共热制Cl2,甲同学认为可制得Cl2 7.1 g,乙同学认为制得Cl2的质量小于7.1 g,你认为__________(填“甲”或“乙”)同学正确,原因是 ___________________。 |
|
| 24. 实验题 | 详细信息 |
实验室里需要纯净的NaCl固体,但现在只有混有Na2SO4、NH4HCO3的NaCl固体混合物。某学生设计了如图所示方案提取纯净的NaCl固体。(已知:NH4HCO3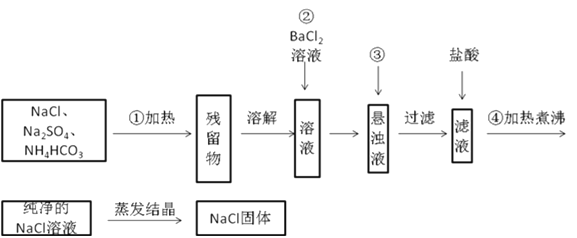 如果此方案正确,回答下列问题: (1)操作①可选择的主要仪器是(________)(多选题) A.酒精灯 B. 蒸馏烧瓶 C. 坩埚 (2)操作②不用硝酸钡溶液,其理由是______________________________________。 (3)进行操作②后,如何判断SO42− 已除尽,方法是________________________。 (4)操作③加的是(________) A.Na2CO3溶液 B.K2CO3溶液 C. NaNO3溶液 (5)操作④的目的是(________)(多选题) A.除去过量的BaCl2溶液 B.除去溶解在溶液中的CO2 C. 除去溶解在溶液中的HCl |
|
最近更新



