2020届高三化学一轮复习 基本概念物质的量
| 1. 选择题 | 详细信息 |
|
化学在人类社会发展中发挥着重要作用,下列事实不涉及化学反应的是( ) A. 利用废弃的秸秆生产生物质燃料乙醇 B. 利用石油生产塑料、化纤等高分子材料 C. 利用基本的化学原料生产化学合成药物 D. 利用反渗透膜从海水中分离出淡水 |
|
| 2. 选择题 | 详细信息 | ||||||||
下列我国科研成果所涉及材料中,主要成分为同主族元素形成的无机非金属材料的是
|
|||||||||
| 3. 选择题 | 详细信息 |
|
反应NH4Cl+NaNO2 A. 中子数为18的氯原子: B. N2的结构式:N=N C. Na+的结构示意图:  D. H2O的电子式: |
|
| 4. 选择题 | 详细信息 | ||||||||||||
下列示意图与化学用语表述内容不相符的是(水合离子用相应离子符号表示)
|
|||||||||||||
| 5. 选择题 | 详细信息 |
|
反应NH4Cl+NaNO2 A. 中子数为18的氯原子: B. N2的结构式:N=N C. Na+的结构示意图:  D. H2O的电子式: |
|
| 6. 选择题 | 详细信息 |
|
以下是中华民族为人类文明进步做出巨大贡献的几个事例,运用化学知识对其进行的分析不合理的是 A. 四千余年前用谷物酿造出酒和醋,酿造过程中只发生水解反应 B. 商代后期铸造出工艺精湛的后(司)母戊鼎,该鼎属于铜合金制品 C. 汉代烧制出“明如镜、声如磬”的瓷器,其主要原料为黏士 D. 屠呦呦用乙醚从青蒿中提取出对治疗疟疾有特效的青蒿素,该过程包括萃取操作 |
|
| 7. 选择题 | 详细信息 |
|
实验室需配制480 mL 1 mol·L-1 NaOH溶液,下列叙述正确的是( ) A. 转移液体时,玻璃棒应紧靠容量瓶口 B. 用托盘天平称量19.2 g NaOH固体 C. 容量瓶上标有温度、浓度、容积和压强 D. 定容时若俯视刻度线观察液面,会使所配制的NaOH溶液的浓度偏高 |
|
| 8. 选择题 | 详细信息 |
|
标准状况下VL氨气溶解在1L水中(水的密度近似为1g/mL),所得溶液的密度为ρg/mL,质量分数为ω,物质浓度为c mol/L,则下列关系中不正确的是 A. B. C. D. |
|
| 9. 选择题 | 详细信息 |
|
M(NO3)2热分解的化学方程式为:2M(NO3)2 A.64 g·mol-1 B.24 g·mol-1 C.65 g·mol-1 D.40 g·mol-1 |
|
| 10. 选择题 | 详细信息 |
|
下图是某学校实验室从化学试剂商店买同的硫酸试剂标签上的部分内容。据此下列说法正确的是 硫酸化学纯(CP) (500mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84g / cm3 质量分数:98% A.该硫酸的物质的量浓度为1.84mol/L B.1mol Zn与足量的该硫酸反应产生2gH2 C.配制200mL 4.6mol/L的稀硫酸需取该硫酸50mL D.该硫酸与等体积的水混合所得溶液的物质的量浓度等于9.2mol/L |
|
| 11. 选择题 | 详细信息 |
|
在三个密闭容器中分别充入Ne、H2、O2三种气体,在以下各种情况下排序正确的是( ) A.当它们的体积、温度和压强均相同时,三种气体的密度ρ(H2)>ρ(Ne)>ρ(O2) B.当它们的温度和密度都相同时,三种气体的压强p(H2)>p(Ne)>p(O2) C.当它们的质量、温度和压强均相同时,三种气体的体积V(O2)>V(Ne)>V(H2) D.当它们的压强、体积和温度均相同时,三种气体的质量m(H2)>m(Ne)>m(O2) |
|
| 12. 选择题 | 详细信息 |
|
在某H2SO4 和Fe2(SO4)3 混合液中,测得c(H+)为0.2mol·L-1,c(SO42-)为0.4 mol·L-1,则混合液中c(Fe3+)为 A. 0.1 mol·L-1 B. 0.2 mol·L-1 C. 0.3 mol·L-1 D. 0.4 mol·L-1 |
|
| 13. 选择题 | 详细信息 |
|
用20 mL 18.4 mol/L浓H2SO4和铜共热一段时间后,使反应混合物冷却,滤去多余的铜,将滤液加水定容到100 mL,测得SO42-离子物质的量浓度为3. 18 mol/L。试求溶液中CuSO4的物质的量浓度( ) A. 0.50 mol/L B. 0.75 mol/L C. 1.00 mol/L D. 3.18 mol/L |
|
| 14. 选择题 | 详细信息 |
|
已知NA是阿伏加德罗常数的值,下列说法错误的是 A. 3g 3He含有的中子数为1NA B. 1 L 0.1 mol·L−1磷酸钠溶液含有的 C. 1 mol K2Cr2O7被还原为Cr3+转移的电子数为6NA D. 48 g正丁烷和10 g异丁烷的混合物中共价键数目为13NA |
|
| 15. 选择题 | 详细信息 |
|
同温同压下,甲容器中充满35Cl2,乙容器中充满37Cl2,下列叙述不正确的是 A. 若两种气体体积相等,甲、乙两容器中气体的密度之比为35∶37 B. 若两种气体体积相等,甲、乙两容器中气体分子数之比为35∶37 C. 若两种气体质量相等,甲、乙两容器中气体所含质子数之比为37∶35 D. 若两种气体体积相等,甲、乙两容器中气体所含中子数之比为9∶10 |
|
| 16. 选择题 | 详细信息 |
|
设NA为阿伏加德罗常数的值,下列说法正确的是 A. 100g46%甲酸(HCOOH)水溶液所含的氧原子数为5NA B. 标准状况下,18 g冰水中共价键的数目为NA C. 56g铁与71gCl2 充分反应,转移电子数目为3NA D. 7.8g Na2O2 与足量的水(H218O)反应生成的氧气所含的中子数为0.5NA |
|
| 17. 选择题 | 详细信息 |
|
NA为阿伏加德罗常数的值。下列说法正确的是 ( ) A. 0.1molCl2与0.2molCH4光照充分反应生成HCl分子数为0.1NA B. 1LpH=12的氨水中加入足量盐酸,生成NH4+数为0.01NA C. 100g 34%的H2O2中加入MnO2充分反应转移电子数为2NA D. 0.1mol乙醇与0.1mol乙酸在浓硫酸作用下充分反应生成乙酸乙酯分子数为0.1 NA |
|
| 18. 选择题 | 详细信息 |
|
下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐。 下列说法中不正确的是( ) A. 当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4 B. 当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO3 C. B和Cl2的反应是氧化还原反应 D. 当X是强酸时,C在常温下是气态单质 |
|
| 19. 综合题 | 详细信息 | ||||||||||
|
物质的分类是学习化学的一种重要方法,科学合理的分类对于系统掌握知识、提高学习效率、解决问题都有着重要的意义。 请回答下列问题: (1)纯净物根据其组成和性质有如图分类形式,这种分类方法层次分明、简洁直观。  ①图中所示所属的分类方法为___________。 ②现有碳、一氧化碳、二氧化碳、碳酸氢钠四种物质,采用下列分类标准,无法将其中两种物质归为一类的是___________________。 A.具有还原性 B.属于氧化物 C.碳元素化合价相同 D.属于电解质 ③实验室常根据物质分类的原则存放药品,某学校实验室其中的四个药品柜已经存放了如下部分药品,实验室新购进一些晶体碘,应该将它存放在________________。
|
|||||||||||
| 20. 实验题 | 详细信息 |
|
实验室用密度为1.18g/ml,质量分数为36.5%浓盐酸配制250ml0.1mol/L的盐酸溶液,填空并请回答下列问题: (1)配制250ml0.1mol/L的盐酸溶液.应量取盐酸体积_________ml,应选用容量瓶的规格__________________ml。 (2)配制时,其正确的操作顺序是________。 A.用30ml水洗涤烧杯 2﹣3次,洗涤液均注入容量瓶,振荡 B.用量筒量准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30ml),用玻璃棒慢慢搅动,使其混合均匀 C.将已冷却的盐酸沿玻璃棒注入250ml的容量瓶中 D.将容量瓶盖紧、振荡、摇匀 E.改用胶头滴管加水,使溶液凹面恰好与刻度相切 F.继续往容量瓶内小心加水,直到液面接近刻度1﹣2cm处 a.BCAFED b.BCFED c.BCAED (3)操作B中,使用量筒量取液体时视线俯视会造成配制液体浓度__________(偏高、偏低或无影响)。操作E中加水超过刻度线该如何处理?____________ (4)若出现如下情况,对所配溶液浓度将有何影响(偏高、偏低或无影响)? a.没有进行A操作____________; b.加蒸馏水时不慎超过了刻度___________; c.定容时俯视_______________。 |
|
| 21. 实验题 | 详细信息 |
|
烟道气中的NOx是主要的大气污染物之一,为了监测其含量,选用如下采样和检测方法。回答下列问题: I.采样 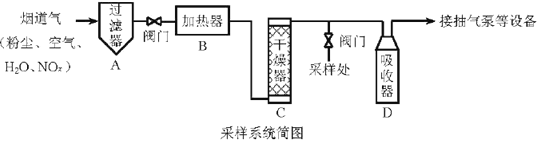 采样步骤: ①检验系统气密性;②加热器将烟道气加热至140。C;③打开抽气泵置换系统内空气;④采集无尘、干燥的气样;⑤关闭系统,停止采样。 II. NOx含量的测定 将VL气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO3-,加水稀释至100.00 mL。量取20.00 mL该溶液,加入V1 mL c1 mol·L-1 FeSO4标准溶液(过量),充分反应后,用c2 mol·L-1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗V2 mL。 (1)NO被H2O2氧化为NO3-的离子方程式是___________。 (2)滴定操作使用的玻璃仪器主要有___________。 (3)滴定过程中发生下列反应: 3Fe2+ +NO3-+4H+ = NO↑+3Fe3+ +2H2O Cr2O72-+ 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O 则气样中NOx折合成NO2的含量为_________mg·m-3。 (4)判断下列情况对NOx含量测定结果的影响(填“偏高” 、“偏低”或“无影响 ”)若缺少采样步骤③,会使测试结果___________。若FeSO4标准溶液部分变质,会使测定结果___________。 |
|
| 22. 计算题 | 详细信息 |
|
碱式硫酸铝溶液可用于烟气脱硫。室温下向一定浓度的硫酸铝溶液中加入一定量的碳酸钙粉末,反应后经过滤得到碱式硫酸铝溶液,反应方程式为(2−x)Al2(SO4)3+3xCaCO3+3xH2O=2[(1−x)Al2(SO4)3·xAl(OH)3]+3xCaSO4↓+3xCO2↑。生成物(1−x)Al2(SO4)3·xAl(OH)3中x值的大小影响碱式硫酸铝溶液的脱硫效率。 通过测定碱式硫酸铝溶液中相关离子的浓度确定x的值,测定方法如下: ①取碱式硫酸铝溶液25.00 mL,加入盐酸酸化的过量BaCl2溶液充分反应,静置后过滤、洗涤,干燥至恒重,得固体2.3300 g。 ②取碱式硫酸铝溶液2.50 mL,稀释至25 mL,加入0.1000 mol·L−1EDTA标准溶液25.00 mL,调节溶液pH约为4.2,煮沸,冷却后用0.08000 mol·L−1CuSO4标准溶液滴定过量的EDTA至终点,消耗CuSO4标准溶液20.00 mL(已知Al3+、Cu2+与EDTA反应的化学计量比均为1∶1)。 计算(1−x)Al2(SO4)3·xAl(OH)3中的x值(写出计算过程)___________________________。 |
|
最近更新