宝鸡市试卷带解析及答案
| 1. 选择题 | 详细信息 |
|
下列有关说法不正确的是( ) A.酒精可以杀灭病毒是因为其能使构成病毒的蛋白质变性 B.“酸可以除锈”、“洗涤剂可以去油”都是发生了化学反应 C.新能源汽车的推广与使用有利于减少光化学烟雾的产生 D.利用肥皂水处理蚊虫叮咬,主要是利用肥皂水的弱碱性 |
|
| 2. 选择题 | 详细信息 |
|
国际计量大会第26次会议新修订了阿伏伽德罗常数(NA=6.022214076×1023mol-1),并于2019年5月20日正式生效。下列说法正确的是( ) A.标准状况下,2.24L CCl4中含有的分子总数为0.1NA B.氢氧根离子与铵根离子所含电子数相同 C.标准状况下,80g SO3中含3NA个氧原子 D.相同物质的量的气体在标准状况和25℃、101kPa时的体积相等 |
|
| 3. 选择题 | 详细信息 |
|
化学实验要注意安全,下列实验操作或实验事故的处理方法正确的是( ) A.不慎将浓硝酸沾到皮肤上,立即用 B.不慎将酸液溅到眼中,应立即用水冲洗,边洗边眨眼睛 C.不慎将烧碱溶液沾到皮肤上,立即用硫酸中和并冲洗 D.配制硫酸溶液时,先在量筒中加入一定体积的水,再边搅拌边慢慢加入浓硫酸 |
|
| 4. 选择题 | 详细信息 |
|
下图所示的装置或操作存在错误不能达到相应目的的是( ) A.  从NaCI溶液提取NaCl固体 从NaCI溶液提取NaCl固体B.  实验室中制取少量蒸馏水 实验室中制取少量蒸馏水C.  闻气体的气味 闻气体的气味D.  分离油和水的混合物 分离油和水的混合物 |
|
| 5. 选择题 | 详细信息 | ||||||||
2020年5月新修订的《北京市生活垃圾管理条例》将正式实施,垃圾分类并回收利用,可以减少污染,节约自然资源。下列垃圾投放有错误的是
|
|||||||||
| 6. 选择题 | 详细信息 |
|
下列说法中不正确的是( ) ①用小苏打可用于治疗胃酸过多 ②SO2的水溶液能导电,所以SO2是电解质 ③液态HCl不导电,所以HCl是非电解质 ④硫酸氢钠电离出的阳离子有氢离子,所以硫酸氢钠是酸 ⑤制备Fe(OH)3胶体,通常是将饱和氯化铁溶液与氢氧化钠溶液混合加热 ⑥某溶液中加入盐酸产生使澄清石灰水变浑浊的气体,则一定含有 A.①③④⑤⑥ B.②③④⑤⑥ C.①②④⑥ D.①②③④ |
|
| 7. 选择题 | 详细信息 |
|
下列反应的离子方程式书写正确的是( ) A.硫酸铜溶液和氢氧化钡溶液混合:Ba2++ B.稀醋酸滴在石灰石上:CaCO3+2H+= Ca2++H2O+CO2↑ C.氯化铁溶液蚀刻印刷铜电路板:Cu+Fe3+= Cu2++Fe2+ D.用稀硫酸清洗铁锈(Fe2O3):Fe2O3+6H+= 2Fe3++3H2O |
|
| 8. 选择题 | 详细信息 | |||||||||||||||
下列分类中错误的是( )
|
||||||||||||||||
| 9. 选择题 | 详细信息 |
|
同温同压下,相同体积的SO2和CO2:①质量相等;②密度相等;③分子数相等;④氧原子数相等;⑤电子数相等,其中正确的是( ) A.①②③④ B.②③④⑤ C.③④ D.③⑤ |
|
| 10. 选择题 | 详细信息 |
|
下列叙述正确的是( ) A.相同条件下的一氧化碳气体和氮气,若体积相等,则质量一定相等 B.等物质的量的甲烷和一氧化碳,在不同条件下所含的分子数不一定相等 C.1L一氧化碳气体一定比1L氧气的质量小 D.同温同压下,相同体积的物质,其物质的量一定相等 |
|
| 11. 选择题 | 详细信息 | ||||||||||||||||||||
下列实验中,所采取的分离方法与对应原理都正确的是 ( )
|
|||||||||||||||||||||
| 12. 选择题 | 详细信息 |
|
用胆矾配制0.1mol/L的硫酸铜溶液。下述方法中,最合理的是( ) A.取25克胆矾溶于1000毫升水中 B.取25克胆矾加热使其失去全部结晶水,然后溶于1000毫升水中 C.称取25克胆矾溶于水,然后将此溶液稀释至1L D.将胆矾加热失去全部结晶水后,称取16克无水硫酸铜溶解于少量水,然后加水配成1000毫升溶液 |
|
| 13. 选择题 | 详细信息 |
|
下列叙述正确的是( ) A.有单质产生的分解反应一定是氧化还原反应 B.氧化还原反应的本质是化合价发生变化 C.氧化剂在同一反应中既可以是反应物,也可以是生成物 D.还原剂在反应中发生还原反应 |
|
| 14. 选择题 | 详细信息 |
|
下列氧化还原反应中,电子转移的方向和数目均正确的是 ( ) A.  B.  C. 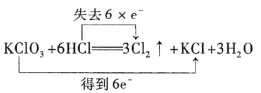 D. 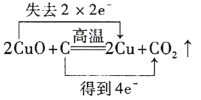 |
|
| 15. 选择题 | 详细信息 |
|
常温下,下列各组离子在指定溶液中一定能大量共存的是( ) A.pH=1的溶液中: B.无色透明的溶液中:K+、 C.遇石蕊变蓝的溶液中: D.含大量NO |
|
| 16. 选择题 | 详细信息 |
|
对于化学反应CaH2+2H2O = Ca(OH)2+2H2↑,下列说法正确的是( ) ①H2只是氧化产物 ②H2只是还原产物 ③H2O是氧化剂 ④CaH2中的H元素被还原 ⑤此反应中的氧化产物和还原产物的分子数之比是1:1 ⑥反应中若有2mol H2生成,则有4mol电子发生转移 A.①④⑤ B.③⑤ C.①⑥ D.②④ |
|
| 17. 选择题 | 详细信息 |
|
VLFe2(SO4)3溶液中含有a克的 A. |
|
| 18. 选择题 | 详细信息 |
|
在溶液中,0.2mol A.+1 B.+2 C.+3 D.+4 |
|
| 19. 选择题 | 详细信息 |
|
制印刷电路时常用FeCl3溶液腐蚀铜,向盛有FeCl3溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是 A. 烧杯中有铜无铁 B. 烧杯中有铁无铜 C. 烧杯中铜、铁都有 D. 烧杯中铜、铁都没有 |
|
| 20. 选择题 | 详细信息 |
纳米级Fe3O4可用于以太阳能为热源分解水制H2,过程如图所示。下列说法中不正确的是 A.过程 Ⅰ 的反应:2Fe3O4 B.过程 Ⅱ 的反应:2H2O=2H2↑+O2↑ C.两个转化过程都发生了氧化还原反应 D.Fe3O4为整个过程的催化剂 |
|
| 21. 填空题 | 详细信息 |
|
有以下物质:①石墨;②铜;③酒精;④氨水;⑤二氧化碳;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氯化氢气体 ⑩碳酸钙固体。 请将选择合适物质的序号填在横线上。 (1)其中能导电的是__________; 属于非电解质的是__________; 属于强电解质的是_________;属于弱电解质的是__________。 (2)按要求回答问题: ① 写出物质⑥的溶液与硫酸氢钠溶液反应的离子方程式:______________; ② 写出⑤和足量的⑦反应的离子方程式:____________________; ③ 写出⑨的水溶液和⑩反应的化学方程式:___________________; |
|
| 22. 填空题 | 详细信息 |
|
现有21.6g由CO和CO2组成的混合气体,在标准状况下其体积为13.44 L。回答下列问题: (1)该混合气体中CO与CO2的分子数之比________________; (2)混合气体中氧原子的物质的量为______________________; (3)将混合气体依次通过如图所示装置,最后收集在气球中(实验在标准状况下测定)。 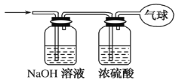 ① 气球中收集到的气体的摩尔质量为______; ② 气球中收集到的气体中,电子总数为___ (用NA表示阿伏加德罗常数的值)。 ③ 气球的体积为___________________L。 |
|
| 23. 实验题 | 详细信息 |
|
“84”消毒液能有效杀灭甲型H1N1等病毒,某同学购买了一瓶“威露士”牌“84”消毒液,并查阅相关资料和消毒液包装说明得到如下信息:含25% NaClO、1000 mL、密度1.192 g•cm-3、稀释后使用。 请根据信息和相关知识回答下列问题: (1)该“84”消毒液的物质的量浓度约为____mol·L-1。 (2)该同学参阅该“84”消毒液的配方,欲用NaClO固体配制480 mL含25% NaClO的该“84”消毒液。请回答下列问题: ① 如下图所示的仪器中,有四种是不需要的,还需的玻璃仪器有__________;(填仪器的名称)  ② 容量瓶用蒸馏水洗净后不烘干,对配制结果____(填“是”或“否”)有影响; ③ 已知NaClO久置在空气中会部分变质,因此利用购买的商品来配制可能导致结果___________(填“偏高”或“不变”或“偏低”); ④ 定容时,液面离容量瓶颈刻度线下______时,改用_________滴加蒸馏水至液面与刻度线相切。 ⑤ 配制480 mL该“84”消毒液,应选取_______的容量瓶,需要称量的NaClO固体质量为___________。 |
|
| 24. 填空题 | 详细信息 |
|
(1)H2O2水溶液称双氧水,医疗上利用它有杀菌消毒作用来清洗伤口,对下列两个涉及H2O2的反应,填写下列空白: A.H2O2 + Cl2 = 2HCl + O2 B.H2O2 + 2 ① H2O2仅体现氧化性的反应是___________(填代号,下同) ② H2O2仅体现还原性的是_______________ (2)已知CuO具有氧化性,能够与NH3反应生成两种单质和H2O,请写出在加热条件下CuO与NH3反应的化学方程式_________________; (3)在一定条件下, (4)已知如下反应,请针对下述两个反应回答问题: A 2H2O+Cl2+SO2=H2SO4+2HCl B 2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O ① 两反应中的氧化剂的氧化性强弱顺序为________,还原剂的还原性强弱顺序为________(用物质的化学式表示)。 ② 在反应②中氯化氢表现出的性质是________。 a.还原性 b.酸性 c.氧化性 |
|
最近更新







