2018-2019年高二第一学期12月份考试化学考试完整版(云南省盐津县三中)
| 1. 选择题 | 详细信息 |
|
主族元素原子失去最外层电子形成阳离子,主族元素原子得到电子填充在最外层形成阴离子。下列各原子或离子的电子排布式错误的是( ) A. Ca2+ 1s22s22p63s23p6 B. O2- 1s22s23p4 C. Fe 1s22s22p63s23p63d64s2 D. Fe2+ 1s22s22p63s23p63d6 |
|
| 2. 选择题 | 详细信息 |
|
为揭示原子光谱是线状光谱这一事实,玻尔提出了核外电子的分层排布理论。下列说法中,不符合这一理论的是( ) A. 电子绕核运动具有特定的半径和能量 B. 电子在特定半径的轨道上运动时不辐射能量 C. 电子跃迁时,会吸收或放出特定的能量 D. 揭示了氢原子光谱存在多条谱线 |
|
| 3. 选择题 | 详细信息 |
|
下列符号中表示电子云伸展方向的是( ) A. K、L、M、N B. s、p、d、f C. px、py、pz D. ↑、↓ |
|
| 4. 选择题 | 详细信息 |
|
下列比较正确的是( ) A. 第一电离能:I1(P)>I1(S) B. 离子半径:r(Al3+)>r(O2-) C. 能量:E(4s)>E(3d) D. 电负性:K原子>Na原子 |
|
| 5. 选择题 | 详细信息 |
|
下列原子或离子原子核外电子排布不属于基态排布的是 A. N:1s22s22p3 B. S2-:1s22s22p63s23p6 C. Na:1s22s22p53s2 D. Si:1s22s22p63s23p2 |
|
| 6. 选择题 | 详细信息 |
|
若以E(nl)表示某能级的能量,以下各式中正确的是( ) A. E(3s)>E(2s)>E(1s) B. E(3s)>E(3p)>E(3d) C. E(4f)>E(4s)>E(3d) D. E(5s)>E(4s)>E(4f) |
|
| 7. 选择题 | 详细信息 |
|
以下符号正确的是 A. 2d1 B. 3f7 C. 6s3 D. 7p2 |
|
| 8. 选择题 | 详细信息 |
|
下列原子半径最小的是( ) A. 1s22s22p3 B. 1s22s22p33s23p3 C. 1s22s22p5 D. 1s22s22p33s23p2 |
|
| 9. 选择题 | 详细信息 |
|
下面有关“核外电子的运动状态”的说法,其中错误的是( )。 A. 能级是描述电子运动的电子云形状 B. 只有在电子层、能级、电子云的伸展方向及电子的自旋状态都确定时,电子的运动状态才能被确定下来 C. 必须在B项所述四个方面都确定时,才能确定组成每一电子层的最多轨道数 D. 电子云伸展方向与能量大小是无关的 |
|
| 10. 选择题 | 详细信息 |
|
下列说法正确的是( ) A. 第三周期所含的元素中钠的第一电离能最小 B. 铝的第一电离能比镁的第一电离能大 C. 在所有元素中,氟的第一电离能最大 D. 钾的第一电离能比镁的第一电离能大 |
|
| 11. 选择题 | 详细信息 |
|
下列分子中所有原子都满足最外层8电子结构的是( ) A. 光气(COCl2) B. 六氟化硫 C. 二氟化氙 D. 三氟化硼 |
|
| 12. 选择题 | 详细信息 |
|
下列不能形成配位键的组合是( )。 A.Ag+、NH3 B.H2O、H+ C.Co3+、CO D.Ag+、H+ |
|
| 13. 选择题 | 详细信息 |
|
Co(Ⅲ)的八面体配合物CoClm•nNH3,若1mol配合物与AgNO3作用生成1molAgCl沉淀,则m、n的值是( ) A. m=3 n=6 B. m=3 n=4 C. m=4 n=1 D. m=4 n=5 |
|
| 14. 选择题 | 详细信息 |
|
下列叙述中正确的是 A.以非极性键结合起来的双原子分子一定是非极性分子 B.以极性键结合起来的分子一定是极性分子 C.非极性分子只能是双原子单质分子 D.非极性分子中,一定含有非极性共价键 |
|
| 15. 选择题 | 详细信息 |
|
N—H键能的含义是( ) A. 由N和H形成1 mol NH3所放出的热量 B. 把1 mol NH3的键全部拆开所吸收的热量 C. 拆开6.02×1023个N—H键所吸收的能量 D. 形成1个N—H键所放出的热量 |
|
| 16. 选择题 | 详细信息 |
|
已知NH3分子可与Cu2+形成配位化合物离子[Cu(NH3)4] 2+, 则除去硫酸铜溶液中少量硫酸可选用的试剂是 A. NaOH B. NH3 C. BaCl2 D. Cu(OH) 2 |
|
| 17. 选择题 | 详细信息 |
|
在硼酸[B(OH)3]分子中,B原子与3个羟基相连,其晶体具有与石墨相似的层状结构。则分子中B原子杂化轨道的类型及同层分子间的主要作用力分别是 A. sp,范德华力 B. sp2,范德华力 C. sp2,氢键 D. sp3,氢键 |
|
| 18. 选择题 | 详细信息 |
|
下列物质中含有非极性键且为盐的是( ) A. CH3COONa B. NH4Cl C. CaCl2 D. H2O2 |
|
| 19. 选择题 | 详细信息 |
|
下列说法中正确的是( ) A. 烯中C=C的键能是乙烷中C-C的键能的2倍 B. 氮气分子中含有1个s键和2个p键 C. N-O键的极性比C-O键的极性大 D. NH4+中4个N-H键的键能不相同 |
|
| 20. 选择题 | 详细信息 |
|
下列关于共价键的说法,正确的是 A.分子内部一定会存在共价键 B.由非金属元素组成的化合物内部一定全是共价键 C.非极性键只存在于双原子单质分子中 D.离子化合物的内部可能存在共价键 |
|
| 21. 选择题 | 详细信息 |
|
下列有关离子晶体的数据大小比较不正确的是( ) A. 熔点:NaF>MgF2>AlF3 B. 晶格能:NaF>NaCl>NaBr C. 阴离子的配位数:CsCl>NaCl>CaF2 D. 硬度:MgO>CaO>BaO |
|
| 22. 选择题 | 详细信息 |
已知CsCl晶体的密度为ρg·cm-3,NA为阿伏加德罗常数,相邻的两个Cs+的核间距为acm,如图所示,则CsCl的相对分子质量可以表示为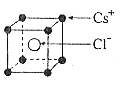 A. NA·a3·ρ B. NA·a3·ρ/6 C. NA·a3·ρ/4 D. NA·a3·ρ/8 |
|
| 23. 选择题 | 详细信息 |
|
下面关于SiO2晶体网状结构的叙述正确的是 A. 存在四面体结构单元,O处于中心,Si处于4个顶角 B. 最小的环上,有3个Si原子和3个O原子 C. 最小的环上,Si和O原子数之比为1:2 D. 最小的环上,有6个Si原子和6个O原子 |
|
| 24. 选择题 | 详细信息 |
|
下列有关晶体和非晶体的说法中正确的是( ) A. 具有规则几何外形的固体均为晶体 B. 晶体具有自范性,非晶体没有自范性 C. 晶体研碎后即变为非晶体 D. 将玻璃加工成规则的固体即变成晶体 |
|
| 25. 选择题 | 详细信息 |
二氧化硅晶体是空间立体网状结构,如图所示: 关于二氧化硅晶体的下列说法中,正确的是( ) A. 1 mol SiO2晶体中Si—O键为2 mol B. 二氧化硅晶体的分子式是SiO2 C. 晶体中Si、O原子最外电子层都满足8电子结构 D. 晶体中最小环上的原子数为8 |
|
| 26. 选择题 | 详细信息 |
|
金刚石是典型的原子晶体,下列关于金刚石的说法中错误的是( ) A.晶体中不存在独立的“分子” B.碳原子间以共价键相结合 C.是硬度最大的物质之一 D.化学性质稳定,即使在高温下也不会与氧气发生反应 |
|
| 27. 选择题 | 详细信息 |
|
下列关于晶体的说法一定正确的是( ) A. 第ⅠA族碱金属元素与ⅦA族元素所形成的化合物在固态时为离子晶体,晶体中阴、阳离子排列方式相同 B. 晶体中存在阴离子就必定存在阳离子,存在阳离子就必定存在阴离子 C. 离子晶体中只含有离子键,分子晶体、原子晶体中必定含有共价键 D. C60晶体(其结构模型如图)中每个C60分子周围与它距离最近且等距离的C60分子有12个 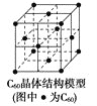 |
|
| 28. 选择题 | 详细信息 |
|
下列数据是对应物质的熔点,有关判断错误的是( ) A. 含有金属阳离子的晶体不一定是离子晶体 B. 在共价化合物分子中各原子都满足8电子稳定结构 C. 同族元素的氧化物可形成不同类型的晶体 D. 金属晶体的熔点不一定比分子晶体的高 |
|
| 29. 综合题 | 详细信息 |
|
原子中质子、中子、电子的数量、质量和电性之间存在一定的相互关系。请填写下列空白: (1)质子数决定________的种类;质子数和中子数决定________的种类。 (2) (3)质量数=________+________,对任一原子,核电荷数=________;对中性原子,核外电子数=________。 (4)ZXn-中核外电子数=________,ZXn+中核外电子数为________。 |
|
| 30. 填空题 | 详细信息 |
|
氯化铬酰(CrO3Cl2)在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。请回答下列问题。 (1)写出铬原子的基态电子排布式:____________________,与铬同周期的所有元素的基态原子中最外层电子数与铬原子相同的元素有________(填元素符号)。 (2)CrO2Cl2常温下为深红色液体,能与CCl4,CS2等互溶,据此可判断CrO2Cl2是________分子(填“极性”或“非极性”)。 (3)在①苯、②CH3OH,③HCHO,④CS2,⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有________(填序号),CS2分子的空间构型是________,易溶于水的有________(填序号),理由是:_______________________________。 |
|
| 31. 综合题 | 详细信息 |
|
传统中药的砷剂俗称“砒霜”,请回答下列问题: (1)砷剂的分子结构如图甲所示.该化合物中As原子的杂化方式为__. (2)基态砷原子的价层电子排布式为__,砷与硒的第一电离能较大的是__. (3)已知:  依据表中数据解释NH3熔点最高的原因__. (4)砷酸(H3AsO4)是一种三元中强酸,根据价层电子对互斥理论推测AsO43﹣的空间构型为__. (5)砷镍合金的晶胞如图乙所示,该晶体中与每个Ni原子距离最近的As原子有__个. 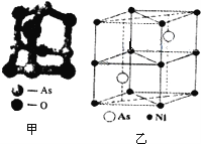 |
|
| 32. 填空题 | 详细信息 |
C60、金刚石和石墨的结构模型如图所示(石墨仅表示其中的一层结构): (1)C60、金刚石和石墨三者的关系互为___________。 A.同分异构体 B.同素异形体 C.同系物 D.同位素 (2)硅晶体的结构跟金刚石相似,1 mol硅晶体中含有硅硅单键的数目约是____________ NA个。二氧化硅的结构相当于在硅晶体结构中每个硅硅单键之间插入一个氧原子。二氧化硅的空间网状结构中,硅、氧原子形成的最小环上氧原子数目是___________。 (3)石墨层状结构中,平均每个正六边形拥有的碳原子个数是个___________。 |
|
| 33. 综合题 | 详细信息 |
|
(1)配位化学创始人维尔纳发现,取COCl3•6NH3(黄色)、CoCl3•5NH3(紫红色)、COCl3•4NH3(绿色)和COCl3•4NH3(紫色)四种化合物各1mol,分别溶于水,加入足量硝酸银溶液,立即产生氯化银,沉淀的量分别为3mol、2mol、1mol和1mol. ①请根据实验事实用配合物的形式写出它们的化学式. COCl3•6NH3__,COCl3•5NH3__,COCl3•4NH3(绿色和紫色)__. ②后两种物质组成相同而颜色不同的原因是__. ③上述配合物中,中心离子的配位数都是__. (2)向黄色的三氯化铁溶液中加入无色的KSCN溶液,溶液变成血红色.该反应在有的教材中用方程式FeCl3+3KSCN═Fe(SCN)3+3KCl表示.经研究表明,Fe(SCN)3是配合物,Fe3+与SCN﹣不仅能以1:3的个数比配合,还可以其他个数比配合.请按要求填空: ①Fe3+与SCN﹣反应时,Fe3+提供__,SCN﹣提供__,二者通过配位键结合. ②所得Fe3+与SCN﹣的配合物中,主要是Fe3+与SCN﹣以个数比1:1配合所得离子显血红色.含该离子的配合物的化学式是__. ③若Fe3+与SCN﹣以个数比1:5配合,则FeCl3与KSCN在水溶液中发生反应的化学方程式可以表示为:_____________。 |
|
最近更新



