2020年河南省濮阳市油田中考模拟化学试卷
| 1. 选择题 | 详细信息 |
|
下列现象不涉及化学变化的是 A. 蜡烛燃烧 B. 酒精挥发 C. 食物腐败 D. 塑料降解 |
|
| 2. 选择题 | 详细信息 |
|
绿色发展理念以人与自然和谐为价值取向。下列物质的大量排放不违背这一理念的是 A.二氧化碳 B.固体粉尘 C.工业废水 D.氮气 |
|
| 3. 选择题 | 详细信息 |
|
下列物质的构成微粒与构成氯化钠的微粒种类相同的是 A.铁 B.氢氧化钠 C.液氮 D.二氧化硫 |
|
| 4. 选择题 | 详细信息 |
高纯硅是半导体、集成电路、光伏电池的制作材料。硅的原子结构示意图如下图所示。下列有关硅元素的说法中不正确的是 A.位于元素周期表第三周期 B.x代表的数字为14 C.其氧化物的化学式为SiO2 D.是地壳中含量最高的非金属元素 |
|
| 5. 选择题 | 详细信息 |
|
下列有关水的说法不正确的是 A.冰水共存物属于纯净物 B.明矾可以促进水中悬浮物的沉降 C.pH小于7的雨水就是酸雨 D.水变成水蒸气,水分子间隔增大 |
|
| 6. 选择题 | 详细信息 |
下列实验设计能够实现其对应实验目的的是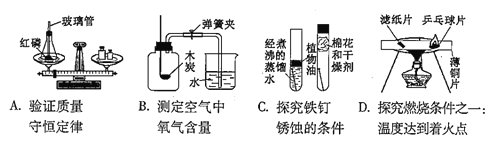 A. A B. B C. C D. D |
|
| 7. 选择题 | 详细信息 |
|
根据生活经验和所学知识判断,下列鉴别物质的试剂或方法错误的是 A.用灼烧后闻气味的方法区分棉线和羊毛线 B.用水可以鉴别氢氧化钠、硝酸铵两种白色固体 C.用酚酞试液可以区分稀硫酸、硫酸钠两种无色溶液 D.用加熟石灰混合研磨后闻气味的方法,区分硫酸铵固体和氯化钾固体 |
|
| 8. 选择题 | 详细信息 |
|
实验室配制一定溶质质量分数的氯化钠溶液时,下列操作会导致结果偏大的是 ①称量的氯化钠固体中含有不溶性杂质;②用量筒量取水时俯视读数; ③往烧杯中加水时有水洒出;④将配制好的溶液装入试剂瓶中时有少量溅出。 A. ①② B. ②③ C. ②④ D. ③④ |
|
| 9. 选择题 | 详细信息 |
小林在学习中构建的“氮元素及其化合物的化合价与物质类别之间的关系图”(如下图)。下列说法中不正确的是 A.a为N2 B.b为NO C.c为HNO3 D.d可能是NaNO3 |
|
| 10. 选择题 | 详细信息 |
|
下列除去杂质(括号内物质)的方法正确的是 A.NaOH溶液(Na2CO3): 加适量稀盐酸 B.Cu (氧化铜):加入足量稀硫酸,过滤 C.CO2 (CO):通入氧气,点燃 D.KCl (MnO2):加足量水溶解、过滤、洗涤、烘干 |
|
| 11. 选择题 | 详细信息 |
|
下列四个图像分别与选项中的操作相对应,其中合理的是 A. 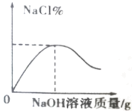 向一定量的盐酸中滴加氢氧化钠溶液 向一定量的盐酸中滴加氢氧化钠溶液B.  向一定量的饱和石灰水中加入生石灰 向一定量的饱和石灰水中加入生石灰C.  向等质量的碳酸镁和碳酸氢钠中分别加入足量的稀盐酸 向等质量的碳酸镁和碳酸氢钠中分别加入足量的稀盐酸D.  向一定量氢氧化钠和氯化钡的混合溶液中加入稀硫酸 向一定量氢氧化钠和氯化钡的混合溶液中加入稀硫酸 |
|
| 12. 选择题 | 详细信息 |
甲、乙、丙的转化关系如图所示(“→”表示反应能一 步实现转化,“一”表示相连的物质之间可以发生反应,部分反应物、生成物及反应条件已略去)。下列各组物质(按甲、乙、丙顺序)中,不能实现上述转化的是 A.C、CO、O2 B.CuSO4、CuCl2、 Cu(OH)2 C.Zn、Fe、H2SO4 D.Na2CO3、Na2SO4、 BaC l2 |
|
| 13. 选择题 | 详细信息 |
|
有一包Mg和MgO的混合物共12.8 g,与一定量的稀硫酸恰好完全反应,所得溶液中溶质的质量为48 g,则原混合物中氧元素的质量为 A. 1.6 g B. 2.4 g C. 3.2 g D. 9.6 g |
|
| 14. 填空题 | 详细信息 |
| 形成化合物种类最多的元素是____________ ;钙、锌、铁、碘元素都属于人体必需的元素,其中属于常量元素的是_________________。 | |
| 15. 填空题 | 详细信息 |
| 氢能源作为理想的能源,其优点是______________(答一 条即可) ;氢化镁(MgH2)可以储氢,氢化镁和水反应生成一种碱和一 种可燃性 气体单质,该反应的化学方程式为_____________; 煤是传统能源,等质量的煤粉比煤块燃烧的更快、更剧烈,其原因是______________________。 | |
| 16. 填空题 | 详细信息 |
我国科学家成功合成新型催化剂,能将CO2高效转化为甲醇(CH3OH).这不仅可以缓解碳排放引起的温室效应,还将成为理想的能源补充形式。该化学反应的微观过程如下图所示。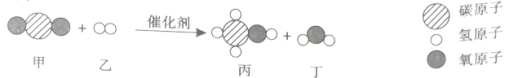 (1)物质丙属于___________(填“无机物”或“有机物”); (2) 物质丁的化学式_________________; (3) 参加反应的甲、乙物质分子个数比为________________。 |
|
| 17. 填空题 | 详细信息 |
A、B、C三种固体的溶解度曲线如图所示。请回答: t2°C时,在50g水中加入50gA物质,充分溶解后得到溶液的质量为____________; t1°C时,将48g A的饱和溶液稀释为质量分数为5%的溶液,需加水的质量为____________; 将t2°C时 A、B、C三种物质的饱和溶液降温到t1°C,所得溶液中溶质的质量分数由大到小的顺序是_________________。 |
|
| 18. 推断题 | 详细信息 |
A~F 均为初中化学常见的物质,它们之间的关系如下图所示(“→”表示某一种物质经一步反应可转化为另一种物质,部分反应物、生成物及反应条件已略去),其中 A俗名为生石灰,C为常见的溶剂,C与E元素组成相同。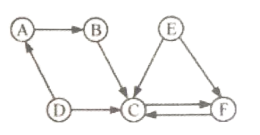 请回答下列问题: (1) F的化学式为______________________。 (2) B在农业上的用途是_______________(写一种)。 (3)由D转化为C的化学方程式为___________。 |
|
| 19. 填空题 | 详细信息 |
| 铝是较活泼的金属,但铝制品耐腐蚀,其原因是___________。某金属混合物样品由Al、Fe、Zn三种金属中的两种组成,取5.6g样品与足量的稀硫酸反应,产生0.2g氢气,则该样品中一定不含的金属是_________。 | |
| 20. 实验探究题 | 详细信息 |
下图是实验室制取气体的部分装置。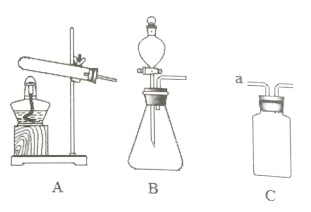 (1)写出实验室用B装置制氧气的化学方程式___________。 (2)加热氯化铵和碱石灰的固体混合物可以制取氨气(化学式为NH3,极易溶于水)。应选择的气体发生装置是___________(填序号);若用C装置采用排空气法收集氨气(气体从a管通入),请把C中的导气管补画完整___________。 |
|
| 21. 填空题 | 详细信息 |
|
将锌粉加入到一定质量Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,可以得到溶液和固体。 (1)若向固体中加入稀盐酸,无气泡产生。写出一定发生反应的化学方程式___________。 (2)若反应前后混合溶液的质量相等,则所得固体中一定含有什么物质___________? |
|
| 22. 流程题 | 详细信息 |
氯碱工业以粗盐(主要成分是NaCl, 含少量泥沙、CaCl2、 MgCl2)为原料,生产氯气和氢氧化钠,模拟流程如下: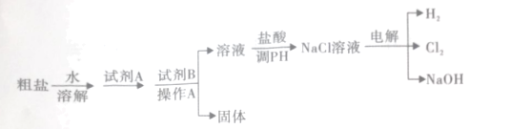 (1)试剂A与试剂B的组合为____________(填序号) ①KOH ②NaOH ③K2CO3 ④Na2CO3 (2)操作A中用到的玻璃仪器有哪些___________? (3)写出电解NaCl溶液的化学方程式___________。 |
|
| 23. 实验探究题 | 详细信息 |
已知甲酸(HCOOH)具有挥发性,在热的浓硫酸中分解生成一氧化碳 和水。用右图所示装置制取CO,用CO还原氧化铁,并检验气体产物。 (1)氢氧化钠固体的作用是什么___________? (2)写出B中Fe2O3反应的化学方程式___________。 |
|
| 24. 简答题 | 详细信息 |
酸、碱、盐是初中化学学到的重要化合物。 (1)盐酸和硫酸具有相似的化学性质,是因为____________;右图是稀盐酸与氢氧化钠溶液反应时pH变化示意图,X代表的是______________溶液。 (2)写出盐酸除铁锈(Fe2O3) 的化学方程式____________________。 (3)用图1装置进行实验,先后将两种溶液快速全部推入(推入一种溶液充分反应后,再推入另一种溶液),测得一段时间内压强变化如图2所示。  ①先推入的溶液是___________。 ②bc段压强不变,其原因是什么___________? ③cd段压强变大,其原因是什么___________? (用化学方 程式表示) (4)像氢氧化钠与稀盐酸的反应、CO2 与氢氧化钠的反应,对于这些无明显现象的化学反应,要证明反应确实发生了,你的设计思路是____________________。 (5)某纯碱含有少量的氯化钠,为测定某纯碱样品中碳酸钠的含量,取12g样品置于烧杯中,加水将其溶解,再滴加氯化钙溶液,产生沉淀的质量与加入氯化钙溶液的质量关系如图所示。 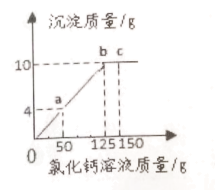 ①求该纯碱样品中碳酸钠的质量分数___________。 ②若要计算CaCl2溶液的质量分数,可使用右图中__________点 (从a、b、c中选择)对应的一组数据。 |
|
最近更新



