河南省郑州市第一〇六高级中学2020-2021年高二前半期11月考试化学题同步训练免费试卷
| 1. 选择题 | 详细信息 |
|
某化学反应其△H= -250 kJ/mol,∆S=18 J/(mol·k),则此反应在下列哪种情况下可自发进行( ) A.在任何温度下都能自发进行 B.在任何温度下都不能自发进行 C.仅在高温下自发进行 D.仅在低温下自发进行 |
|
| 2. 选择题 | 详细信息 |
|
在HNO2溶液中存在如下平衡:HNO2 A.水 B.硫酸 C.NaNO2固体 D.NaHSO4固体 |
|
| 3. 选择题 | 详细信息 |
|
在一密闭烧瓶中,在25℃时存在如下平衡:2NO2(g) ①颜色 ②平均相对分子质量 ③质量 ④压强 ⑤密度 A.①和③ B.③和⑤ C.④和⑤ D.②和④ |
|
| 4. 选择题 | 详细信息 |
一定条件下,在2L密闭容器中加入等物质的量的FeO和CO,发生下列反应:FeO(s)+CO(g)⇌Fe(s)+CO2(g),在T1、T2温度下,物质的量n随时间t变化的曲线如图所示,下列叙述正确的是( ) A.平衡前,随着反应的进行,容器内气体的相对分子质量始终不变 B.平衡时,其他条件不变,取出适当铁可提高CO的转化率 C.该反应的△H<0,K1<K2=1.5 D.当反应进行到t1时刻仅改变一个条件,可能是通入了氮气 |
|
| 5. 选择题 | 详细信息 |
|
某温度下,当1 g氨气完全分解为氮气、氢气时,吸收2.72 kJ的热量,则此状态下,下列热化学方程式正确的是 ( ) ①N2(g)+3H2(g) = 2NH3(g) ΔH=-92.4 kJ/mol ②N2(g)+3H2(g) = 2NH3(g) ΔH=-46.2 kJ/mol ③NH3(g) = ④2NH3(g) = N2(g)+3H2(g) ΔH=-92.4 kJ/mol A.①② B.①③ C.①②③ D.全部 |
|
| 6. 选择题 | 详细信息 |
|
在容积不变的密闭容器中,一定条件下发生反应:2A(?)B(g)+C(s),达到化学平衡后,升高温度,容器内气体的密度增大,则下列叙述正确的是( ) A. 若正反应是吸热反应,则A为非气态 B. 若正反应是放热反应,则A为非气态 C. 在平衡体系中加入少量C,该平衡向逆反应方向移动 D. 改变压强对该平衡的移动一定无影响 |
|
| 7. 选择题 | 详细信息 |
|
2.0mol PCl3和1.0molCl2充入体积不变的密闭容器中,在一定条件下发生下述反应:PCl3(g)+ Cl2(g) A.0.2mol B.小于0.2mol C.大于0.2mol,小于0.4 mol D.无法确定 |
|
| 8. 选择题 | 详细信息 |
下列图示与对应的叙述不相符合的是 A. 图甲表示燃料燃烧反应的能量变化 B. 图乙表示酶催化反应的反应速率随反应温度的变化 C. 图丙表示弱电解质在水中建立电离平衡的过程 D. 图丁表示强碱滴定强酸的滴定曲线 |
|
| 9. 选择题 | 详细信息 |
经一定时间后,可逆反应aA+bB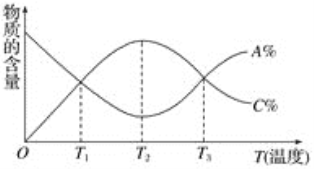 A.该反应在T1、T3温度时达到化学平衡 B.该反应在T2温度时达到化学平衡 C.该反应的逆反应是放热反应 D.升高温度,平衡会向正反应方向移动 |
|
| 10. 选择题 | 详细信息 |
|
下列有关仪器使用方法或实验操作正确的是( ) A.洗净的锥形瓶和容量瓶必须放进烘箱中烘干才能开始实验 B.用容量瓶配溶液时,若加水超过刻度线,立即用滴管吸出多余液体 C.酸式滴定管装标准溶液前,必须先用该溶液润洗 D.酸碱滴定实验中,用待滴定溶液润洗锥形瓶以减小实验误差 |
|
| 11. 选择题 | 详细信息 |
|
将浓度为0.1 mol·L−1HA溶液(pH=3)加水稀释100倍,下列各量保持增大的是( ) A.c(H+) B.Ka(HA) C.c(OH-) D.c(HA) |
|
| 12. 选择题 | 详细信息 |
|
已知:t℃下的某一气态平衡体系中含有X(g)、Y(g)、Z(g)、W(g)四种物质,此温度下发生反应的平衡常数表达式为: A.升高温度,平衡常数K变大 B.增大压强,W(g)物质的量分数变大 C.升温,若混合气体的平均相对分子质量变小,则正反应放热 D.增大X浓度,平衡向正反应方向移动 |
|
| 13. 选择题 | 详细信息 |
|
下列有关电解质的说法正确的是( ) A.强电解质溶液的导电能力一定比弱电解质溶液的导电能力强 B.强电解质溶液中存在的分子只有溶剂分子 C.强电解质都是离子化合物,而弱电解质都是共价化合物 D.Na2O与水反应生成NaOH,因此Na2O是非电解质 |
|
| 14. 选择题 | 详细信息 |
|
在298K、100kPa时,已知: 2H2O(g)=2H2(g)+O2(g) △H1 H2(g)+Cl2(g)=2HCl(g) △H2 2Cl2(g)+2H2O(g)=4HCl(g)+O2(g) △H3 则△H3与△H1和△H2间的关系正确的是: A.△H3=△H1+2△H2 B.△H3=△H1+△H2 C.△H3=△H1-2△H2 D.△H3=△H1-△H2 |
|
| 15. 选择题 | 详细信息 |
|
下列说法正确的是( ) A.常温下,由水电离出的c(H+)与c(OH-)乘积为10−28的溶液中:K+、NO B.常温下,c(H+)=10−12 mol·L−1的溶液中:Na+、S2−不能大量共存 C.在测定中和热的实验中,用0.5 mol·L−1 NaOH溶液分别与0.5 mol·L−1的盐酸、醋酸溶液反应,如所取的溶液体积相等,则测得的中和热数值相同 D.纯水在25℃比100℃时的pH大 |
|
| 16. 选择题 | 详细信息 |
|
室温下,下列溶液等体积混合后,所得溶液的pH一定大于7的是( ) A.0.1 mol·L-1的盐酸和0.1 mol·L-1的氢氧化钠溶液 B.0.1 mol·L-1的盐酸和0.05 mol·L-1的氢氧化钡溶液 C.pH=4的醋酸溶液和pH=10的氢氧化钠溶液 D.pH=4的盐酸和pH=10的氨水 |
|
| 17. 选择题 | 详细信息 |
我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下。 下列说法不正确的是 A. 生成CH3COOH总反应的原子利用率为100% B. CH4→CH3COOH过程中,有C―H键发生断裂 C. ①→②放出能量并形成了C―C键 D. 该催化剂可有效提高反应物的平衡转化率 |
|
| 18. 选择题 | 详细信息 |
|
某温度下,在一个2L的密闭容器中,加入4molA和2molB进行如下反应: A.该反应的化学平衡常数表达式是K=c(C)4c(D)2/c(A)3c(B B.此时,B的平衡转化率是 C.增大该体系的压强,平衡向右移动,化学平衡常数增大 D.增加C,B的平衡转化率不变 |
|
| 19. 选择题 | 详细信息 |
浓度均为 0.10 mol·L-1 、体积均为V 的 MOH 和 ROH 溶液,分别加水稀释的变化如图所示。下列叙述错误的是( ) A.MOH 的碱性强于ROH 的碱性 B.ROH 的电离程度:b点大于a点 C.若两溶液无限稀释,则它们的c(OH-)相等 D.当lg |
|
| 20. 填空题 | 详细信息 | ||||||||||||
在一固定容积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)⇌CO(g)+H2O(g),其化学平衡常数K和温度T的关系如表:
试回答下列问题: |
|||||||||||||
| 21. 填空题 | 详细信息 | ||||||||
|
已知某气体反应的平衡常数可表示为K=c(CH3OCH3)c(H2O)/[c(CH3OH)]2,该反应在不同温度下的平衡常数:400℃,K=32;500℃,K=44。请回答下列问题: (1)写出上述反应的化学方程(标出各物质状态)________。 (2)已知在密闭容器中,测得某时刻各组分的浓度如下:
① 此时系统温度400℃,比较正、逆反应速率的大小:υ正____υ逆(填“>”、“<”或“=”)。 |
|||||||||
最近更新





