2017-2018年初三上半年期末化学题免费试卷(河北省保定市)
| 1. 选择题 | 详细信息 |
|
下列食品、调味品的制作过程中,主要发生物理变化的是 A.水果榨果汁 B.黄豆酿酱油 C.糯米酿甜酒 D.鲜奶制酸奶 |
|
| 2. 选择题 | 详细信息 |
|
下列饮品属于溶液的是 A.蔗糖水 B.奶茶 C.果粒橙 D.豆浆 |
|
| 3. 选择题 | 详细信息 |
加油站、面粉加工厂都需张贴的图标是 A. B. C. D. |
|
| 4. 选择题 | 详细信息 |
|
生活中常接触到“含氟牙膏”、“高钙牛奶”、“碘盐”、“富硒茶叶”等用品,这里的氟、钙、碘、硒指的是 A.单质 B.原子 C.离子 D.元素 |
|
| 5. 选择题 | 详细信息 |
镁有“国防金属”的美誉。在元素周期表中,镁元素的信息如下图所示,对图中信息解释不正确的是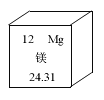 A. 原子序数为12 B. 核外电子数为 24 C. 元素符合为Mg D. 相对原子质量为24.31 |
|
| 6. 选择题 | 详细信息 |
|
食醋中约含有3%-5%的醋酸(C2H4O2),下列有关醋酸的说法正确的是 A.醋酸的相对分子质量为60g B.醋酸中碳元素的质量分数为40% C.醋酸中碳氧元素的质量比为1:1 D.一个醋酸分子中含有2个水分子 |
|
| 7. 选择题 | 详细信息 |
|
下列关于O和O2-的认识正确的是 A.它们的质子数不相同 B.它们的核外电子数相同 C.他们不属于同种元素 D.氧离子比氧原子的化学性质稳定 |
|
| 8. | 详细信息 |
|
能说明水中含有氧元素的现象的是 A. 水在常温下呈液态 B. 在加热条件下水变成气体 C. 电解水可以得到使带火星木条复燃的气体 D. 许多物质可以溶解在水中 |
|
| 9. 选择题 | 详细信息 |
如图所示,向小试管内的水中分别加入一定量的下列物质,右侧U型管中液面a升b降,则加入的物质可能是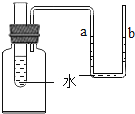 A.蔗糖 B.氢氧化钠 C.硝酸铵 D.生石灰 |
|
| 10. 选择题 | 详细信息 |
如图是X、Y两种固态物质的溶解度曲线,下列判断正确的是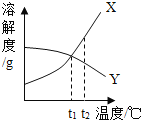 A.t1℃时,X物质和Y物质的溶解度相等 B.X物质和Y物质的溶解度均随温度的升高而增大 C.将Y物质的饱和溶液从t2℃降到t1℃有晶体析出 D.t2℃时,X、Y两份溶液,所含溶质的质量不可能相等 |
|
| 11. 选择题 | 详细信息 |
下列关于测定空气中氧气含量的实验分析中(图中药品为红磷和水),不正确的是 A.氮气不与红磷反应且难溶于水,是设计该实验的依据之一 B.不能用木炭代替红磷 C.图Ⅰ中进入集气瓶的水约占烧杯中水体积的五分之一 D.图Ⅱ所示装置也可以测定空气中氧气含量 |
|
| 12. 选择题 | 详细信息 |
|
下列关于化学实验操作先后顺序的叙述错误的是 ( ) A.制取少量气体时,先装药品,后检查装置气密性 B.点燃可燃气体时,先检查气体的纯度,后点燃 C.给试管中的药品加热时,先预热试管,后集中加热 D.用托盘天平称量药品时,先调节天平平衡,后称量 |
|
| 13. 选择题 | 详细信息 |
|
下列有关质量守恒定律的说法正确的是 A.镁条的质量等于它燃烧后生成物的质量 B.蜡烛燃烧时逐渐变短,不符合质量守恒定律 C.高锰酸钾受热分解的总质量等于生成物的总质量 D.12g碳和16g氧气反应,可生成28g二氧化碳 |
|
| 14. 选择题 | 详细信息 |
|
据探测卫星发回的数据分析,火星大气中95%是二氧化碳,其余为少量的氮气.氢气,还找到了有液态水存在的证据。根据以上信息,某同学作出如下推断:①火星大气是混合物②火星大气与地球大气成分相似③火星上钢铁不容易生锈 ④火星环境适宜人类生存⑤火星上温室效应显著。你认为正确的是 A. ①③⑤ B. ②③⑤ C. ②③④ D. ①④⑤ |
|
| 15. 选择题 | 详细信息 |
已知氯酸钾和二氧化锰混合加热可以制取氧气,下图表示一定质量的KClO3和MnO2混合受热过程中,某变量y随时间的变化趋势。纵坐标表示的是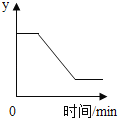 A.固体中氧元素的质量 B.生成O2的质量 C.固体中MnO2的质量 D.固体中钾元素的质量分数 |
|
| 16. 填空题 | 详细信息 |
|
写出下列化学符号: (1)一个氮原子_________________。 (2)两个水分子________________。 (3)三个铝离子________________。 (4)硅元素________________。 (5)硫酸钠________________。 (6)碳酸根离子________________。 |
|
| 17. 填空题 | 详细信息 |
|
化学与生活联系紧密。 (1)食品包装采用充气包装,其中的气体应具有的性质是________(回答一条即可)。 (2)洗涤剂可以去除油污,这是利用了洗涤剂的_____________作用。 (3)日常生活中,可以用________________区分硬水和软水。 (4)俗话说“真金不怕火炼”,说明金具有的性质是________________。 (5)人体中化学元素含量的多少会直接影响人体健康。下列人体所缺元素与引起的健康问题关系错误的是________________。 A 缺铁会引起贫血 B 缺碘会引起龋齿 C 缺钙会引起骨质疏松 D 缺锌会引起食欲不振而导致发育不良 |
|
| 18. 填空题 | 详细信息 |
柴油机尾气中的主要污染物是氮氧化物,某种尾气处理技术是利用氨气与氮氧化物发生化学反应,降低污染物排放,其中一个反应的微观示意图如下所示。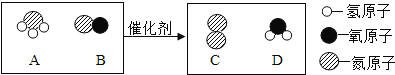 请回答以下问题: (1)根据图示,反应物和生成物一共涉及到____________种化合物。 (2)B中氮元素的化合价为________。 (3)上述反应中,一定发生改变的是______(填序号)。 ①元素种类 ②原子种类 ③分子种类 (4)参加反应的A与B的分子个数比为________。 |
|
| 19. 填空题 | 详细信息 |
|
水是重要的自然资源。 (1)下列净化水的操作中,其中净化程度最高的是________。 A 过滤 B 蒸馏 C 煮沸 D 静置沉淀 (2)某直饮水的主要生产流程为:自来水→活性炭→超滤膜分离一紫外线消毒→直饮水,其中活性炭起____作用,超滤膜起_______作用。 (3)如图为电解水的装置,试管1中的气体为__,通过该实验得到水的组成结论是__。 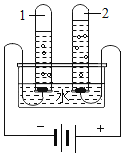 (4)节约用水是每个公民的义务,下列用水方式应该提倡的是________(填字母序号)。 A 用漱口杯接水刷牙 B 不间断地边流水边洗衣 C 用淘米水、洗菜水浇花、冲厕所 D 用喷灌、滴灌的方法浇灌农田 |
|
| 20. 填空题 | 详细信息 |
|
金属在生活生产中有着非常广泛的应用。请回答下列问题: (1)根据下图金属应用实例推断,金属具有的物理性质有__________(至少答两点)。  (2)铝制品表面会形成一层致密的氧化膜,该氧化膜的成分是_____(用化学式表示)。 (3)工业常用赤铁矿和一氧化碳在高温条件下炼铁,该反应的化学方程式为_______。 (4)在古代人们把烧红的生铁放在铁砧上反复捶打最终使生铁转化为钢,这就是“百炼成钢”的来历,这样做的目的是降低生铁中__________元素的含量。 |
|
| 21. 实验探究题 | 详细信息 |
农业生产中常用溶质质量分数为16%的氯化钠溶液来选种。现配制200g溶质质量分数为16%的氯化钠溶液,实验操作如下: (1)实验中正确的操作顺序为______________(填序号)。 (2)实验中需要称量氯化钠的质量为______________。 (3)需要量取水的体积是______________(水的密度为1g/mL)。量取读数时,下图视线角度正确的是______________。(选填字母标号) 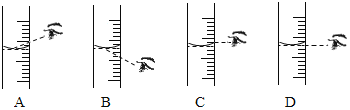 |
|
| 22. 推断题 | 详细信息 |
A~H是初中常见的八种物质,已知A和B、C和H、D和G都是化合物且组成元素相同。D、E、G是气体。八种物质之间有如图转化关系(反应条件已略去)。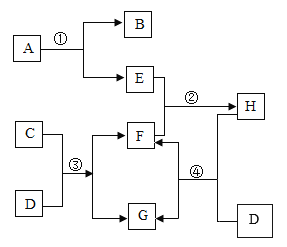 请回答: (1)写出C、F的化学式:C______________,F______________。 (2)反应①的化学方程式为______________。 (3)反应②的基本反应类型为______________。 (4)指出D和G在化学性质上的一点不同之处:______________。 |
|
| 23. 实验探究题 | 详细信息 |
根据下图实验装置,回答下列问题。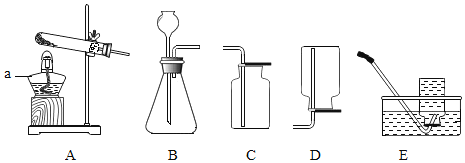 (1)仪器a的名称是________。 (2)实验室制取二氧化碳所选用的发生装置是____(填装置序号,下同),不选择装置E收集二氧化碳的原因是______。 (3)实验室用高锰酸钾制取氧气反应的化学方程式是___,所选用的收集装置是E或__。 (4)主要的实验步骤有:①加热②装药品并固定试管③检查装置的气密性④用排水法收集氧气⑤停止加热⑥将导管从水槽中取出。正确的操作顺序是______。(用序号表示) |
|
| 24. 实验探究题 | 详细信息 |
化学是一门以实验为基础的科学,下面是初中化学中几组重要的对比实验。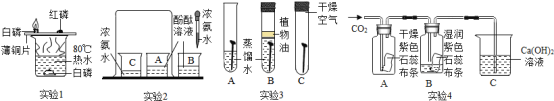 (1)实验1中,双察到铜片上的白磷燃烧而红磷不燃烧,可得出可燃物燃烧的一个条件为_。 (2)实验2中,观察到A烧杯中的现象是_________,由此可验证分子的性质。 (3)实验3中,最易生锈的是______,对比铁钉表面的不同现象,可推知防止铁生锈的原理。生活中使用过的菜刀、铁锅等铁制品,清洗后需要及时擦干放置,可以减少_______对铁锈蚀的影响。 (4)实验4中,整个实验过程中的现象是____,涉及到的化学反应方程式__,___。 |
|
| 25. 科学探究题 | 详细信息 | |||||||||||||||||||||||||||||||||
已知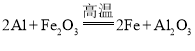 被称为“铝热反应”。镁和氧化铜也能发生类似的反应(条件相同),其化学方程式是__________________。 被称为“铝热反应”。镁和氧化铜也能发生类似的反应(条件相同),其化学方程式是__________________。某小组同学在实验室中进行镁和氧化铜反应的实验,充分反应后对于固体剩余物进行了实验探究。 (提出问题)固体剩余物是什么? (猜想假设)假设①Cu和MgO; 假设②Cu、MgO和Mg; 假设③______________。 (查阅资料一)大多数金属氧化物都能与盐酸反应生成金属氯化物和水(反应中元素化合价不发生改变)。 (实验探究)请完成下列实验。
|
||||||||||||||||||||||||||||||||||
| 26. 计算题 | 详细信息 |
过氧化钙(CaO2)在工农业生产中常用作漂白剂、种子消毒剂及鱼类运输时的制氧剂等。过氧化钙与水反应方程式为: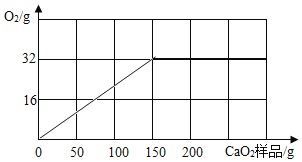 请计算: (1)完全反应后,生成氧气的质量是 。 (2)样品中CaO2的纯度是多少? |
|
最近更新



