河北2018年高二上册化学月考测验带答案与解析
| 1. 选择题 | 详细信息 |
|
下列过程吸收能量的是 A. 镁条燃烧 B. 氨气液化 C. 浓硫酸稀释 D. 冰雪消融 |
|
| 2. 选择题 | 详细信息 |
|
下列有关化学用语正确的是( ) A. 二氧化碳的电子式 B. CaCO3和CH3COOH均为弱电解质 C. 用于考古断代的中子数为8的碳原子表示为 D. 明矾溶液水解可制得Al(OH)3胶体,用于杀菌消毒 |
|
| 3. 选择题 | 详细信息 |
|
某原子最外层电子排布为2s22p3,则该原子 A. 核外有5个电子 B. 核外有3种能量不同的电子 C. 最外层电子占据3个轨道 D. 最外层上有3种运动状态不同的电子 |
|
| 4. 选择题 | 详细信息 |
|
下列基态原子或离子的电子排布式错误的是( ) A. K:1s22s22p63s23p64s1 B. F-:1s22s22p6 C. Fe:1s22s22p63s23p63d54s3 D. Kr:1s22s22p63s23p63d104s24p6 |
|
| 5. 选择题 | 详细信息 |
|
下列各组表述中,正确的是( ) A. 基态核外电子的排布为 B. 第四周期中,未成对电子数最多的原子为Mn C. Fe2+的基态核外电子排布为1s22s22p63s23p63d6 D. 2p能级有2个未成对电子的基态原子的价电子排布一定为2s22p2 |
|
| 6. 选择题 | 详细信息 |
|
下列有关碳原子排布图中,正确的是 A.  B.  C.  D. 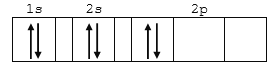 |
|
| 7. 选择题 | 详细信息 |
|
下列各式中,属于正确的电离方程式的是 A. HCO3-+H2O B. HCO3-+OH-=H2O+CO32- C. NH3+H+=NH4+ D. NH3•H2O |
|
| 8. 选择题 | 详细信息 |
|
下列叙述正确的是 A. 泡沫灭火器中用的是苏打和硫酸铝 B. 沸水中滴加适量饱和FeCl3溶液,形成带电的胶体,导电能力增强 C. 理想的催化剂可以大幅度提高目标产物在最终产物的比率 D. Na与H2O的反应是熵减的放热反应,该反应能自发进行 |
|
| 9. 选择题 | 详细信息 | ||||||||||
现有部分短周期元素的性质或原子结构如下表:
|
|||||||||||
| 10. 选择题 | 详细信息 |
|
一定温度下,下列溶液的离子浓度关系式正确的是 A. pH=5的H2S溶液中,c(H+)= c(HS-)=1×10—5mol·L—1 B. pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 C. pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合:c(Na+)+ c(H+)= c(OH-)+c( HC2O4-) D. pH相同的①CH3COO Na②NaHCO3③NaClO三种溶液的c(Na+):①>②>③ |
|
| 11. 选择题 | 详细信息 |
|
在蒸馏水中按物质的量之比为1∶1∶1∶2加入AgNO3,Ba(NO3)2,Na2SO4,NaCl,使之完全溶解,以铂电极电解该混合物至原溶质恰好反应完全,则所得氧化产物与还原产物的质量比为:( ) A. 35.5∶108 B. 71∶2 C. 108∶35.5 D. 71∶109 |
|
| 12. | 详细信息 |
下列图示与对应的叙述相符的是 A. 图I表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 B. 图Ⅱ表示常温下,0.1000mol·L-1 NaOH溶液滴定20.00mL 0.1000mol·L-1 CH3COOH溶液所得到的滴定曲线 C. 图Ⅲ表示一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化曲线,图中a、b、c三点醋酸的电离程度:a<b<c D. 图Ⅳ表示反应4CO(g)+2NO2(g ) |
|
| 13. 选择题 | 详细信息 |
|
能正确表示下列反应的离子方程式的是 A. 用惰性电极电解MgCl2 溶液:2Cl-+2H2O B. 向氯化铝溶液中滴加少量Na2CO3溶液:2Al3++3CO32-=Al2(CO3)3↓ C. 一定量明矾溶液中滴加Ba(OH)2溶液至沉淀的质量最大时:2Ba2++4OH-+Al3++2SO42-=2BaSO4↓+AlO2-+2H2O D. FeCl3溶液与NaAlO2溶液混合:Fe3++ 3AlO2-=Fe(AlO2)3↓ |
|
| 14. 选择题 | 详细信息 |
|
反应NH4HS(s) ①温度、容积不变时,通入SO2气体 ②移走一部分NH4HS固体 ③容积不变,充入氮气 ④充入氮气,保持压强不变 A. ①② B. ①③ C. ①②③ D. ②③ |
|
| 15. 选择题 | 详细信息 |
|
用惰性电极电解AgNO3溶液一段时间后,下列有关说法正确的是( ) A. 阳极质量增加 B. 向溶液中加入适量的Ag2O固体可使溶液恢复电解前的状况 C. 电解过程中溶液的pH不断升高 D. 电解后两极产生的气体体积比为2∶1 |
|
| 16. 选择题 | 详细信息 |
将图1所示的装置中盐桥换成铜导线与两石墨棒连接得到图2所示装置,并将NaCl溶液换为HCl溶液,发现电流表指针仍然有偏转,下列说法正确的是( ) A. 图1盐桥中的阳离子移向甲装置 B. 两图都是将化学能转变成电能的装置 C. 图2中乙装置总反应的离子方程式:Cu2++2Cl- D. 图2中电子流向为Fe→电流计 |
|
| 17. 选择题 | 详细信息 |
右图1为甲烷和O2构成的燃料电池示意图,电解质溶液为KOH溶液,图2为电解AlCl3溶液的装置,电极材料均为石墨。用该装置进行实验,反应开始后观察到x电极附近出现白色沉淀。下列说法正确的是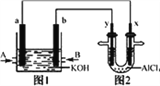 A. 图2中Y电极为阴极 B. 图2中总反应的化学方程式为:2AlCl3+6H2O2 C. 图1中电解质溶液的pH增大 D. 图1中的a 电极反应式为:CH4-8e-+8OH-=CO2+6H2O |
|
| 18. 选择题 | 详细信息 |
|
下列说法正确的是 A. 反应N2(g)+3H2(g)⇌2NH3(g)为放热反应,则△H<0,△S>0 B. 地下钢铁管道用导线连接铜块可以减缓管道的腐蚀 C. 利用太阳能在催化剂参与下分解水制氢是把光能转化为化学能的绿色化学 D. 常温常压下,锌与稀H2SO4反应生成11.2 L H2,反应中转移的电子数为6.02×1023 |
|
| 19. 选择题 | 详细信息 |
如图所示的装置,C、D、E、F、X、Y都是惰性电极,将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色,则以下说法正确的是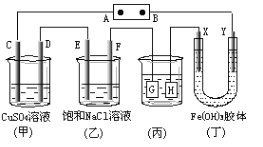 A. 电源B极是正极 B. 装置(丁)中X极附近红褐色变深,说明氢氧化铁胶粒带正电荷 C. 欲用(丙)装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液 D. (甲)、(乙)装置的C、D、E、F电极均有单质生成,其物质的量之比为1 : 2 : 2 : 2 |
|
| 20. 选择题 | 详细信息 |
下列图示与对应的叙述一定正确的是( )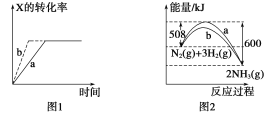  A.图1所示,反应:X(g)+2Y(g) B.图2表明合成氨反应是放热反应,b表示在反应体系中加入了催化剂 C.图3所示,t1 ℃时质量分数均为20%的甲、乙两种溶液,升温到t2 ℃时,两种溶液中溶质的质量分数仍然相等 D.图4所示,用水稀释pH相同的盐酸和醋酸,Ⅰ表示醋酸,Ⅱ表示盐酸,且溶液导电性:c>b>a |
|
| 21. 选择题 | 详细信息 |
关于下列装置说法正确的是 A. 装置①中,盐桥中的Cl-移向ZnSO4溶液 B. 装置②工作一段时间后,b极附近溶液的pH增大 C. 用装置③精炼铜时,c极为粗铜 D. 装置④中电子由Zn流向Fe,装置中有Fe2+生成 |
|
| 22. 选择题 | 详细信息 |
|
下列能用勒夏特列原理解释的是( ) A. 铁在潮湿的空气中易腐蚀 B. H2、I2、HI平衡混和气加压后颜色变深 C. 往往需要在催化剂条件下SO2氧化成SO3 D. 棕红色NO2加压后颜色先变深后变浅 |
|
| 23. 选择题 | 详细信息 |
|
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是 A. 氢氧燃料电池在碱性介质中的负极反应式:O2+2H2O+4e一=4OH- B. 电解饱和食盐水时,阳极的电极反应式为:2C1-一2e一=C12↑ C. 粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu一2e-=Cu2+ D. 钢铁发生电化学腐蚀的正极反应式:Fe一2e—=Fe2+ |
|
| 24. 选择题 | 详细信息 |
|
下列有关说法正确的是 A. 反应NH3(g)+HCl(g)= NH4Cl(s)在室温下可自发进行,则该反应的ΔH<0 B. 稀氨水中加入氢氧化化钠固体少量,由于氨水的电离平衡逆向移动,所以溶液的碱性减弱 C. 25℃下,在NH3·H2O稀溶液中加水稀释, D. 电化学降解NO2的原理如图所示,若电解过程中转移2mol电子,则交换膜两侧电解液的质量变化差△m左-△m右=10.4g 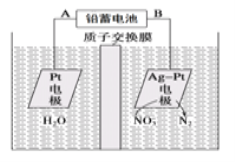 |
|
| 25. 选择题 | 详细信息 |
已知:2H2S(g)+O2(g)=S2(s)+2H2O(1) ΔH =-632 kJ·mol-1。下图为H2S燃料电池的示意图。下列说法正确的是 A. 电极a为电池的负极 B. 电极b上发生的电极反应为:O2+2H2O+4e-=4OH- C. 每有10mol氧气参加反应,电池内部吸收632 kJ热能 D. 每34gH2S参与反应,电路中有2mol电子通过 |
|
| 26. 填空题 | 详细信息 | ||||||
现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大.
|
|||||||
| 27. 填空题 | 详细信息 |
|
工业燃烧煤、石油等化石燃料释放出大量氮氧化物(NOx)、CO2、CO、SO2等气体,严重污染空气。对废气进行脱硝、脱碳和脱硫处理可实现绿色环保、废物利用。 Ⅰ.脱硝: 已知:H2的燃烧热为285.8kJ/mol N2(g)+2O2(g)=2NO2(g)△H=+133kJ/mol H2O(g)=H2O(l)△H=-44kJ/mol (1)催化剂存在下,H2还原NO2生成水蒸气和其它无毒物质的热化学方程式为__________________________。 Ⅱ.脱碳: (2)向2L密闭容器中加入2molCO2、6molH2,在适当的催化剂作用下,发生反应:CO2(g)+3H2(g) 下列叙述能说明此反应达到平衡状态的是__________。 A.混合气体的平均式量保持不变 B.CO2和H2的体积分数保持不变; C.CO2和H2的转化率相等 D.混合气体的密度保持不变 E.1molCO2生成的同时有3molH—H键断裂 (3)在T1℃时,体积为2L的恒容容器中充入物质的量之和为3mol的H2和CO,发生反应CO(g)+2H2(g) 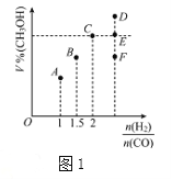  ①当起始n(H2)/n(CO)=2,经过5min达到平衡,CO的转化率为0.4,则0~5min内平均反应速率V(H2)=__________。若此时再向容器中加入CO(g)和CH3OH(g)各0.4mol,达新平衡时H2的转化率将__________(选填“增大”、“减小”或“不变”); ②当起始n(H2)/n(CO)=3.5时,达到平衡状态后,CH3OH的体积分数可能是图1中的___________点(选填“D”、“E”或“F”) Ⅲ.脱硫: 如图2所示。 |
|
| 28. 填空题 | 详细信息 |
Ⅰ.按如图所示装置进行实验,并回答下列问题: (1)甲池,通入CH3OH(甲醇)的电极反应式为______________________。 (2)乙池中的总反应化学方程式为______________________。 (3)当甲池中消耗O20.56L(标准状况下)时,理论上乙池中B极的质量增加__________g;此时丙装置中___________(填“c”或“d”)电极折出1.20g金属,则按丙装置中的的某盐溶液可能是__________________(填序号)。 a.MgSO4溶液 b.CuSO4溶液 c.NaCl溶液 d.AgNO3溶液 Ⅱ.SO2、CO、CO2、NOx是对环境影响较大的几种气体,对它们的合理控利和治理是优化我们生存环境的有效途径。 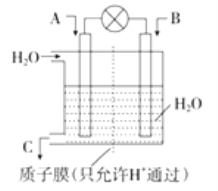 (4)利用化学原理将C0、SO2转化为重要化工原料,装置如图所示: ①若A为CO,B为H2,C为CH3OH,则通入CO一极为____________________极。 ②若A为SO2,B为O2,C为H2SO4,则负极的电极反应式为____________________。 ③若A为NO2,B为O2,C为HNO3,则正极的电极反应式为____________________。 |
|
| 29. 实验题 | 详细信息 |
|
我国规定:室内甲醛含量不得超过0.08mg·m-3。某研究性学习小组欲利酸性KMnO4溶液测定空气中甲醛的含量, (部分装置如图),其反应原理及步骤如下: 4MnO4-+5HCHO+H +=Mn2++5CO2↑+11H2O 2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O 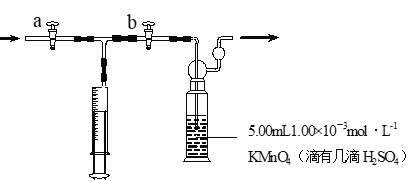 步骤:①量取5.00mL 1.00×10-3mol·L-1 KMnO4,溶液于洗气瓶中,并滴入几滴稀H2SO4,加水20mL稀释备用。 ②取1.00×10-3mol·L-1草酸标准溶液于酸式滴定管中备用。 ③用注射器抽取100mL新装修室内空气。再将注射器气体推入洗气瓶中充分反应。再重复4次。 ④将洗气瓶中溶液转移到锥形瓶中(包括洗涤液),再用标准草酸溶液进行滴定,记录滴定所消耗的草酸溶液的体积。 ⑤再重复实验2次(每次取高锰酸钾溶液5.00mL)。3次实验消耗草酸溶液的体积平均值为12.38mL。 回答下列问题 (1)此实验用指示剂____________(填字母)。A 甲基橙 b酚酞 c淀粉 d无需另外添加试剂 (2)量取5.00mL KMnO4溶液应用______________滴定管 (3)下列操作能引起室内甲醛浓度偏高的是________。 a.滴定终点俯视读数 b.滴定前有气泡滴定后无气泡 c.在高锰酸钾溶液中加入少量水 d.装草酸的滴定管未润洗 (4)草酸是二元中强酸,草酸氢钠溶液显酸性。常温下,如果向10 mL 0.01 mol•L-1 H2C2O4溶液中滴加0.0 1 mol•L-1 NaOH溶液 ①当加入的NaOH溶液体积为10 mL,请你写出溶液中质子守恒关系式__________。 ②当加入的NaOH溶液体积为20 mL,请你写出溶液中离子的浓度大小关系__________。 |
|
高中化学 试卷推荐
最近更新




