马关县二中高三化学2019年上册开学考试附答案与解析
| 1. 选择题 | 详细信息 |
|
下列叙述正确的是 A. 24 g 镁与27 g铝中,含有相同的质子数 B. 同等质量的氧气和臭氧中,电子数相同 C. 1 mol重水与1 mol水中,中子数比为2∶1 D. 1 mol乙烷和1 mol乙烯中,化学键数相同 |
|
| 2. 选择题 | 详细信息 |
|
物质的量相同的N2、O2、CO2混合后,通过Na2O2颗粒一段时间,测得体积变为原混合气体体积的8/9(同温同压下),此时N2、O2、CO2的物质的量之比为 A. 1∶1∶0 B. 6∶9∶0 C. 3∶4∶1 D. 3∶3∶2 |
|
| 3. 选择题 | 详细信息 |
|
化学与生活密切相关。下列说法错误的是 A. 碳酸钠可用于去除餐具的油污 B. 漂白粉可用于生活用水的消毒 C. 氢氧化铝可用于中和过多胃酸 D. 碳酸钡可用于胃肠X射线造影检查 |
|
| 4. 选择题 | 详细信息 |
我国科学家研发了一种室温下“可呼吸”的Na—CO2二次电池。将NaClO4溶于有机溶剂作为电解液,钠和负载碳纳米管的镍网分别作为电极材料,电池的总反应为:3CO2+4Na A. 放电时,ClO4-向负极移动 B. 充电时释放CO2,放电时吸收CO2 C. 放电时,正极反应为:3CO2+4e− =2CO32-+C D. 充电时,正极反应为:Na++e−=Na |
|
| 5. 选择题 | 详细信息 |
|
下列有关电解质溶液的说法正确的是 A. 向0.1mol/LCH3COOH溶液中加入少量水,溶液中c(H+)/c(CH3COOH)减小 B. 将CH3COONa溶液从20℃升温至30℃,溶液中c(CH3COO-)/c(CH3COOH)·c(OH-)增大 C. 向盐酸中加入氨水至中性,溶液中c(NH4+)/c(Cl-)>1 D. 向AgCl、AgBr的饱和溶液中加入少量硝酸银,溶液中c(Cl-)/c(Br-)不变 |
|
| 6. 选择题 | 详细信息 |
|
化学与生活密切相关。下列说法错误的是 A. PM2.5是指粒径不大于2.5μm的可吸入悬浮颗粒物 B. 绿色化学要求从源头上消除或减少生产活动对环境的污染 C. 燃煤中加入CaO可以减少酸雨的形成及温室气体的排放 D. 天然气和液化石油气是我国目前推广使用的清洁燃料 |
|
| 7. 选择题 | 详细信息 |
|
在一定温度下,向足量的饱和Na2CO3溶液中加入1.06 g无水Na2CO3,搅拌后静置,最终析出晶体的质量( ) A.等于1.06 g B.大于1.06 g而小于2.86 g C.等于2.86 g D.大于2.86 g |
|
| 8. 实验题 | 详细信息 |
|
K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。回答下列问题: (1)晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,以K3[Fe(CN)6]溶液为显色剂。其光解反应的化学方程式为:2K3[Fe(C2O4)3] (2)某小组为探究三草酸合铁酸钾的热分解产物,按下图所示装置进行实验。  ①通入氮气的目的是________________________________________。 ②实验中观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色,由此判断热分解产物中一定含有___________、___________。 ③为防止倒吸,停止实验时应进行的操作是_____________________________。 ④样品完全分解后,装置A中的残留物含有FeO和Fe2O3,检验Fe2O3存在的方法是:________________。 (3)测定三草酸合铁酸钾中铁的含量。 ①称量m g样品于锥形瓶中,溶解后加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点。滴定终点的现象是___________________________。 ②向上述溶液中加入过量锌粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中。加稀H2SO4酸化,用c mol·L-1 KMnO4溶液滴定至终点,消耗KMnO4溶液V mL。该晶体中铁的质量分数的表达式为________________________________。 |
|
| 9. 综合题 | 详细信息 |
|
钢铁工业是国家工业的基础,钢铁生锈现象却随处可见,为此每年国家损失大量资金。请回答钢铁腐蚀与防护过程中的有关问题。 (1)钢铁的电化学腐蚀原理如图所示:  ①写出石墨电极的电极反应式______; ②将该装置作简单修改即可成为钢铁电化学防护的装置,请在如图虚线框内所示位置作出修改,并用箭头标出导线中电子流动方向。______ ③写出修改后石墨电极的电极反应式______。 (2)生产中可用盐酸来除铁锈。现将一生锈的铁片放入盐酸中,当铁锈被除尽后,溶液中发生的化合反应的化学方程式_____。 (3)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图:  ①A电极对应的金属是__(写元素名称),B电极的电极反应式是____。 ②若电镀前铁、铜两片金属质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12g,则电镀时电路中通过的电子为___ mol。 ③镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因___。 |
|
| 10. 实验题 | 详细信息 | ||||
|
某研究小组为探究SO2和Fe(NO3)3溶液的反应的实质。设计了如下图所示装置进行实验. 已知:1.0 mol/L的Fe(NO3)3溶液的pH=1。  请回答: (1)装置A中用于添加浓硫酸的仪器名称为__________________。 (2)实验前鼓入N2的目的是________________________________。 (3)装置B中产生了白色沉淀,其成分是________,说明SO2具有________性。 (4)分析B中产生白色沉淀的原因。 观点1:SO2与Fe3+反应; 观点2:在酸性条件下SO2与NO3-反应; ①若观点1正确,除产生沉淀外,还应观察到的现象是_________________。 ②按观点2,装置B中反应的离子方程式是______________________________, ③有人认为,如将装置B中的Fe(NO3)3溶液替换为等体积的下列溶液,在相同条件下进行实验,也可验证观点2是否正确。此时应选择的最佳试剂是(填序号)_____。
|
|||||
| 11. 推断题 | 详细信息 |
|
(题文)[化学——选修5:有机化学基础] 近来有报道,碘代化合物E与化合物H在Cr-Ni催化下可以发生偶联反应,合成一种多官能团的化合物Y,其合成路线如下: 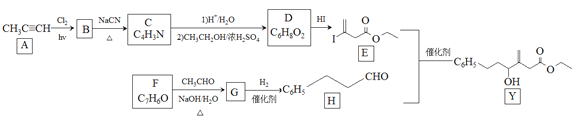 已知: 回答下列问题: (1)A的化学名称是________________。 (2)B为单氯代烃,由B生成C的化学方程式为________________。 (3)由A生成B、G生成H的反应类型分别是________________、________________。 (4)D的结构简式为________________。 (5)Y中含氧官能团的名称为________________。 (6)E与F在Cr-Ni催化下也可以发生偶联反应,产物的结构简式为________________。 (7)X与D互为同分异构体,且具有完全相同官能团。X的核磁共振氢谱显示三种不同化学环境的氢,其峰面积之比为3∶3∶2。写出3种符合上述条件的X的结构简式________________。 |
|
| 12. 填空题 | 详细信息 |
|
[化学——选修3:物质结构与性质] 锌在工业中有重要作用,也是人体必需的微量元素。回答下列问题: (1)Zn原子核外电子排布式为________________。 (2)黄铜是人类最早使用的合金之一,主要由Zn和Cu组成。第一电离能Ⅰ1(Zn)_______Ⅰ1(Cu)(填“大于”或“小于”)。原因是________________。 (3)ZnF2具有较高的熔点(872 ℃),其化学键类型是_________;ZnF2不溶于有机溶剂而ZnCl2、ZnBr2、ZnI2能够溶于乙醇、乙醚等有机溶剂,原因是________________。 (4)《中华本草》等中医典籍中,记载了炉甘石(ZnCO3)入药,可用于治疗皮肤炎症或表面创伤。ZnCO3中,阴离子空间构型为________________,C原子的杂化形式为________________。 (5)金属Zn晶体中的原子堆积方式如图所示,这种堆积方式称为_______________。六棱柱底边边长为a cm,高为c cm,阿伏加德罗常数的值为NA,Zn的密度为________________g·cm-3(列出计算式)。  |
|
最近更新



