内蒙古2018年高二化学上半期期中考试带参考答案与解析
| 1. 选择题 | 详细信息 |
|
下列说法不正确的是 A. 增加反应物的物质的量,反应速率不一定能加快 B. 可逆反应A(g) C. 对达到平衡的一个放热的可逆反应,若降低温度正反应速率减小,逆反应速率增大 D. 参加反应物质的性质是决定化学反应速率的主要因素 |
|
| 2. 选择题 | 详细信息 |
|
利用反应2NO(g)+2CO(g) A.降低温度 B.增大压强同时加催化剂 C.升高温度同时充入N2 D.及时将CO2和N2从反应体系中移走 |
|
| 3. 选择题 | 详细信息 |
|
下列关于化学反应速率的说法正确的是 ①恒温时,增大压强,化学反应速率一定加快 ②其他条件不变,温度越高,化学反应速率越快 ③ 使用催化剂可改变反应速率,从而改变该反应过程中吸收或放出的热量 ④ 3 mol•L﹣1•s﹣1的反应速率一定比1 mol•L﹣1•s﹣1的反应速率大 ⑤升高温度能使化学反应速率增大,主要原因是增大了反应物分子中活化分子的百分数 ⑥有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 ⑦增大反应物浓度,可增大活化分子的百分数,从而使单位时间有效碰撞次数增多 ⑧催化剂反应前后的质量不变,但能降低活化能,增大活化分子的百分数,从而增大反应速率 A. ②⑤⑧ B. ②⑥⑧ C. ②③⑤⑦⑧ D. ①②④⑤⑧ |
|
| 4. 选择题 | 详细信息 |
|
298 K时,各反应的平衡常数如下: ①N2(g)+O2(g) ②2H2(g)+O2(g) ③2CO2(g) 则常温下,NO、H2O、CO2这三个化合物分解放氧的倾向最大的是( ) A.① B.② C.③ D.无法判断 |
|
| 5. 选择题 | 详细信息 |
|
下列说法中,能说明化学平衡一定向正反应方向移动的是( ) A. N2O4(g) B. H2(g)+I2(g) C. N2(g)+3H2(g) D. 2SO2(g) +O2(g) |
|
| 6. 选择题 | 详细信息 |
|
下列事实能用勒夏特列原理解释的是( ) A. 加入催化剂有利于合成氨的反应 B. 由H2(g)、I2(g)和HI(g)组成的平衡体系加压后颜色变深 C. 500 ℃时比室温更有利于合成氨的反应 D. 将混合气体中的氨液化有利于合成氨反应 |
|
| 7. 选择题 | 详细信息 |
|
已知428 ℃时,H2(g)+I2(g) A. 1/49 B. 1/7 C. 492 D. 无法确定 |
|
| 8. 选择题 | 详细信息 |
|
下列关系中能说明可逆反应N2+3H2 A. υ正(N2)=υ逆(NH3) B. υ正(N2)=3υ逆(H2) C. 3υ正(N2)=υ正(H2) D. 2υ正(H2)=3υ逆(NH3) |
|
| 9. 选择题 | 详细信息 |
|
已知:2CO(g)+O2(g)=2CO2(g)ΔH=-566kJ/mol Na2O2(s)+CO2(g)=Na2CO3(s)+ 根据以上热化学方程式判断,下列说法正确的是 A. CO的燃烧热为283 kJ B. 如图可表示由CO生成CO2的反应过程和能量关系 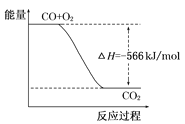 C. 2Na2O2(s)+2CO2(s)=2Na2CO3(s)+O2(g) ΔH>-452 kJ/mol D. CO(g)与Na2O2(s)反应放出509 kJ热量时,电子转移数为6.02×1023 |
|
| 10. 选择题 | 详细信息 |
|
某温度下,浓度都是1 mol·L-1的两种气体X2和Y2,在密闭容器中反应生成气体Z。反应2 min后,测得参加反应的X2为0.6 mol·L-1,用Y2的变化表示的反应速率v(Y2)=0.1 mol·L-1· min-1,生成的c(Z)为0.4 mol·L-1,则该反应的化学方程式是 A. X2+2Y2 C. X2+3Y2 |
|
| 11. 选择题 | 详细信息 |
|
一定温度下,在固定容积的密闭容器中,可逆反应:mA(g)+nB(g) A. ②③④⑥ B. ③⑥⑦ C. ②③⑥ D. ③⑥ |
|
| 12. 选择题 | 详细信息 |
|
一定条件下,向一带活塞的密闭容器中充入1 mol N2和3 mol H2,发生下列反应:N2(g)+3H2(g) A. 保持温度和容器压强不变,充入1 mol NH3(g) B. 保持温度和容器体积不变,充入1 mol NH3(g) C. 保持温度和容器压强不变,充入1 mol N2(g) D. 保持温度和容器体积不变,充入1 mol H2(g) |
|
| 13. 选择题 | 详细信息 |
|
已知:a.C2H2(g)+ H2(g)= C2H4(g)ΔH<0 b. 2CH4(g)= C2H4(g)+ 2H2(g)ΔH>0 判断以下3个热化学方程式: ①C(s)+ 2H2(g)= CH4(g)ΔH1 ②C(s)+ ③C(s)+ H2(g)= ΔH1、ΔH2、ΔH3由大到小的顺序是( ) A. ΔH2 >ΔH3 >ΔH1 B. ΔH3 >ΔH2 >ΔH1 C. ΔH3 >ΔH1 >ΔH2 D. ΔH1 >ΔH2 >ΔH3 |
|
| 14. 选择题 | 详细信息 |
右图中的曲线表示在一定条件下,2NO + O2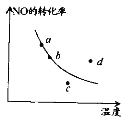 A.a点 B.b点 C.c点 D.d点 |
|
| 15. 选择题 | 详细信息 |
|
已知723K时,2SO2(g)+O2(g) A.Q2= |
|
| 16. 选择题 | 详细信息 |
|
已知①CH3COOH(l)+2O2(g)===2CO2(g)+2H2O(l) ΔH1=-870.3 kJ/mol ②C(s)+O2(g)===CO2(g) ΔH2=-393.5 kJ/mol ③H2(g)+ 则2C(s)+2H2(g)+O2(g)===CH3COOH(l)的反应热为 A. -870.3 kJ/mol B. -571.6 kJ/mol C. +787.0 kJ/mol D. -488.3 kJ/mol |
|
| 17. 选择题 | 详细信息 |
|
一定温度下,在固定容积、体积为2 L的密闭容器中充入1 mol N2和3 mol H2发生反应,当反应进行到10 s末时反应达到平衡,此时容器中c(NH3)=0.1mol·L-1。下列有关判断错误的是 A.反应达平衡时N2的转化率为10% B.反应进行到10 s末时,H2的平均反应速率是0.03 mol·(L·s)-1 C.该反应达到平衡时,N2的平衡浓度为0.45 mol/L D.该反应达到平衡时的压强是起始时压强的0.95倍 |
|
| 18. 选择题 | 详细信息 |
已知某反应aA(g)+bB(g)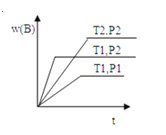 A. T1<T2,P1<P2,a+b>c,Q<0 B. T1>T2,P1<P2,a+b<c,Q>0 C. T1<T2,P1>P2,a+b<c,Q>0 D. T1<T2,P1>P2,a+b>c,Q<0 |
|
| 19. 选择题 | 详细信息 |
在容积可变的密闭容器中存在如下反应:CO(g)+H2O(g)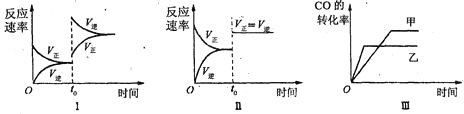 下列分析中正确的是 A、图Ⅱ研究的只是t0时使用催化剂对反应速率的影响 B、图Ⅰ研究的是t0时缩小容器体积对反应速率的影响 C、图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高 D、图Ⅲ研究的是催化剂对化学平衡的影响,且甲使用了催化剂 |
|
| 20. 选择题 | 详细信息 |
在一定条件下,向一带活塞的密闭容器中充入2molA和1molB,发生下列反应:2A(g)+B(g)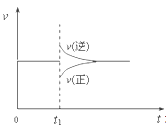 A、保持压强不变,升高反应温度 B、保持温度不变,增大容器体积 C、保持温度和容器体积不变,充入1molC(g) D、保持温度和压强不变,充入1molC(g) |
|
| 21. 选择题 | 详细信息 |
|
在密闭容器发生下列反应:aA(g) A. 平衡向正反应方向移动 B. a<c+d C. D的体积分数增大 D. A的转化率变大 |
|
| 22. 选择题 | 详细信息 |
右图是温度和压强对X+Y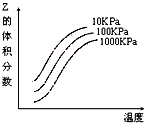 A. 上述可逆反应的正反应为放热反应 B. X、Y、Z均为气态 C. X和Y中只有一种是气态,Z为气态 D. 上述反应的逆反应的△H>0 |
|
| 23. 选择题 | 详细信息 |
|
在温度相同、容积均为2 L的3个恒容密闭容器中,按不同方式投入反应物,保持恒温,测得反应达到平衡时的有关数据如下。下列说法正确的是( ) 已知N2(g)+3H2(g)  A. 2p1=2p3<p2 B. 达到平衡时丙容器中NH3的体积分数最大 C. α2+α3<1 D. Q1+Q3=92.4 |
|
| 24. 实验题 | 详细信息 |
|
某化学兴趣小组要完成中和热的测定。 (1)实验桌上备有大、小两个烧杯、泡沫塑料、泡沫塑料板、胶头滴管、环形玻璃搅拌棒、0.5 mol•L-1盐酸、0.55 mol•L-1NaOH溶液,实验尚缺少的玻璃用品是__、__。 (2)实验中能否用环形铜丝搅拌棒代替环形玻璃搅拌棒?__(填“能”或“否”),其原因是__。 (3)他们记录的实验数据如下: 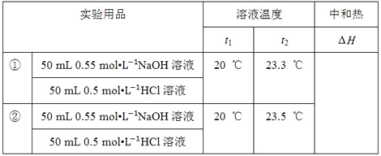 已知:Q=cm(t2﹣t1),反应后溶液的比热容c为4.18 J•℃﹣1•g﹣1,各物质的密度均为1 g•cm﹣3。 ① 计算完成上表ΔH=__(保留2位小数)。 ②根据实验结果写出NaOH溶液与HCl溶液反应的热化学方程式:__。 (4)若用KOH代替NaOH,对测定结果__(填“有”或“无”)影响;若用醋酸代替HCl做实验,对测定结果__(“有”或“无”)填影响。 |
|
| 25. 综合题 | 详细信息 |
|
(1)甲醚(CH3OCH3)是一种无色气体,具有轻微的醚香味,其燃烧热为1455kJ/mol,写出甲醚燃烧的热化学方程式_____;已知H2(g)和C(s)的燃烧热分别是285.8kJ•mol﹣1、393.5kJ•mol﹣1;计算反应4C(s)+6H2(g)+O2(g)═2CH3OCH3(g)的反应热△H=______; (2)用CH4催化还原NOx可以消除氮氧化物的污染。例如: CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1 CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH=-1160 kJ·mol-1 若用标准状况下4.48L CH4还原NO2至N2,整个过程中转移的电子总数为________(阿伏加德罗常数用NA表示),放出的热量为________ kJ。 (3)在25 ℃、101 kPa时,1.00 g C6H6(l)燃烧生成CO2(g)和H2O(l),放出41.8 kJ的热量,则表示C6H6燃烧热的热化学方程式为_______________________________________。 |
|
| 26. 综合题 | 详细信息 |
|
在容积为1.00 L的容器中,通入一定量的N2O4,发生反应N2O4(g) 回答下列问题: (1)反应的ΔH________(填“大于”或“小于”)0;100 ℃时,体系中各物质浓度随时间变化如下图所示。在0~60 s时段,反应速率v(N2O4)为________mol·L-1·s-1。 (2)100 ℃时达平衡后,改变反应温度为T,c(N2O4)以0.002 0 mol·L-1·s-1的平均速率降低,经10 s又达到平衡。 a.T________(填“大于”或“小于”)100 ℃,判断理由是________________________________。 b.温度T时反应的平衡常数K2=____________________。 (3)温度T时反应达平衡后,将反应容器的容积减少一半,平衡向________(填“正反应”或“逆反应”)方向移动,判断理由是________________________________。 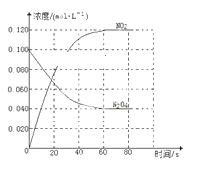 |
|
| 27. 填空题 | 详细信息 |
Ⅰ.二甲醚是一种重要的清洁燃料,可以通过CH3OH分子间脱水制得:2CH3OH(g) 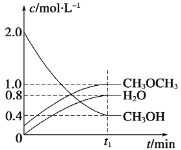 (1)该条件下反应平衡常数表达式K=______________;在t1 ℃时,反应的平衡常数为____________,达到平衡时n(CH3OCH3):n(CH3OH):n(H2O)=_____________________。 (2)相同条件下,若改变起始浓度,某时刻各组分浓度依次为:c(CH3OH)=0.4 mol·L-1、c(H2O)=0.6 mol·L-1、c(CH3OCH3)=2.4mol·L-1,此时正、逆反应速率的大小:v正________v逆(填“>”、“<”或“=”),反应向__________反应方向进行(填“正”或“逆”).。 Ⅱ.已知可逆反应:M(g)+N(g) (1)在某温度下,反应物的起始浓度分别为c(M)=1 mol·L-1,c(N)=2.4 mol·L-1。达到平衡后,M的转化率为60%,此时N的转化率为____________。 (2)若反应温度升高,M的转化率__________(填“增大”、“减小”或“不变”)。 (3)若反应温度不变,反应物的起始浓度分别为c(M)=4 mol·L-1,c(N)=a mol·L-1;达到平衡后,c(P)=2 mol·L-1,a=____________。 |
|
最近更新



