曲靖市高二化学上册期末考试模拟考试训练
| 1. 选择题 | 详细信息 |
|
可逆反应:2SO2+O2 A.1 mol/L B.0.9 mol/L C.0.2 mol/L D.0.1mol/L |
|
| 2. 选择题 | 详细信息 |
已知某可逆反应在密闭容器中进行:A(g)+2B(g)⇌3C(g) ΔH>0,如图中曲线a代表一定条件下该反应的过程,若使a曲线变为b曲线,可采取的措施是( )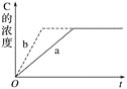 A.恒温恒容条件下将A、B的浓度增加一倍 B.恒温条件下加压(缩小容器体积) C.使用合适的催化剂 D.升高温度 |
|
| 3. 选择题 | 详细信息 |
|
下列有关化学反应速率的说法不正确的是( ) A.化学反应达到最大限度时,正逆反应速率也达到最大且相等 B.催化剂能降低化学反应的活化能,加快反应速率,提高生产效率 C.用锌和稀硫酸反应制取H2时,滴加几滴硫酸铜溶液能加快反应速率 D.用铁片和稀硫酸反应制H2比用98%的浓硫酸产生H2的速率快 |
|
| 4. 选择题 | 详细信息 |
|
等物质的量浓度的下列五种溶液:①CH3COOH ②(NH4)2CO3 ③NaHSO4 ④NaHCO3 ⑤Ba(OH)2,溶液中水的电离程度由大到小排列正确的是( ) A. ⑤③①④② B. ⑤③①②④ C. ②④③①⑤ D. ②④①③⑤ |
|
| 5. 选择题 | 详细信息 |
如图所示甲、乙两个装置,所盛溶液体积和浓度均相同且足量,当电路中通过的电子都是0.1 mol时,下列说法正确的是( )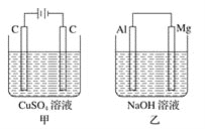 A.溶液的质量变化:甲减小乙增大 B.溶液pH值变化:甲减小乙增大 C.相同条件下产生气体的体积:V甲=V乙 D.电极反应式:甲中阴极:Cu2++2e﹣=Cu,乙中负极:Mg﹣2e﹣=Mg2+ |
|
| 6. 选择题 | 详细信息 |
|
关于浓度均为0.1mol·L-1的三种溶液:①氨水、②盐酸、③氯化铵溶液,下列说法不正确的是( ) A.c(NH4+):③>① B.水电离出的c(H+):②>① C.①和②等体积混合后的溶液:c(H+)=c(OH-)+c(NH3·H2O) D.①和③等体积混合后的溶液:c(NH4+)>c(Cl-)>c(OH->c(H+) |
|
| 7. 选择题 | 详细信息 |
|
在密闭容器中进行可逆反应,A与B反应生成C,其反应速率分别用υ(A)、υ(B)、υ(C)(mol•L﹣1•s﹣1)表示,且υ(A)、υ(B)、υ(C)之间有如下所示的关系:υ(B)=3υ(A); 3υ(C)=2υ(B)。则此反应可表示为( ) A. 2A+3B C. 3A+B |
|
| 8. 选择题 | 详细信息 |
用酸性氢氧燃料电池电解苦卤水(含Cl-、Br-、Na+、Mg2+)的装置如下图所示(a、b为石墨电极).下列说法中,正确的是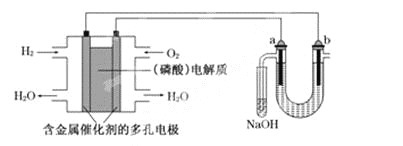 A. 电池工作时,正极反应式为: O2+2H2O+4e-===4OH- B. 电解时,a电极周围首先放电的是Br-而不是Cl-,说明当其他条件相同时前者的还原性强于后者 C. 电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极 D. 忽略能量损耗,当电池中消耗0.02 g H2时,b极周围会产生0.04 g H2 |
|
| 9. 选择题 | 详细信息 |
|
纯水在25 ℃和80 ℃时,c(H+)前后大小关系及酸碱性分别是( ) A. 大于 弱酸性 B. 等于 都显中性 C. 小于 弱酸性 D. 小于 都显中性 |
|
| 10. 选择题 | 详细信息 |
|
在恒容密闭容器中可以作为2NO2(g) ①单位时间内生成n mol O2的同时生成2n mol NO2;②单位时间内生成n mol O2的同时生成2n mol NO;③混合气体的颜色不再改变;④混合气体的密度不再改变的状态;⑤混合气体的平均相对分子质量不再改变的状态;⑥混合气体中NO与O2的物质的量之比保持恒定;⑦混合气体中NO与NO2的物质的量之比保持恒定 A. ①③⑤⑦ B. ②④⑤ C. ①③④ D. ①②③④⑤ |
|
| 11. 选择题 | 详细信息 |
|
下列关于电解池中形成闭合回路的叙述中,正确的是( ) A. 电解池中的闭合回路仅是由电子的定向运动形成的 B. 电子由电源的负极流向电解池的阳极,从电解池的阴极流向电源的正极 C. 在电解质溶液中,阴离子向阴极移动,阳离子向阳极移动 D. 相同时间内阳离子在阴极得到的电子与阴离子在阳极失去的电子数相等 |
|
| 12. 选择题 | 详细信息 |
|
在一固定容积的密闭容器中,充入2 mol A和1 mol B发生如下反应:2A(g)+B(g) A.5 B.4 C.3 D.1 |
|
| 13. 选择题 | 详细信息 |
|
中科院广州化学研究所采用最新的纳米技术,成功地开发出了“CO2制取全降解塑料”的新技术,则下列有关此项技术的说法错误的是( ) A. 是纳米技术应用的重大突破 B. 将有助于缓解“温室效应” C. 该塑料不属于有机合成材料 D. 有助于减少“白色污染” |
|
| 14. 选择题 | 详细信息 |
|
下列说法正确的是( ) A.葡萄糖与果糖、淀粉与纤维素均互为同分异构体 B.油脂在酸的催化作用下可发生水解,工业上利用该反应生产肥皂 C.甲烷、苯、乙酸和乙酸乙酯都可发生取代反应 D.向蛋白质溶液中加入浓的Na2SO4或CuSO4溶液均可使蛋白质盐析而分离提纯 |
|
| 15. 选择题 | 详细信息 |
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物。下列说法正确的是( )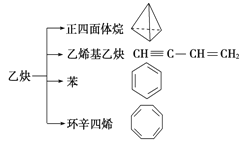 A.正四面体烷的分子式为C4H4,其二氯代物有两种 B.等质量的乙炔与乙烯基乙炔完全燃烧时的耗氧量相同 C.苯为平面六边形结构,分子中存在C—C和C==C,能使酸性KMnO4溶液褪色 D.环辛四烯跟苯的结构很像,不能使溴水褪色 |
|
| 16. 选择题 | 详细信息 |
|
化学与生产、生活密切相关,下列叙述正确的是( ) A. 淀粉、油脂和蛋白质都是天然高分子化合物 B. 葡萄糖注射液不能产生丁达尔效应现象,不属于胶体 C. 14C可用于文物年代的鉴定,14C与12C互为同素异形体 D. 从海水中可以得到NaCl,电解饱和NaCl溶液可以得到金属Na |
|
| 17. 选择题 | 详细信息 |
|
下列物质既能使酸性高锰酸钾溶液褪色,又能使溴水褪色,还能和NaOH反应的是( ) A. 乙酸 B. 乙酸乙酯 C. CH2=CHCOOH D. 苯 |
|
| 18. 选择题 | 详细信息 |
|
下列各组物质相互间一定互为同系物的是( ) A. 淀粉和纤维素 B. 蔗糖和麦芽糖 C. C3H6与C4H8 D. C4H10与C10H22 |
|
| 19. 选择题 | 详细信息 |
|
下列说法正确的是( ) A. 实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取 B. 用乙醇和浓H2SO4制备乙烯时,可用水浴加热控制反应的温度 C. 氯离子存在时,铝表面的氧化膜易被破坏,因此含盐腌制品不宜直接放在铝制容器中 D. 将(NH4)2SO4、CuSO4溶液分别加入蛋白质溶液,都出现沉淀,表明二者均可使蛋白质变性 |
|
| 20. 选择题 | 详细信息 |
|
酒后驾车是引发交通事故的重要原因。交警对驾驶员进行呼气酒精检测的原理是:橙色的K2Cr2O7酸性水溶液遇乙醇迅速生成蓝绿色Cr3+。下列对乙醇的描述与此测定原理有关的是 ①乙醇沸点低 ②乙醇密度比水小 ③乙醇有还原性 ④乙醇是烃的含氧化合物 A. ②④ B. ②③ C. ①③ D. ①④ |
|
| 21. 选择题 | 详细信息 |
有关下图所示化合物的说法不正确的是 A.既可以与Br2的CCl4溶液发生加成反应,又可以在光照下与Br2发生取代反应 B.1mol该化合物最多可以与3mol NaOH反应 C.既可以催化加氢,又可以使酸性KMnO4溶液褪色 D.既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体 |
|
| 22. 选择题 | 详细信息 |
|
下列各组物质中,实验式相同,但既不是同系物,又不是同分异构体的是( ) A. 丙烯和丙烷 B. 正戊烷和2—甲基丁烷 C. 环己烷和苯 D. 乙炔和苯 |
|
| 23. 选择题 | 详细信息 |
|
下列关于苯的叙述正确的是( ) A.苯的分子式为C6H6,它不能使酸性KMnO4溶液褪色,属于饱和烃 B.从苯的凯库勒式( C.在催化剂作用下,苯与液溴反应生成溴苯,发生了加成反应 D.苯分子为平面正六边形结构,6个碳原子之间的价键完全相同 |
|
| 24. 选择题 | 详细信息 |
|
下列说法正确的是( ) A.CF2Cl2有两种同分异构体 B.凡是卤代烃一定能发生消去反应 C.卤代烃在碱性溶液中的水解反应属于取代反应 D.凡能发生消去反应的物质一定是卤代烃 |
|
| 25. 实验题 | 详细信息 | ||||||||||||||||||||||||
|
化学学习小组进行如下实验。 [探究反应速率的影响因素]设计了如下的方案并记录实验结果(忽略溶液混合体积变化)。限选试剂和仪器:0.20 mol·L-1H2C2O4溶液、0.010 mol·L-1KMnO4溶液(酸性)、蒸馏水、试管、量筒、秒表、恒温水浴槽
|
|||||||||||||||||||||||||
| 26. 实验题 | 详细信息 |
亚甲基蓝(Methylnene Blue)在碱性条件下与葡萄糖作用生成亚甲基白(Methylene White),亚甲基蓝的结构简式: 著名的蓝瓶子实验操作步骤如下: ①如图示在250mL锥形瓶中,依次加入2g NaOH、100mL H2O和3g葡萄糖,搅拌溶解后,再加入3滴~5滴0.2%的亚甲基蓝溶液,振荡混合液呈现蓝色; ②塞紧橡皮塞(活塞a、b关闭),将溶液静置,溶液变为无色; ③再打开瓶塞,振荡,溶液又变为蓝色; ④再塞紧橡皮塞,将溶液静置,溶液又变为无色,以上③、④可重复多次。 试回答下列问题: 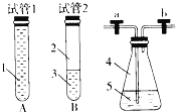 (1)某学生将起初配得的蓝色溶液分装在A,B两支试管中(如上图,A试管充满溶液,B中有少量溶液),塞上橡皮塞静置片刻,两溶液均显无色,若再同时振荡A,B试管,能显蓝色的是_________(填“A”或“B”); (2)若塞紧锥形瓶塞并打开活塞a、b,通入足量氢气后,再关闭活塞a、b并振荡,溶液能否由无色变为蓝色_________(填“能”或“不能”);若塞紧锥形瓶塞并打开a、b通入足量氧气,溶液能否由无色变为蓝色_________(填“能”或“不能”); (3)上述转化过程中,葡萄糖的作用是_________,亚甲基蓝的作用是_________; (4)上述实验中葡萄糖也可用鲜橙汁(其中含丰富维生素C)代替,这是因为维生素C具有_____; (5)该实验中③、④操作能否无限次重复进行_________(填“能”或“不能”),理由是 _____。 |
|
| 27. 实验题 | 详细信息 |
|
为了检验淀粉水解的产物,设计如下实验方案: 请回答下列问题: (1)试剂1为20%的H2SO4溶液,其作用是_________; (2)试剂2为_________NaOH溶液,其作用是_________,使检验水解产物的实验得以顺利进行;发生反应的离子方程式为:_________; (3)反应①的化学方程式为_________; (4)为检验淀粉液是否已完全水解,取少量水解液于试管中,加入碘水,则证明淀粉未完全水解的现象是_________; (5)如果实验过程中没有加入试剂2而直接加入试剂3,能否实现实验目的_________(填”能”或”否”)否,若不能,其原因是_________硫酸能溶解Cu(OH)2而使实验失败,最简单的改正措施是_________。 |
|
| 28. 综合题 | 详细信息 |
实验室制乙酸乙酯得主要装置如图中A所示,主要步骤①在a试管中按2:3:2的体积比配制浓硫酸、乙醇、乙酸的混合物;②按A图连接装置,使产生的蒸气经导管通到b试管所盛的饱和碳酸钠溶液(加入几滴酚酞试液)中;③小火加热a试管中的混合液;④等b试管中收集到约2mL产物时停止加热.撤下b试管并用力振荡,然后静置待其中液体分层;⑤分离出纯净的乙酸乙酯。 请回答下列问题: (1)步骤①中,配制这一比例的混合液的正确操作是__; (2)若实验中用含18O的乙醇与乙酸作用,该反应得化学方程式是:__; (3)步骤③中,要用小火加热,其原因是__; (4)步骤④中可观察到b试管中有细小的气泡冒出,写出该反应的离子方程式:__; (5)A装置中使用球形管除起到冷凝作用外,另一重要作用是__,步骤⑤中分离乙酸乙酯必须使用的一种仪器是__; (6)为充分利用反应物,甲、乙两位同学分别设计了图中甲、乙两个装置(乙同学待反应完毕冷却后,再用饱和碳酸钠溶液提取烧瓶中的产物),你认为合理的是__。 |
|
| 29. 综合题 | 详细信息 |
|
已知:25 ℃时,CH3COOH和NH3·H2O的电离常数相等。 (1)25 ℃时,取10 mL 0.1 mol·L-1醋酸溶液测得其pH=3。 ①将上述(1)溶液加水稀释至1 000 mL,溶液pH数值范围为___________,溶液中c(CH3COO-)/[c(CH3COOH)·c(OH-)]___________(填“增大”“减小”“不变”或“不能确定”)。 ②25 ℃时,0.1 mol·L-1氨水(NH3·H2O溶液)的pH=___________。用pH试纸测定该氨水pH的操作方法为_______________________________________________________。 ③氨水(NH3·H2O溶液)电离平衡常数表达式Kb=_______________________________,25 ℃时,氨水电离平衡常数约为___________。 (2)25 ℃时,现向10 mL 0.1 mol·L-1氨水中滴加相同浓度的CH3COOH溶液,在滴加过程中c(NH4+)/c(NH3.H2O)___________(填序号)。 a.始终减小 b.始终增大 c.先减小再增大 d.先增大后减小 (3)某温度下,向V1mL 0.1 mol·L-1NaOH溶液中逐滴加入等浓度的醋酸溶液,溶液中pOH与pH的变化关系如图。已知:pOH=- lgc(OH-)。 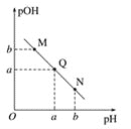 图中M、Q、N三点所示溶液呈中性的点是___________(填字母,下同)。 图中M、Q、N三点所示溶液中水的电离程度最大的点可能是___________。 |
|
| 30. 填空题 | 详细信息 |
|
水煤气(CO 和H2)是合成甲醇的重要原料,它可用水蒸气通过炽热的炭层制得:C(s)+H2O(g) ⑴该反应的平衡常数的表达式为:_________________;升高温度,K值将 ;容器中气体的平均相对分子质量将 。(填“增大”、“减小”或“不变”)。 ⑵上述反应达到平衡后,将体系中的C(s)部分移走,平衡将 (填序号)。 A.向左移 B.向右移 C.不移动 ⑶下列事实能说明该反应在一定条件下已达到平衡状态的有 (填序号)。 A.单位体积内每消耗1molCO的同时生成1molH2 B.混合气体总物质的量保持不变 C.生成H2O(g)的速率与消耗CO的速率相等 D.H2O(g)、CO、H2的浓度相等 ⑷上述反应在t0时刻达到平衡(如图),若在t1时刻改变某一条件,请在图中继续画出t1时刻后c(CO)随时间的变化曲线: ①缩小容器体积(用实线表示)。 ②降低温度(用虚线表示)。  ⑸某温度下,将4.0mol H2O(g)和足量的炭充入2L的密闭容器中,发生如下反应,C(s)+H2O(g) |
|
最近更新