2018-2019年高二上半期12月考试化学免费试卷(云南省大关县一中)
| 1. 选择题 | 详细信息 |
|
N—H键能的含义是( ) A. 由N和H形成1 mol NH3所放出的热量 B. 把1 mol NH3的键全部拆开所吸收的热量 C. 拆开6.02×1023个N—H键所吸收的能量 D. 形成1个N—H键所放出的热量 |
|
| 2. 选择题 | 详细信息 |
|
对配合物[Cu(NH3)4]SO4的叙述,错误的是( ) A. Cu2+和NH3之间以配位键结合 B. [Cu(NH3)4]2+和SO42-之间以离子键结合 C. Cu2+和NH3之间以离子键结合 D. [Cu(NH3)4]SO4在水中全部电离成[Cu(NH3)4]2+和SO42- |
|
| 3. 选择题 | 详细信息 |
|
下列各元素最易形成离子化合物的是( ) ①第三周期第一电离能最小的元素 ②价电子构型为2s22p6的原子 ③2p能级为半满的元素 ④电负性最大的元素 A. ①② B. ③④ C. ②③ D. ①④ |
|
| 4. 选择题 | 详细信息 |
|
下列说法中正确的是( ) A. 含有非极性键的分子一定是非极性分子 B. 非极性分子中一定含有非极性键 C. 由极性键形成的双原子分子一定是极性分子 D. 两个原子之间共用两对电子,形成的化学键一定有极性 |
|
| 5. 选择题 | 详细信息 |
|
X和Y两元素的阳离子具有相同的电子层结构,X元素的阳离子半径大于Y元素的阳离子半径,Z和Y两元素的原子核外电子层数相同,Z元素的原子半径小于Y元素的原子半径.X、Y、Z三种元素原子序数的关系是() A. X>Y>Z B. Y>X>Z C. Z>X>Y D. Z>Y>X |
|
| 6. 选择题 | 详细信息 |
|
某物质的实验式为PtCl4·2NH3,其水溶液不导电,加入AgNO3溶液反应也不产生沉淀,以强碱处理并没有NH3放出,则关于此化合物的说法中正确的是( ) A. 配合物中中心原子的电荷数和配位数均为6 B. 该配合物可能是平面正方形结构 C. Cl- 和NH3分子均与Pt4+配位 D. 配合物中Cl- 与Pt4+配位,而NH3分子不配位 |
|
| 7. 选择题 | 详细信息 |
|
下列物质属于等电子体的一组是( ) A. CH4和NH3 B. B3H6N3和C6H6 C. F-和Mg D. H2O和CH4 |
|
| 8. 选择题 | 详细信息 |
|
已知某元素的+2价离子的电子排布式为1s22s22p63s23p6,则该元素在周期表中的位置正确的是( ) A. 第三周期ⅣA族,p区 B. 第四周期ⅡB族,s区 C. 第四周期Ⅷ族,d区 D. 第四周期ⅡA族,s区 |
|
| 9. 选择题 | 详细信息 |
|
下列说法中正确的是 A. s区都是金属元素 B. s区都是主族元素 C. 稀有气体在ds区 D. 所有非金属元素都在p区 |
|
| 10. 选择题 | 详细信息 |
|
下列物质中含离子键的是( ) A. Cl2 B. CO2 C. NaCl D. CH4 |
|
| 11. 选择题 | 详细信息 |
|
具有下列特征的元素,一定是非金属元素的是( ) A. 对应氢氧化物是两性氢氧化物 B. 具有负化合价 C. 最高价氧化物对应的水化物是酸 D. 具有可变化合价 |
|
| 12. 选择题 | 详细信息 |
|
当H原子和F原子沿z轴结合成HF分子时,F原子中和H原子对称性不一致的轨道是( ) A. 1s B. 2s C. 2px D. 2pz |
|
| 13. 选择题 | 详细信息 |
|
H2O分子中每个O原子结合2个H原子的根本原因是 A.共价键的方向性 B.共价键的饱和性 C.共价键的键角 D.共价键的键长 |
|
| 14. 选择题 | 详细信息 |
根据下列五种元素的电离能数据(单位:kJ·mol-1),判断下列说法不正确的是( )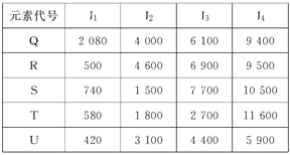 A. 元素的电负性最大的可能是Q元素 B. R和S均可能与U在同一主族 C. U元素可能在周期表的s区 D. 原子的价电子排布为ns2np1的可能是T元素 |
|
| 15. 选择题 | 详细信息 |
关于金属晶体的六方最密堆积的结构形式的叙述正确的是( ) A. 晶胞是六棱柱 B. 晶胞是六面体 C. 每个晶胞中含4个原子 D. 每个晶胞中含17个原子 |
|
| 16. 选择题 | 详细信息 |
|
下列有关晶体和非晶体的说法中正确的是( ) A. 具有规则几何外形的固体均为晶体 B. 晶体具有自范性,非晶体没有自范性 C. 晶体研碎后即变为非晶体 D. 将玻璃加工成规则的固体即变成晶体 |
|
| 17. 选择题 | 详细信息 |
|
镁铝合金因坚硬、轻巧、美观、洁净、易于加工而成为新型建筑装潢材料,主要用于制作窗框、卷帘门、防护栏等,下列与这些用途无关的性质是( ) A. 不易生锈 B. 导电性好 C. 密度小 D. 强度高 |
|
| 18. 选择题 | 详细信息 |
二氧化硅晶体是空间立体网状结构,如图所示: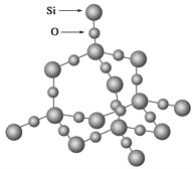 关于二氧化硅晶体的下列说法中,正确的是( ) A. 1 mol SiO2晶体中Si—O键为2 mol B. 二氧化硅晶体的分子式是SiO2 C. 晶体中Si、O原子最外电子层都满足8电子结构 D. 晶体中最小环上的原子数为8 |
|
| 19. 选择题 | 详细信息 |
表中原子化热、晶格能、键能的单位都是kJ•mol﹣1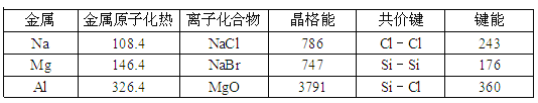 则下列说法正确的是 A. Na(s)与Cl2(g)反应生成1mol NaCl(s)放出的热量为556.1kJ B. Si(s)+2Cl2(g)═SiCl4(g)△H=﹣602kJ•mol﹣1 C. 从表中可以看出,氯化钠的熔点比晶体硅高 D. 从表中数据可以看出,微粒半径越大金属键、离子键越弱,而共价键却越强 |
|
| 20. 选择题 | 详细信息 |
|
石墨烯是由碳原子构成的单层片状结构的新材料(结构示意图如下),可由石墨剥离而成,具有极好的应用前景。下列说法正确的是 A.石墨烯与石墨互为同位素 B.0.12g石墨烯中含有6.02*1022个碳原子 C石墨烯是一种有机物 D.石墨烯中的碳原子间以共价键结合 |
|
| 21. 选择题 | 详细信息 |
|
下列性质体现了金属通性的是( ) A. 银不易生锈 B. 铁常温下不溶于浓硝酸 C. 钠与水剧烈反应放出氢气 D. 金属具有良好的延展性 |
|
| 22. 选择题 | 详细信息 |
|
下列说法正确的是( ) A.原子晶体中只存在非极性共价键 B.稀有气体形成的晶体属于分子晶体 C.干冰升华时,分子内共价键会发生断裂 D.金属元素和非金属元素形成的化合物一定是离子化合物 |
|
| 23. 选择题 | 详细信息 |
已知X、Y、Z三种元素组成的化合物是离子晶体,其晶胞如图所示,则下面表示该化合物的化学式正确的( )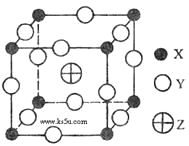 A. ZXY3 B. ZX2Y6 C. ZX4Y8 D. ZX8Y12 |
|
| 24. 选择题 | 详细信息 |
|
能与氢氧化钠溶液反应且属化合物的原子晶体是( ) A. 铝 B. 金刚石 C. 硅 D. 二氧化硅 |
|
| 25. 选择题 | 详细信息 |
高温下,超氧化钾晶体呈立方体结构.晶体中氧的化合价部分为0价,部分为﹣2价.如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元).则下列说法正确的是( )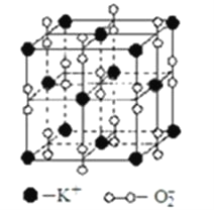 A. 超氧化钾的化学式为KO2,每晶胞含有14个K+和13个O2﹣ B. 晶体中每个K+周围有8个O2﹣,每个O2﹣周围有8个K+ C. 晶体中与每个K+距离最近的K+有8个 D. 晶体中,0价氧原子与﹣2价氧原子的数目比为3:1 |
|
| 26. 选择题 | 详细信息 |
|
关于晶体和非晶体的说法,正确的是( ) A. 晶体在三维空间里呈周期性有序排列,因此在各个不同的方向上具有相同的物理性质 B. 晶体在熔化过程中需要不断的吸热,温度不断地升高 C. 普通玻璃在各个不同的方向上力学、热学、电学、光学性质相同 D. 晶体和非晶体之间不可以相互转化 |
|
| 27. 选择题 | 详细信息 |
高温下,超氧化钾晶体(KO2)呈立方体结构。如图为超氧化钾晶体的一个晶胞(晶体中最小的重复单元)。则下列有关说法正确的是( )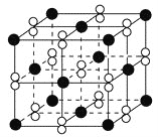 A. KO2中只存在离子键 B. 超氧化钾的化学式为KO2,每个晶胞含有1个K+和1个O2- C. 晶体中与每个K+距离最近的O2-有6个 D. 晶体中,所有原子之间都以离子键相结合 |
|
| 28. 综合题 | 详细信息 |
|
(1)①在BF3分子中,F—B—F的键角是________,B原子的杂化轨道类型为________,BF3和过量NaF作用可生成NaBF4,BF ②在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为________,层间作用力为________。 (2)①Y2X2(C2H2)分子中Y原子轨道的杂化类型为______,1 mol Y2X2含有σ键的数目为______。 ②元素Y(C)的一种氧化物与元素Z(N)的一种氧化物互为等电子体,元素Z的这种氧化物的分子式为________。 ③化合物ZX3(NH3)的沸点比化合物YX4(CH4)的高,其主要原因是______________________。 |
|
| 29. 填空题 | 详细信息 |
二氧化硅晶体是立体的网状结构。其晶体模型如下图所示。请认真观察该晶体模型后回答以下问题: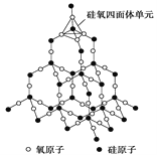 二氧化硅的晶胞结构 (1)二氧化硅晶体中最小环为________元环。 (2)每个硅原子为________个最小环共有。 (3)每个最小环平均拥有________个硅原子、________个氧原子。 |
|
| 30. 综合题 | 详细信息 |
|
X、Y、T、Q 四种元素,位于元素周期表前四周期,元素的性质或结构信息如下. ①X 单质为双原子分子,分子中含有3对共用电子对,常温下单质气体性质稳定,但其原子较活泼; ②Y 二价阳离子的外围电子层排列为3d9; ③T原子核外s轨道电子总数等于p轨道电子总数;人体内含量最多的元素,且其单质是常见的助燃剂; ④Q 第三周期主族元素中原子半径最小。 请根据上述信息回答下列问题: (1)写出 X3﹣的一种等电子体的化学式__; X的气态氢化物易液化的原因是:__. (2)写出T元素基态原子的核外电子排布式__;Q元素的原子核外有__种运动状态不同的电子. (3)元素 X、T 的电负性相比,__的小(填元素名称);元素X的第一电离能与T相比较,T的__(填“大”或“小”). (4)Y元素在周期表中位于__区.Y单质晶体的晶胞中实际拥有__个原子,该晶体中Y原子在三维空间的堆积方式为__堆积.CaO与NaCl的晶胞同为面心立方结构,已知CaO晶体密度为ag•cm﹣3,NA表示阿伏加德罗常数,则CaO晶胞体积为__cm3. (5)在硫酸铜溶液中通入X的气态氢化物至过量,先出现蓝色沉淀,最后溶解形成深蓝色的溶液.此蓝色沉淀溶解的离子方程式为:__. (6)元素X与Q可形成化合物XQ3,根据价层电子对互斥理论判断XQ3的空间构型为:__,分子中X原子的杂化方式为__杂化. |
|
| 31. 综合题 | 详细信息 | ||||||||
|
请按要求填空: (1)Mg是第3周期元素,该周期部分元素氟化物的熔点见下表:
|
|||||||||
| 32. 填空题 | 详细信息 |
|
(1)将等径圆球在二维空间里进行排列,可形成密置层和非密置层,在图1所示的半径相等的圆球的排列中,A属于________层,配位数是________;B属于________层,配位数是________。 (2)将非密置层一层一层地在三维空间里堆积,得到如图2所示的一种金属晶体的晶胞,它被称为简单立方堆积,在这种晶体中,金属原子的配位数是________,平均每个晶胞所占有的原子数目是________。 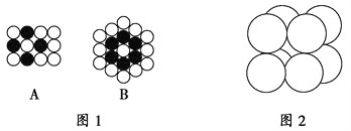 (3)有资料表明,只有钋的晶体中的原子具有如图2所示的堆积方式,钋位于元素周期表的第________周期第__________族,元素符号是________,最外电子层的电子排布式是________。 |
|
| 33. 填空题 | 详细信息 |
|
已知X、Y和Z三种元素的原子序数之和等于42。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子。X跟Y可形成化合物X2Y3,Z元素可以形成负一价离子。请回答下列问题: (1)X元素原子基态时的电子排布式为__________,该元素的符号是__________;  (2)Y元素原子的价层电子的轨道表示式为________,该元素的名称是__________; (2)Y元素原子的价层电子的轨道表示式为________,该元素的名称是__________;(3)X与Z可形成化合物XZ3,该化合物的空间构型为____________; (4)已知化合物X2Y3在稀硫酸溶液中可被金属锌还原为XZ3,产物还有ZnSO4和H2O,该反应的化学方程式是_________________________________________________; (5)比较X的氢化物与同族第二、第三周期元素所形成的氢化物稳定性、沸点高低并说明理由____。 |
|