嘉兴市2019年高三化学上半年高考模拟试卷带解析及答案
| 1. | 详细信息 |
|
下列属于碱性氧化物的是 A. Na2O2 B. SiO2 C. CaO D. CO2 |
|
| 2. | 详细信息 |
|
下列仪器名称为“蒸馏烧瓶”的是 A. 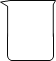 D. D. |
|
| 3. | 详细信息 |
|
下列属于电解质的是 A. 硫酸钡 B. 石墨 C. 医用酒精 D. 氯仿(CHCl3) |
|
| 4. | 详细信息 |
|
下列物质溶于水后溶液显碱性的是 A. SO2 B. NaHCO3 C. NH4NO3 D. KCl |
|
| 5. | 详细信息 |
|
下列说法正确的是 A. 煤的液化是物理变化 B. 天然气为可再生能源 C. 食盐溶于水会显著放热 D. 电解水的反应中含有电能转化为化学能的过程 |
|
| 6. | 详细信息 |
|
下列说法不正确的是 A. 水玻璃可用作建筑黏合剂 B. 硫酸亚铁可用于生产防治缺铁性贫血的药剂 C. 碳酸钠可用于治疗胃酸过多 D. 碘化银可用于人工降雨 |
|
| 7. | 详细信息 |
|
下列反应中有非金属元素被氧化的 A. H2+CuO C. CaO+H2O=Ca(OH)2 D. Mg+2HCl=MgCl2+H2↑ |
|
| 8. | 详细信息 |
|
下列有关化学用语的表示正确的是 A. 苯分子的球棍模型 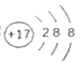 C. 乙炔的结构简式CHCH D. HCl的电子式 |
|
| 9. | 详细信息 |
|
下列说法不正确的是 A. 漂白粉暴露在潮湿的空气中会变质 B. 在常温下,单质硅比较稳定,很难与硫酸发生反应 C. SO2能使溴水褪色,说明SO2具有漂白性 D. 工业上常用高温冶炼黄铜矿的方法获得铜 |
|
| 10. | 详细信息 |
|
下列实验操作不正确的是 A. 保存FeCl2溶液时,常加入少量铁粉 B. 用10mL量筒量取6.4mL的稀盐酸 C. 用溴水除去甲烷中的少量乙烯 D. 用分液漏斗分离苯和汽油的混合物 |
|
| 11. | 详细信息 |
|
下列说法正确的是 A. 乙酸和硬脂酸互为同系物 B.  和 和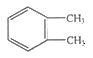 互为同分异构体 互为同分异构体C. H2O和D2O互为同素异形体 D. 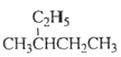 的名称为2—乙基丁烷 的名称为2—乙基丁烷 |
|
| 12. | 详细信息 |
四种短周期元素X、Y、Z、W在周期表中的位置如图所示,其中Z元素的最外层电子数是内层电子总数的1/2。下列说法不正确的是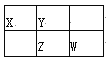 A. Z元素位于周期表的第3周期第VA族 B. X与W形成共价化合物XW2, X的原子半径比Y小 C. Y元素的气态氢化物的热稳定性比Z的高 D. X、W元素的最高价氧化物对应水化物的酸性:W强于X |
|
| 13. | 详细信息 |
|
下列离子方程式书写正确的是 A. 过量CO2通到NaClO溶液中:H2O+CO2+ClO—=HClO+HCO3— B. 用食醋除去水垢的原理:2H++CaCO3=CO2↑+H2O C. 浓盐酸与铁屑反应:2Fe+6H+=2Fe3++3H2O D. FeBr2溶液中通入过量的氯气: 2Fe2 + +2Br—+3Cl2=2Fe3++Br2+6Cl— |
|
| 14. | 详细信息 |
|
一定温度下,0.1mol N2和0.3molH2在恒容的密闭容器中发生如下反应:N2(g)+3H2(g) A. 达到平衡状态时,v正(NH3): v逆(N2)=2 : 1 B. c(N2):c(H2):c(NH3)=1:3:2时,说明反应已达到平衡状态 C. 容器内的压强不再变化时,说明反应已达到平衡状态 D. 升高温度时,v正(NH3)增大,v逆(NH3)增大 |
|
| 15. | 详细信息 |
|
下列说法不正确的是 A. 煤焦油中含有苯、二甲苯等物质,可通过分馏进一步分离 B. 环己烷与溴的四氯化碳溶液在光照条件下褪色,说明发生了取代反应 C. 甲醇含有羟基,也能和金属钠反应产生氢气 D. 含有5个碳原子的烃分子中最多含有4个碳碳单键 |
|
| 16. | 详细信息 |
|
下列说法不正确的是 A. 检验淀粉是否水解完全的方法是:在水解液中先加入过量的氢氧化钠溶液,然后滴加碘水, 未变蓝,说明已水解完全 B. 检验皂化反应是否完全的方法是:用玻璃棒蘸取反应液滴到盛有热水的烧杯中,振荡,观察是否有油滴浮在水面上 C. 利用蛋白质盐析的性质,可进行分离提纯 D. 氨基酸分子中含有氨基(-NH2)、羧基(-COOH),所以既能和酸反应又能和碱反应 |
|
| 17. | 详细信息 |
一种新型的电池,总反应为: 3Zn+2FeO42-+8H2O=2Fe(OH)3↓+3Zn(OH)2↓+4OH—,其工作原理如图所示。下列说法不正确的是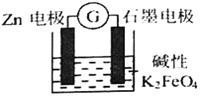 A. Zn极是负极,发生氧化反应 B. 随着反应的进行,溶液的pH增大 C. 电子由Zn极流出到石墨电极,再经过溶液回到Zn极,形成回路 D. 石墨电极上发生的反应为:FeO42—+3e—+4H2O=Fe(OH)3↓+5OH— |
|
| 18. | 详细信息 |
|
下列说法不正确的是 A. MCl2在水溶液中的电离方程式为:MCl2=M2++2Cl—,则M(OH)2可能是弱电解质 B. 足量的锌分别与等体积的盐酸(pH=1)和醋酸(0.1moL/L)反应,在相同条件下产生的氢气体积相同 C. NaHSO3溶液显酸性的原因是HSO3—的电离强于水解 D. pH相同的氨水和氢氧化钠加水稀释相同倍数后,c(NH4+)=c(Na+) |
|
| 19. | 详细信息 |
|
下列说法正确的是 A. 干冰和石英晶体中的化学键类型相同,熔化时需克服微粒间的作用力类型也相同 B. CO2和CS2每个原子的最外层都具有8电子稳定结构 C. H2O、H2S、H2Se由于分子间作用力依次增大,所以熔沸点依次升高 D. 某晶体固态时不导电,水溶液能导电,说明该晶体是离子晶体 |
|
| 20. | 详细信息 |
|
设NA为阿伏加德罗常数的值,下列说法正确的是 A. 1L0.lmol·L-1的氢氧化钾溶液中O—H键的数目为0.1NA B. 0.5mol·L-1的碳酸钠溶液中CO32-的数目小于0.5NA C. 4.6g金属钠与500mL0.2 mol·L-1稀盐酸充分反应,转移电子数为0.1 NA D. 标准状况下,2.24L乙烯和甲烷混合气体中含有的氢原子数目为0.4 NA |
|
| 21. | 详细信息 |
几种物质的能量关系如下图所示。下列说法正确的是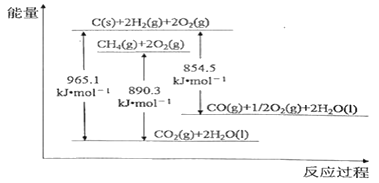 A. C(s)+O2(g)=CO2(g) △H =—965.1 kJ·mol-1 B. 2CO(g)+O2(g)=2CO2(g) △H =-221.2 kJ·mol-1 C. 由图可知,甲烷的燃烧热为779.7 kJ·mol-1 D. 通常由元素最稳定的单质生成生成1mol纯化合物时的反应热称为该化合物的标准生成焓,由图可知,CH4(g)的标准生成焓为+74.8 kJ·mol-1 |
|
| 22. | 详细信息 |
CO(g)和H2O(g)以1 : 2体积比分别通入到体积为2 L的恒容密闭容器中进行反应:CO(g)+H2O(g)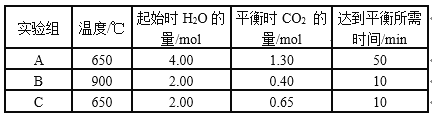 下列说法不正确的是 A. 从实验数据分析,该反应的正反应是吸热反应 B. 实验A中,在0~10min内,以v(H2)表示的反应速率大于0.013mol(L·min)-1 C. 从生产效益分析,C组实验的条件最佳 D. 比较实验B、C,说明C实验使用了更高效的催化剂 |
|
| 23. | 详细信息 |
常温下,用0.01000 mol·L-1的盐酸滴定0.01000 mol·L-1NaA溶液20.00mL。滴定曲线如图所示,下列说法正确的是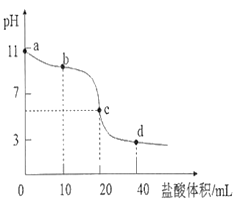 A. a点到d点的过程中,等式c(HA)+c(A—)=0.01000 mol·L—1恒成立 B. b点时,溶液中微粒浓度大小关系为:c(A—)>c(Cl —)>c(HA)>c(OH—)>c(H+) C. c点时,溶液中微粒浓度存在关系:c(Na+)+c(H+) = c(HA)+c(OH—)+2c(A—) D. d点时,溶液中微粒浓度存在关系:c(OH—)+c(A—)=c(H+) |
|
| 24. | 详细信息 |
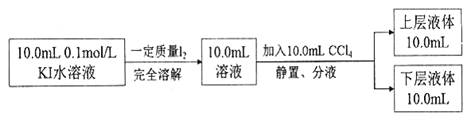
某实验小组用MgBr2稀溶液模拟从海水中制取无水氯化镁和溴单质,实验流程如下,下列说法不正确的是 A. 步骤①中的NaOH溶液,可用Na2CO3、Na2SO3溶液代替 B. 步骤②可用硫酸酸化,发生的离子反应为5Br—+BrO3—+6H+=3Br2+3H2O C. 步骤③包含过滤、洗涤等操作,可用AgNO3溶液检验是否洗涤干净 D. 经步骤③④,溶液1和溶液2的主要成份是相同的,但浓度上有较大差异 |
|
| 25. | 详细信息 |
|
某无色溶液X可能含有:K+、Na+、 NH4+、 Mg2+ 、Ba2+ 、HCO3—、Cl—、SO42—中若干种,且离子浓度相同,为确定其组成,依次进行下列实验。①取少量溶液X,向其中加入足量的氢氧化钠溶液,有白色沉淀A产生;微热,闻到刺激性气味。②过滤上述混合物,在滤液中加入足量的氯化钡溶液,有白色沉淀B产生,再加入足量的稀硝酸,沉淀不溶解。根据上述实验,以下说法正确的是 A. 溶液X —定含有NH4+、Mg2+、SO42—可能含有HCO3— B. 溶液X中一定没有HCO3—,但不能确定是否含有Cl— C. 溶液X中是否含有Na+、K+需要通过焰色反应确定 D. 白色沉淀A和白色沉淀B都是纯净物 |
|
| 26. | 详细信息 |
下图是中学化学中常见的有机物转化关系(部分相关物质和反应条件已略去)。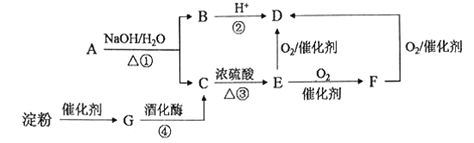 (1)写出E的官能团名称:____________; (2)③的反应类型为 _______________; (3)写出反应①的化学方程式:__________________________________; (4)下列有关上述有机物的说法正确的是____________________。 A.将绿豆大小的钠块投入C中,钠块浮于液面上,并有大量气泡产生 B.可用新制Cu(OH)2鉴别C、D、F三种无色液体(实验过程可加热) C.G能够发生酯化、水解、氧化、加成等反应 D.相同物质的量的C、E充分燃烧时消耗等量的氧气 |
|
| 27. | 详细信息 |
某兴趣小组为探究难溶性盐X(仅含三种元素)的组成和性质,设计并完成如下实验: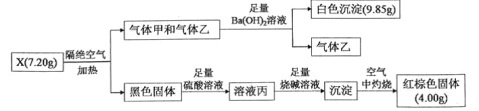 已知:气体甲和气体乙组成元素相同,物质的量之比为1:1。请回答: (1)X的化学式为___________。 (2)溶液丙与H2O2溶液在酸性条件下反应的离子方程式是___________________________。 (3)写出利用流程图中某种物质将红棕色固体重新转化为黑色固体的化学方程式:____________。 |
|
| 28. | 详细信息 |
纯净的氮化镁(Mg3N2)是淡黄色固体,热稳定性较好,遇水极易发生反应。某同学初步设计了如下实验装置制备氮化镁(夹持及加热仪器没有画出)。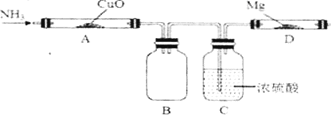 己知:Mg + 2NH3→Mg(NH2)2+H2。请回答: (1)A中观察到的实验现象是_____________,装置C的作用除了干燥以外还有________________; (2)下列说法不正确的是 __________ A.为了得到纯净的氮化镁,实验前需要排除装置中的空气 B.装B起到了缓冲安全的作用 C.将装罝B、C简化成装有碱石灰的U型管,也能达到实验目的 D.实验后,取D中固体加少量水,能生成使湿润的蓝色石蕊试纸变红的气体 |
|
| 29. | 详细信息 |
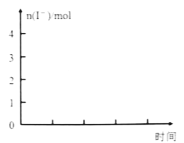
标准状况下,往一定量的NaOH固体中,逐滴加入1.00 mol·L−1NH4HSO4溶液充分反应,反应产生的NH3随NH4HSO4溶液体积的变化如图所示(假设生成的NH3全部逸出),请计算: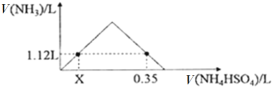 (1)X的值为______________。 (2)NaOH的物质的量为______________。 |
|
| 30. | 详细信息 | |||||||||
(1)世界水产养殖协会介绍了一种利用电化学原理净化鱼池中水质的方法,其装置如图所示。请写出阴极的电极反应式 _________________________。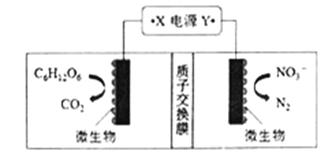 (2)甲醇可利用水煤气合成:CO(g)+2H2(g) 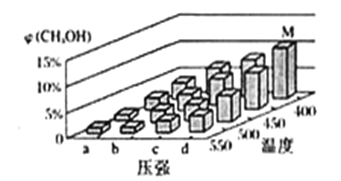 A.状态M,平衡时的CO转化率为10% B.图中压强的大小关系是a<b<c<d C.恒温恒压时,在原平衡体系中再充入适量甲醇,重新平衡后体系中甲醇的体积分数不变 D.当体系中 n(CO)/n(H2)的值不随时间变化时,体系达到平衡 (3)二氧化硫和碘水会发生如下二步反应:
|
||||||||||
| 31. | 详细信息 |
硫酸锌是制备荧光粉的原料之一。某实验室用炼锌厂的烟道灰(主要成分为:炭粉、ZnO、PbO、FeO、SiO2)制备皓矾(ZnSO4· 7H2O)的流程如下: 已知:ZnSO4易溶于水,难溶于乙醇。请回答下列问題: (1)下列操作或描述正确的是 _________ A.“抽滤洗涤”时,将洗液与溶液I合并,有利于提高皓矾的产率 B.溶液I中含量较高的溶质有ZnSO4、PbSO4、FeSO4、H2SO4 C.重结晶时,需加少量稀盐酸抑制Zn2+水解 D. “洗涤干燥”时,可用95%的酒精作为洗涤剂 (2)如图安装抽滤装置,经过一系列操作完成抽滤。请选择合适的编号,按正确的搡作顺序补充完整: 在布氏漏斗中加入滤纸→_____ →_____→_______→________→确认抽干。__________  ①转移固液混合物;②开大水龙头;③关闭水龙头;④微开水龙头;⑤加入少量蒸馏水润湿滤纸 (3)某同学设计了一个实验方案,证明晶体II中的杂质Fe3+含量低于晶体Ⅰ,请把该方案补充完整。_____ (填操作),分别加入2滴稀硝酸和6滴15%KSCN,________(填现象),证明晶体II中的杂质含量低于晶体I (4)某同学称取28.700g研细的皓矾晶体(0.100mol), 置于坩埚中充分加热、冷却、称量,发现晶体失重13.100g。该同学分析认为,在加热失水过程中还发生副反应,该副反应可能的化学方程式为_____________ (5)将烟道灰在氧气中髙温灼烧后,再按上述流程操作,皓矾产率有明显提高,其原因是________ |
|
| 32. | 详细信息 |
米力农是一种用于治疗慢性心衰竭的化合物。某研究小组按下列路线合成米力农.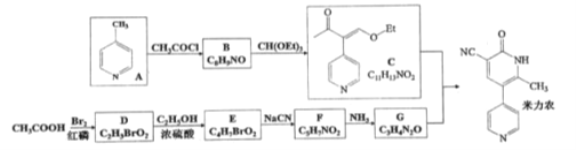 已知: ①化合物B中只含一个甲基。 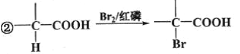 。请回答下列问题: 。请回答下列问题:(1)化合物B的结构简式是 ________________ (2)下列说法不正确的是____________ A.CH(OEt)3的化学式为 C7H16O3 B.C+G → 米力农的反应类型为加成反应 C.上图D→ E→ F的合成路线,避免毒性极强HCN的生成 D.化合物D中滴加AgNO3溶液,会有淡黄色沉淀生成 (3)写出F→ G的化学方程式 _________________________________ (4)化合物A经充分加氢,可得化学式为C6H13N的化合物X,X有多种结构,请写出符合下列条件的X的同分异构体的结构简式__________。 ①含有一个五元环;②1H —NMR谱中只有4种峰。 (5)写出以乙酸为原料制备 |
|
高中化学 试卷推荐
最近更新