2016江苏九年级下学期苏教版初中化学月考试卷
| 1. | 详细信息 |
|
下列做法不利于保护环境的是( ) A.垃圾分类处理 B.使用一次性塑料餐盒 C.使用节水龙头 D.乘坐公共交通工具
|
|
| 2. | 详细信息 |
|
下列属于化学变化的是( ) A.冰雪融化 B.纸张燃烧 C.水分蒸发 D.矿石粉碎
|
|
| 3. | 详细信息 |
|
不含原子团的物质是( ) A.KCl B.NaOH C.NH4Cl D.BaSO4
|
|
| 4. | 详细信息 |
|
下列物品所使用的主要材料为有机合成材料的是( ) A. 塑料玩具 B. 纯棉帽子 C. 陶瓷餐具 D. 黄金饰品
|
|
| 5. | 详细信息 |
|
含氟牙膏中常添加氟化钠,NaF中F元素的化合价是( ) A.+1 B.0 C.﹣1 D.﹣2
|
|
| 6. | 详细信息 |
|
工业冶炼金属锰的原理是3MnO2+4Al A.置换反应 B.化合反应 C.分解反应 D.复分解反应
|
|
| 7. | 详细信息 |
|
下列方法能鉴别空气、氧气和二氧化碳3瓶气体的是( ) A.闻气味 B.将集气瓶倒扣在水中 C.观察颜色 D.将燃着的木条伸入集气瓶中
|
|
| 8. | 详细信息 |
|
地壳中含量最多的金属元素是( ) A.氧 B.硅 C.铝 D.铁
|
|
| 9. | 详细信息 |
|
物质所对应用途错误的是( ) A.氧化钙:作干燥剂 B.氢氧化钠:治疗胃酸过多 C.碳酸氢铵:作氮肥 D.稀盐酸:除铁锈
|
|
| 10. | 详细信息 |
|
如图所示实验操作正确的是( ) A. 稀释浓硫酸 B. 倾倒液体 C. 称量固体 D. 过滤
|
|
| 11. | 详细信息 |
|
工业上常把煤块粉碎后使其充分燃烧,其目的是( ) A.减少煤的浪费 B.减少氧气的消耗 C.减少二氧化碳的排放 D.减少酸雨的形成
|
|
| 12. | 详细信息 |
|
赵洋同学的笔记上有如下对实验现象的记录,你能判断出哪个是正确的吗?( ) A.细铁丝在空气中剧烈燃烧,火星四射,有黑色固体生成 B.亮红色的铜丝加热后表面变黑 C.块状石灰石放入足量稀硫酸溶液中,持续产生气泡 D.红磷在空气中燃烧,发出红色的火焰,产生大量白色烟雾
|
|
| 13. | 详细信息 |
|
施用S﹣诱抗素(C15H20O4)可保证盆栽鲜花按时盛开.关于S诱抗素的说法正确的是( ) A.相对分子质量为264g B.碳元素质量分数小于氢元素质量分数 C.一个分子中含有39个元素 D.S诱抗素中氢氧元素的质量比为5:16
|
|
| 14. | 详细信息 |
|
下列可用于验证铜、铁、锌三种金属的活动性强弱的一组药品是( ) ①Cu、Zn、FeSO4溶液;②Cu、Fe、ZnSO4溶液;③Zn、FeSO4溶液、CuSO4溶液;④Fe、CuSO4溶液、ZnSO4溶液. A.①④ B.①② C.②③ D.③④
|
|
| 15. | 详细信息 |
|
取含铁、氧两种元素的固体样品11.6g,通入足量CO并充分加热,将产生的气体通入足量澄清石灰水,充分反应后,得沉淀20.0g.该固体的组成不可能是( ) A.Fe2O3 B.Fe3O4 C.Fe和Fe2O3 D.FeO和Fe2O3
|
|
| 16. | 详细信息 |
|
下列物质中,含有氧分子的是( ) A.液氧 B.MnO2 C.CO2 D.H2O2
|
|
| 17. | 详细信息 |
|
下列物质长期露置于空气中,因发生化学变化而使溶液质量减少的是( ) A.浓硫酸 B.石灰水 C.浓盐酸 D.氯化钠溶液
|
|
| 18. | 详细信息 | ||||||||||||||||||||
|
除去下列各组物质中的杂质,所用试剂或方法不正确的是( )
A.A B.B C.C D.D
|
|||||||||||||||||||||
| 19. | 详细信息 |
|
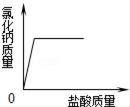
取实验室中部分变质的NaOH样品配成溶液,向其中滴加过量的稀盐酸.下列示意图能正确反映其中变化的( ) A.
|
|
| 20. | 详细信息 |
|
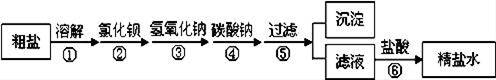
为除去粗盐中含有的硫酸钠、氯化镁、氯化钙等杂质,应加入过量的氯化钡、氢氧化钠、碳酸钠等物质.将杂质转化为沉淀过滤除去,再向滤液中加入适量的盐酸得到精盐水.该工艺示意如图,对该过程的认识中,不正确的是( )
A.操作①中需要进行搅拌,目的是提高氯化钠的溶解度 B.操作③、④两步顺序可以颠倒 C.操作⑤得到的沉淀中有三种成份的物质 D.操作⑥中,加入盐酸的目的是除去过量的氢氧化钠和碳酸钠,将滤液的pH调为7
|
|
| 21. | 详细信息 |
|
煤、和天然气并称为三大化石燃料,煤燃烧会释放出SO2等污染物,这些气体在空气中反应后的生成物溶于雨水,形成酸雨,酸雨对下列物品无损害的是( ) A.大理石塑像 B.铝制门窗 C.玻璃 D.花草树木
|
|
| 22. | 详细信息 |
|
化学用语是学习化学的重要工具 (1)在C、H、O、Ca、Fe、N六种元素中选择适当元素,组成符合下列要求的物质,并将其化学式填入空格中. ①密度最小的气体 ; ②汽水中含有的酸 ;③溶于水温度降低的物质; ④赤铁矿的主要成分 ;⑤相对分子质量最小的氧化物 ;⑥改良酸性土壤的碱 . (2)生活中处处有化学.你知道下列化学原理吗? ①要证明自来水是硬水还是软水,可用 来检验. ②使用久了的水壶内壁会形成水垢,用可厨房中的 浸泡除去. ③白糖与红糖,主要成分都是蔗糖.利用活性炭的 性,可将红糖脱色变成白糖. ④撒盐可以让公路积雪尽快融化,原理是 .
|
|
| 23. | 详细信息 |
|
节假日或双休日,去郊游野炊实为一大快事.然而,在野炊的情趣之中,如果遇到下面一些问题,你是如何处理的? (1)对野炊有经验的人会告诉你,餐具最好是导热性好、不易破碎的材料制的,你准备带的餐具是用 (填字母)制的. A.金属 B.陶瓷 C.无所谓 (2)在“灶”上悬挂野炊锅时,应调节野炊锅到合适的高度.你觉得原因可能是 . A.使用焰心加热 B.使用内焰加热 C.使用外焰加热 (3)野餐食谱如下:主食:馒头;配菜:烤火腿、鲫鱼汤、五香豆干.从营养角度来看,你准备再添一样 (填字母). A.炒鸡蛋 B.牛奶 C.黄瓜 D.烤野兔肉 (4)在引燃细枯枝后,如果迅速往“灶”里塞满枯枝,结果反而燃烧不旺,并产生很多浓烟,说明物质充分燃烧需要的条件是 . (5)若不小心被蚊虫叮咬(蚊虫能分泌出蚁酸),下列物质可用于涂抹以减轻疼痛的是 (填字母) A.食醋(pH<7)B.食盐水(pH=7)C.肥皂水(pH>7) (6)郊外通常比较泥泞,如果你的交通工具是自行车,你回来进行清洗后将链条传动部件涂上油进行防锈,你依据的原理是 .
|
|
| 24. | 详细信息 |
|
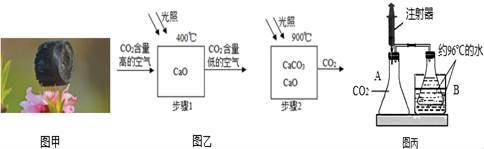
多彩的“碳”,多姿的生活,让我们一起走进“碳”的世界. (1)下列含碳元素的物质中,属于有机物的是 (填字母序号). A.碳酸钙 B.乙醇(C2H5OH)C.二氧化碳 (2)近期,浙江大学实验室里诞生了世界上最轻的材料﹣﹣“碳海绵”.(如图甲所示),由碳元素组成,具有多孔结构,弹性好.它对石油有很强的吸附能力(不吸水),将吸入的石油挤出后仍可恢复原状.下列关于碳海绵的说法正确的是 A (填字母序号). A.具有吸附性 B.可重复利用C.可处理海上石油泄漏 (3)如图乙,二氧化碳是很重要的化工原料,科学家设想利用太阳能加热器“捕捉CO2”、“释放CO2”,实现碳循环.
①步骤1的化学方程式为 . ②为确定步骤2中的碳酸钙是否完全分解,设计的实验步骤为:取少量固体于试管中,滴加过量 溶液,若观察到试管内 .则分解不完全. ③上述设想的优点有 (填字母序号). a.原料易得且可循环利用 b.充分利用太阳能 c.可全地域全天候使用 ④CO2是宝贵的碳氧资源.CO2和H2在一定条件下可合成甲酸(HCOOH),此反应中CO2与H2的分子个数比为 ,若要检验1%甲酸水溶液是否显酸性,能选用的有 (填字母序号). a.无色酚酞溶液 b.紫色石蕊溶液 c.pH试纸 (4)如图丙,在A瓶中盛满CO2气体,将装有96℃以上但未沸腾热水的B瓶,放入装有相同热水的烧杯中,进行如下实验: ①先用注射器抽取20mL的水,注入A瓶中,充分振荡,其化学方程式为 ,但未见B瓶中发生现象. ②再用另一只注射器抽取20mL的浓NaOH,注入A瓶中,充分振荡,观察到的现象为 ,产生此现象的原因是 .
|
|
| 25. | 详细信息 | ||||||||||||||||||
|
如表是KNO3、NaCl在不同温度下的部分溶解度数据,请回答问题:
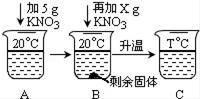
(1)10℃时,KNO3溶解度是 g. (2)40℃时,将70gKNO3固体加入100g水中,充分搅拌,形成的溶液质量为 g. (3)60℃时,KNO3的饱和溶液中含有少量NaCl,通过 方法获得较纯净的KNO3晶体. (4)t℃时,NaCl和KNO3的饱和溶液溶质质量分数相同,该温度范围是 . a.10℃~20℃b.20℃~40℃c.40℃~60℃d.60℃~80℃ (5)向20mL水中溶解一定量KNO3固体的操作如图:请根据实验现象和溶解度数据回答:A、B、C中溶液一定不饱和溶液的是 .当x= g时,B中恰好没有固体剩余.
|
|||||||||||||||||||
| 26. | 详细信息 |
|
汽车尾气的排放也会带来一系列环境问题.“尾气催化转化器”可将汽车尾气中的有毒气体转化为无毒气体.其反应的微观示意图如图:
①写出上述反应中属于氧化物的化学式 ②对上述反应,下列说法中不正确的是 (填序号). A.物质丁的化学式为N2 B.参加反应的乙与生成丁的分子个数比为2:1 C.反应后所得气体对环境有影响 D.若生成56g丁,则参加反应的甲的质量为184g.
|
|
| 27. | 详细信息 |
|
根据如图所示制取气体的装置,回答下列问题(装置选择用序号填写):
(1)实验仪器b的名称是 . (2)用高锰酸钾制取氧气时,反应的化学方程式为 ,所选用的发生装置是 ,若收集干燥的氧气应选用的装置是 ,验满的方法是把带火星的木条放于 处,看是否复燃;若收集纯度高的氧气选用装置是 , (3)用过氧化氢溶液和二氧化锰制取氧气,选 用做发生装置,可以较平稳产生氧气. (4)用大理石和稀盐酸制取二氧化碳时,反应的化学方程式为 .若装置B中反应剧烈,从实验安全角度考虑,不宜采取的措施有 (填序号). ①用容积较小的锥形瓶 ②减慢液体的滴加速度 ③加热反应物 ④降低液体反应物的浓度.
|
|
| 28. | 详细信息 |
|
某品牌纯碱中含有少量氯化钠.某化学探究小组欲测定该品牌纯碱的纯度(即碳酸钠的质量分数). (一)甲组同学设计如图甲所示实验: 【实验步骤】 ①组装好如图甲仪器,并检查 ; ②称取13.0g样品放入锥形瓶中,加入少量蒸馏水溶解,并在其他装置中加入相应的药品; ③称量装置C的质量; ④打开分液漏斗旋塞滴入稀硫酸,直到不再产生气泡为止; ⑤再次称量装置C的总质量; ⑥计算出样品中碳酸钠的质量分数. 【实验分析】 (1)A装置中反应的化学方程式为 . (2)B装置的作用是 . (3)如果没有B装置则所测样品中碳酸钠的质量分数 .(填偏大、偏小、不变) (4)小明提出能否用盐酸代替硫酸?同学们经过讨论认为不能,理由是 . (5)称得纯碱样品的质量为13.0g,实验前、后C装置(包含药品)的质量分别为61.2g和65.6g,则该纯碱样品的纯度为 %(精确到0.1%). (二)乙组同学采用生成沉淀的方法来测定样品中纯碱的质量分数,设计了如图乙实验:
(1)判断加入氯化钡溶液是否过量的合适方法是 ,(填序号)然后观察现象判断. A.静置混合物X,向上层清液中继续滴加氯化钡溶液,若无白色沉淀生成,则氯化钡已经过量; B.向混合物X中滴加稀硫酸,若有白色沉淀生成则说明氯化钡已经过量. (2)判断滤渣是否洗涤干净,可以采取向最后的洗出液中滴加 ,(填序号)然后观察现象判断. A.氯化钡溶液 B.稀硫酸 C.硝酸银溶液 D.稀盐酸 (3)根据实验数据,乙组测得样品中碳酸钠的质量分数为 %(精确到0.1%). 【实验反思】 甲乙两组同学所测该品牌中碳酸钠的质量分数,你认为 组(填“甲”或“乙”)更准确,另一组存在较大偏差的原因可能是 .
|
|
| 29. | 详细信息 |
|
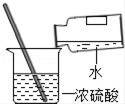
要想把煤燃烧释放出的SO2变废为宝,可把二氧化硫尾气、石灰石、空气、碳酸氢铵、氨气和氯化钾等为原料可以合成有重要应用价值的硫酸钾等物质.合成流程如图所示:
①写出反应Ⅱ的总反应的化学方程式: . ②上述流程中可循环使用的物质是 . ③反应Ⅱ的温度需控制在60~70℃,其理由是 . ④上述流程中的副产物可做 (写出在农业生产中的一种用途)
|
|
















 B
B
 C
C
 D
D