2020河南人教版(2019)高中化学月考试卷
| 1. | 详细信息 |
|
装运乙醇的包装箱应贴的图标是( ) A B C D
|
|
| 2. | 详细信息 |
|
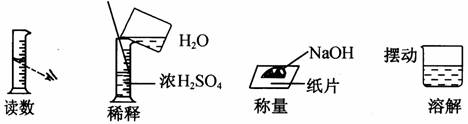
下图四种操作均有错误,其中有两个错误的是( )
A B C D
|
|
| 3. | 详细信息 |
|
现有三组溶液:①汽油和氯化钠溶液;②39%的乙醇溶液;③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是:( ) A. 分液、萃取、蒸馏 B. 萃取、蒸馏、分液 C. 分液、蒸馏、萃取 D. 蒸馏、萃取、分液
|
|
| 4. | 详细信息 |
|
相等物质的量的CO和CO2相比较,下列有关叙述中正确的是( ) ①它们所含的分子数目之比为1:1 ②它们所含的氧原子数目之比为1:2 ③它们所含的原子总数目之比为2:3 ④它们所含的碳原子数目之比为1:1 A. ①和④ B. ②和③ C. ④ D. ①②③④
|
|
| 5. | 详细信息 |
|
标准状况下,有①6.72 L CH4;②3.01×1023个氯化氢分子;③13.6g H2S; ④0.2 mol NH3。下列对这四种气体的关系,描述不正确的是( ) A. 体积:④<①<②<③ B. 密度:①<④<③<② C. 质量:④<①<③<② D. 氢原子数:②<④<③<①
|
|
| 6. | 详细信息 |
|
同温同压下,盛有氧气的A容器与盛有氨气的B容器中所含的原子个数相等,则A与B的体积比是( ) A. 1:1 B. 2:1 C. 1:2 D. 2:3
|
|
| 7. | 详细信息 |
|
100mL 0.3 mol/L Na2SO4溶液和100mL 0.2 mol/L Al2(SO4)3溶液混合后,溶液中 A. 0.2 mol/L B. 0.25 mol/L C. 0.45 mol/L D. 0.50 mol/L
|
|
| 8. | 详细信息 |
|
已知0.5L的NaCl溶液中含有0.5 mol Na+。下列关于该溶液的说法不正确的是( ) A. 该溶液中溶质的物质的量浓度为1 mol·L-1 B. 该溶液中含有58.5 g NaCl C. 配制1000mL 该溶液需用58.5 g NaCl D. 量取100 mL 该溶液倒入烧杯中,烧杯中Na+的物质的量为0.1 mol
|
|
| 9. | 详细信息 |
|
下列关于物质的量的叙述中,正确的是( ) A.1 mol任何物质都含有6.02×1023个分子 B.0.012kg 12C中含有约6.02×1023个碳分子 C.1 mol NH3中含有1 mol 氮和3 mol氢 D.1 mol Ne中含有6.02×1024个电子
|
|
| 10. | 详细信息 |
|
设NA表示阿伏加德罗常数,下列叙述中正确的是( ) A. 常温常压下,11.2 L CO2所含的原子数为1.5 NA B. 常温常压下,48 g O3所含的原子数为3 NA C. 标准状况下,22.4 L H2O所含的分子数为 NA D. 22.4 L H2 所含的原子数为 2 NA
|
|
| 11. | 详细信息 |
|
实验室里需要480 mL0.1 mol·L-1的硫酸铜溶液,以下操作正确的是( ) A. 称取7.68g硫酸铜,加入500mL水 B. 称取12.0g胆矾配成500mL溶液 C. 称取8.0g硫酸铜,加入500mL水 D. 称取12.5g胆矾配成500mL溶液
|
|
| 12. | 详细信息 |
|
用NA代表阿伏加德罗常数,下列说法正确的是( ) A. 0.5 mol Al含有电子数为0.5 NA B. 标准状况下,11.2 L CCl4所含的分子数为0.5 NA C. 0.1 mol CH4含有电子数为1 NA D. 0.2 mol H2O含有氢原子数为0.2NA
|
|
| 13. | 详细信息 |
|
下列叙述中正确的是( ) A. 0.5 mol SO2中共含有9.03×1023个原子 B. 将40 g NaOH 溶于1 L H2O中,所得溶液中溶质的物质的量浓度为1 mol/L C. CO2的摩尔质量为44 g D. 22.4 L任何气体的物质的量均为1 mol
|
|
| 14. | 详细信息 |
|
分别用10 mL 0.1 mol·L-1的BaCl2溶液恰好使相同体积的Fe2(SO4)3、ZnSO4和K2SO4 三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质的量浓度之比是( ) A. 3:2:2 B. 1:2:3 C. 1:3:3 D. 3:1:1
|
|
| 15. | 详细信息 |
|
标准状况下,与32g O2的体积相等的N2,其( ) A.质量为14g B.分子数为6.02╳1023 C.体积为11.2L D.物质的量为2mol
|
|
| 16. | 详细信息 |
|
已知1.505╳1023个x气体分子的质量为8克,则x气体的摩尔质量是( ) A.16g B.32g C.64g/mol D.32g/mol
|
|
| 17. | 详细信息 |
|
(1)等质量的CO和SO2分别装入同温同体积的容器,所含氧原子之比 ,压强之比 。 (2)在标准状况下,由CO和CO2组成的混合气体8.96 L,质量是16g。此混合物中CO和CO2的物质的量之比是 ,混合气体的平均摩尔质量是 。 (3)将标准状况下a L的HCl(g)溶于1000g水,得到的盐酸的密度为bg/cm3,则该盐酸的物质的量浓度为 mol·L-1。 (4)1.204╳1023个NH4+的物质的量为______mol,质量为 g.
|
|
| 18. | 详细信息 |
|
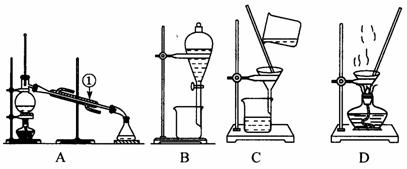
下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题:
(1)从氯化钾溶液中得到氯化钾固体,选择装置 (填代表装置图的字母,下同);除去自来水中的Cl-等杂质,选择装置 ,检验自来水中Cl-是否除尽的方法: ____________________________________________________________。 (2)从碘水中分离出I2,选择装置 ,该分离方法的名称为 。 (3)装置A中①的名称是 ,进水的方向是从 口进水。 装置B在分液时为使液体顺利下滴,应进行的具体操作是 。 (4)海水中蕴藏着丰富的资源,在实验室中取少量海水,进行如下流程的实验:
粗盐中含Ca2+、Mg2+、Fe3+、 的步骤有: ①加入过量的Na2CO3溶液; ②加入过量的BaCl2溶液; ③加入过量的NaOH溶液; ④调节溶液的pH等于7; ⑤溶解; ⑥过滤; ⑦蒸发。 正确的操作顺序是 (填写序号)。 a. ⑤②③①⑥④⑦ b. ⑤①②③⑥④⑦ c.⑤②①③④⑥⑦ d. ⑤③②①⑥④⑦
|
|
| 19. | 详细信息 |
|
某学生需要用烧碱固体配制0.5 mol·L-1的NaOH溶液500 mL。实验室提供以下仪器: ①100mL烧杯 ②100mL量筒 ③1000 mL容量瓶 ④500 mL容量瓶 ⑤玻璃棒 ⑥托盘天平(带砝码)。请回答下列问题: (1)计算:需要称取NaOH固体 g; (2)配制时,必须使用的仪器有 (填代号),还缺少的仪器是 、 。(填仪器名称) (3)配制时,其正确的操作顺序是(字母表示,每个操作只用一次) 。 A. 用少量水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡 B. 在盛有NaOH固体的烧杯中加入适量水溶解 C. 将烧杯中已冷却的溶液沿玻璃棒注入容量瓶中 D. 将容量瓶盖紧,反复上下颠倒,摇匀 E.改用胶头滴管加水,使溶液凹面恰好与刻度相切 F.继续往容量瓶内小心加水,直到液面接近刻度1~2 cm处 (4)实验两次用到玻璃棒,其作用分别是: ; (5)若出现如下情况,其中将引起所配溶液浓度偏高的是 ;(填下列编号) ①容量瓶实验前用蒸馏水洗干净,但未烘干 ②定容观察液面时俯视、 ③配制过程中遗漏了(3)中步骤A ④加蒸馏水时不慎超过了刻度 (6)若实验过程中出现(5)中④这种情况你将如何处理? 。
|
|