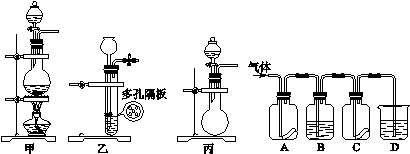2018湖北高一上学期人教版高中化学月考试卷
| 1. | 详细信息 |
|
下列说法正确的是( ) ①正常雨水的pH为7.0,酸雨的pH小于7.0; ②严格执行机动车尾气排放标准有利于防止大气污染; ③使用二氧化硫和某些含硫化合物增白的食品会损害人体健康; ④使用氯气对自来水消毒可能对人体有害; ⑤食品厂产生的含丰富氮、磷营养素的废水可长期排向养鱼水库 A.①②③ B.①④⑤ C.②③④ D.③④⑤
|
|
| 2. | 详细信息 |
|
下列变化中,不能说明SO2是酸性氧化物的是( ) A.二氧化硫与水化合生成亚硫酸 B.二氧化硫与氢氧化钠反应生成亚硫酸钠和水 C.二氧化硫被催化氧化变为三氧化硫 D.二氧化硫与氧化钙化合生成亚硫酸钙
|
|
| 3. | 详细信息 |
|
油井发生火灾,产生的大量废气中含有以下成分(①浓烟中的炭粒、②氮的氧化物、③碳的氧化物、④硫的氧化物、⑤碳氢化合物的蒸气),其中对大气造成污染并导致雨水酸化的有害、有毒气体是( ) A.①③⑤ B.②④ C.②③④ D.②④⑤
|
|
| 4. | 详细信息 |
|
.同温同压下,在3支相同体积的试管中分别充 A.V1>V2>V3
|
|
| 5. | 详细信息 |
|
下列叙述正确的是( ) A.向氯水中通入SO2后溶液的酸性增强 B.向明矾溶液中加入过量NaOH溶液会产生大量白色沉淀 C.Na、Fe等金属在一定条件下与水反应都生成H2和对应的碱 D.在KI-淀粉溶液中通入氯气,溶液变蓝,说明氯气能与淀粉发生显色反应
|
|
| 6. | 详细信息 |
|
下列关于漂白粉的叙述不正确的是( ) A.漂白粉的有效成分是Ca(ClO)2和CaCl2 B.漂白粉在空气中久置后能变质 C.漂白粉是由Cl2与石灰乳制得 D.为了增强漂白粉的漂白效果,使用时可以加少量稀醋酸
|
|
| 7. | 详细信息 |
|
同温同压下,两个等体积的干燥圆底烧瓶中分别充满NH3和NO2, 进行喷泉实验,如图所示,经充分反应后,瓶内溶液的物质的量 浓度为( ) A.①>② B.①<② C.①=② D.不能确定
|
|
| 8. | 详细信息 |
|
下列表述不正确的是( ) A.人造刚玉熔点很高,可用作高级耐火材料,主要成分是Al2O3 B.在医疗上碳酸氢钠可用于治疗胃酸过多 C.用于现代通讯的光导纤维的主要成分是高纯度的硅 D.分散系中分散质粒子的直径:Fe(OH)3 悬浊液>Fe(OH)3 胶体>FeCl3 溶液
|
|
| 9. | 详细信息 |
|
不能鉴别二氧化碳与二氧化硫的试剂是( ) A.品红溶液 B.澄清的石灰水 C.溴水 D.酸性高锰酸钾溶液
|
|
| 10. | 详细信息 |
|
将足量的二氧化锰与40 mL 10 mol/L浓盐酸反应产生的氯气同0.1 mol二氧化锰与足量的浓盐酸反应产生的氯气相比( ) A.前者产生的Cl2多
|
|
| 11. | 详细信息 |
|
某无色透明溶液,在酸性环境下能大量共存的离子组是( ) A.Na+、K+、SiO、Cl- B.Na+、SO、HCO、Cl- C.K+、MnO、NO、Fe2+ D.Mg2+、Cl-、NH、SO
|
|
| 12. | 详细信息 |
|
氯气是一种重要的工业原料。工业上利用反应3Cl2+2NH3===N2+6HCl检查氯气管道是否漏气。下列说法错误的是( ) A.若管道漏气遇氨就会产生白烟 B.该反应利用了Cl2的强氧化性 C.该反应NH3被还原 D.生成1 mol N2有6 mol电子转移
|
|
| 13. | 详细信息 |
|
.能正确表示下列反应的离子方程式的是( ) A.铝粉与NaOH溶液反应:Al + 2OH-===AlO+ H2↑ B.SiO2和NaOH溶液反应:SiO2+ 2OH-===SiO+ H2O C.氯化铵浓溶液跟浓NaOH溶液混合后加热:NH+OH -NH3·H2O D.碳酸氢铵溶液与足量的NaOH溶液混合后加热: NH+OH-NH3↑+H2O
|
|
| 14. | 详细信息 |
|
工业上制金刚砂(SiC)的化学反应为SiO2+3CSiC+ 2CO↑,在这个氧化还原反应中,氧化剂与还原剂的物质 的量之比是( ) A.1∶2 B.2∶1 C.1∶1 D.3∶5
|
|
| 15. | 详细信息 | |||||||||||||||||||||||||
|
拟用右图所示装置制取并收集下表中的四种气体(图中夹 持仪器均已略去;a、b、c表示相应仪器中加入的试剂) 能达到实验目的的是( )
|
||||||||||||||||||||||||||
| 16. | 详细信息 |
|
向BaCl2溶液中通入SO2至饱和,此过程无明显实验现象。再向溶液中加入一种物质,溶液变浑浊。加入的这种物质不可能是( ) A.FeCl3溶液 B.AgNO3溶液 C.稀氨水 D.NH4Cl溶液
|
|
| 17. | 详细信息 |
|
化学就在我们身边,它与我们的日常生活密切相关。按要求回答以下问题: (1)明矾是__________________,漂白粉的有效成分是________(均填化学式)。硅是无机非金属材料的主角,请你举出一种含硅的材料名称__ (2)①用少量氯气消毒的自来水养金鱼时,通常需要先将自来水晒一晒,其原因是________________________________________(用化学方程式表示)。 ②绿柱石(绿宝石)矿藏其主要化学成分为BenAl2Si6O18,可用氧化物形式表示为nBeO·Al2O3·6SiO2,其n值为_______; 北京奥运金牌“金镶玉”环形玉璧由昆仑玉制成,昆仑玉的成分可简单看成是Ca2Mg5Si8O22(OH)2,将其化学式改写成氧化物形式为________________。 ③缺铁性贫血患者应补充Fe2+,通常以硫酸亚铁的形式补充,而硫酸铁无这种药效。当用硫酸亚铁制成药片时外表包有一层特殊的糖衣,这层糖衣的作用是___________________。 (3) SiO2广泛存在于自然界中,其用途也非常广泛,可用于制造光导纤维,也用于生产半导体材料硅。写出工业上用石英制备粗硅的化学反应方程式:_____________________。
|
|
| 18. | 详细信息 |
|
研究工业废弃物的处理和防治具有重要的意义。 (1)利用反应CH4+2NO2N2+CO2+2H2O可消除NO2的污染,该反应中氧化剂是________,当消耗CH4的体积是11.2 L(标准状况下)时,理论上可处理________g NO2。 (2)治理汽车尾气中CO和NO的一种方法是:在汽车排气管中安装一个催化转化装置,该装置能将CO和NO转化为参与大气循环的无毒气体。该反应的化学方程式为___________。 (3)有一 ① 用pH试纸检验,表明溶液呈强酸性 ② 取部分溶液,加入数滴氯水及2 mL CCl4,经振荡后CCl4层呈紫红色; ③ 另取部分溶液,加入NaOH溶液使其变为碱性,无沉淀生成; ④ 取部分上述碱性溶液,加Na2CO3溶液,有白色沉淀生成; ⑤ 将③得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。 根据上述实验事实,可知该溶液中 肯定含有的离子是______________; 肯定没有的离子是________________; 还不能确定是否含有的离子是________________。
|
|
| 19. | 详细信息 |
|
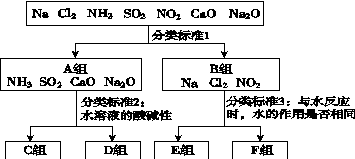
按照一定标准,根据物质与水反应的不同情况,对下列物质进行分类,如图所示,请填空:
(1)上图中分类标准1(分成A、B组的依据)为_________________________________。 (2)工业上常用D组中________________(填化学式),来消除C组中物质对大气的污染,该反应的化学方程式为_____________________________________________。 (3)实验室由Al3+制备Al(OH)3时,应选择D组中________(填化学式)的水溶液,离子方程式为__________________________。 (4)F组中有两种物质,在工业上均有重要的用途,请各写出一个化学方程式表示其用途: ________________________________;________________________________________。
|
|
| 20. | 详细信息 |
|
(1)下列实验方法合理的是________。 A.用加热法除去碳酸钠固体中的碳酸氢钠 B.将碘的饱和水溶液中的 C.实验室制取Al(OH)3:向AlCl3溶液中加入NaOH溶液至过量 D.向FeCl2溶液中滴入KSCN溶液,检验FeCl2是否已氧化变质 (2)某研究
A、C中为干燥的有色布条,B为无色液体,D中为Na ① 在常温下,KMnO4固体可以与浓盐酸反应生成氯气,其反应方程式为 2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O, 则其反应装置应选用甲、乙、丙中的________。 ② B中的液体为____________,其作用为_________________________________。 ③ A、C中有色布条的颜色变化分别为__________________________________,A、C的实验现象说明氯气是否具有漂白性?________(填“是”或“否”)。 ④ D中NaOH溶液的作用是_______________________(用离子方程式说明)。 ⑤ 将产生的氯气通入滴有酚酞的NaOH溶液中,溶液红色褪去。小组内有甲、乙两种意见: 甲:氯气溶于水后溶液显酸性,中和了NaOH,使溶液褪为无色; 乙:氯气溶于水生成漂白性物质,使溶液褪为无色。 丙同学在褪色后的溶液中逐渐加入足量的NaOH溶液,溶液一直未见红色,则 ________(填“甲”或“乙”)的意见正确。
|
|
| 21. | 详细信息 |
|
有A、B两种常温下有刺激性气味的气体,将A通入品红溶液中,品红溶液变为无色;将B通入品红溶液中,品红溶液也变为无色;将A和B按1∶1的体积比混合充分,通入品红溶液中,品红溶液不褪色。只将A通入紫色石蕊溶液中,溶液只变红不褪色。试回答下列问题: (1)写出A、B的化学式:________、________。 (2) 写出A和B按1∶1的体积比混合充分的离子方程式::_______________________。 (3) 加热通入A后变为无色的品红溶液,现象是________________________; 加热通入B后变为无色的品红溶液,现象是_______________________
|
|