2021江苏苏教版高中化学月考试卷
| 1. | 详细信息 |
|
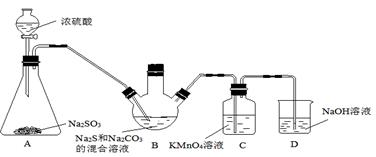
实验室制取硫代硫酸钠晶体(Na2S2O3·5H2O)的装置如图所示。
(1)装置A用于制备SO2,该反应的化学方程式为 ▲ 。 (2)为使SO2在装置B中吸收完全,下列措施合理的是 ▲ 。(填字母) a.B装置溶液中的导管口使用多孔球泡 b.减慢浓硫酸的滴加速度 c.适当搅拌 d.加热煮沸 (3)为测定某Na2S2O3·5H2O样品的纯度,进行如下实验:①取0.750 g样品,溶于水,配成50 mL的溶液X。②向10 mL 0.0100 mol·L-1的K2Cr2O7酸性溶液中加入2 g KI(过量),发生反应
|
|
| 2. | 详细信息 |
|
阅读下列材料,回答7~13题。 以电解饱和食盐水为基础制取Cl2(2NaCl + 2H2O 7.下列化学用语表示不正确的是 A.中子数为18的Cl: C.NaCl的电离方程式:NaCl = Na+ + Cl- D.氯原子的结构示意图: 8.电解饱和食盐水涉及到的物质中属于氧化物的是 A.NaCl B.H2O C.NaOH D.Cl2 9.检验Cl2的反应 Cl2+2KI=2KCl+I2 属于 A.化合反应 B.分解反应 C.置换反应 D.复分解反应 10.检验Cl2的反应中 Cl2+2KI=2KCl+I2 氧化剂是 A.Cl2 B.KI C.I2 D.KCl 11.下列关于Cl2的离子方程式中正确的是 A.MnO2和浓盐酸反应:MnO2 + 4H+ + 4Cl- B.Cl2与KI溶液反应:Cl2 + 2I-= I2 + 2Cl- C.Cl2与NaOH溶液反应:Cl2 + 2OH-= 2ClO-+ H2↑ D.Cl2与FeCl2溶液反应:Cl2 + Fe2+ = 2Cl-+ Fe3+ 12.实验室收集HCl可以采用的方法是 A. 13.下列关于工业合成氨反应的说法正确的是 A.升高体系温度能加快反应速率 B.降低N2的浓度能加快反应速率 C.使用催化剂不影响反应速率 D.反应若在密闭容器中进行,N2和H2能100%转化
|
|
| 3. | 详细信息 |
|
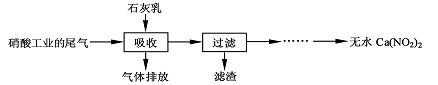
利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得应用广泛的Ca(NO2)2,其部分工艺流程如下:
(1)上述工艺中采用气-液逆流接触吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋),其目的是 ▲ 。 (2)滤渣可循环使用,滤渣的主要成分是 ▲ (填化学式)。 (3)工业生产中常用石灰乳与氯气制备漂白粉,写出制备反应化学方程式为 ▲ 。
|
|
| 4. | 详细信息 |
|
苯甲酸( (1)苯甲酸中的含氧官能团为 ▲ 。(填名称) (2)根据苯甲酸的结构简式推断,向苯甲酸溶液中滴加2~3滴紫色石蕊试液,溶液会 变成 ▲ 色。 (3)苯甲酸钠( (4)苯甲酸乙酯(
|
|
| 5. | 详细信息 |
|
某溶液中只可能含有下列离子中的若干种: A.一定不存在 C.一定存在K+ D.c
|
|
| 6. | 详细信息 |
|
短周期主族元素X、Y、Z、W的原子序数依次增大, X原子的核内质子数为8,Y原子最外层只有1个电子,Z原子最外层电子数是其电子层数的2倍,W原子最外层电子数为7。下列叙述正确 A.Z的非金属性比X的强 B.X、Y形成的化合物是共价化合物 C.W的简单气态气化物的热稳定性比Z的强 D.原子半径的大小顺序:r(W)>r(Z)>r(Y)>r(X)
|
|
| 7. | 详细信息 |
|
下列有机反应方程式书写正确的是 A.2CH3CH2OH + 2Na B. CH2=CH2 + Br2 C.CH4 + Cl2 D.CH3COOH + CH3CH2OH
|
|
| 8. | 详细信息 |
|
下列关于乙醇的说法正确的是 A.可用作燃料 B.属于有机高分子 C.能发生加成反应 D.与乙酸互为同分异构体
|
|
| 9. | 详细信息 |
|
下图为番茄电池,下列说法正确的是
A.一段时间后,锌片质量会增大 B.一段时间后,铜片质量会减小 C.电子由锌通过导线流向铜 D.锌电极是该电池的正极
|
|
| 10. | 详细信息 |
|
下列鉴别物质的方法能达到目的的是 A.用丁达尔效应鉴别NaCl和KCl溶液 B.用肥皂水鉴别CaCl2和Ca(NO3)2溶液 C.用KSCN溶液鉴别FeCl3和Fe2(SO4)3溶液 D.用加热法鉴别Na2CO3和NaHCO3固体
|
|
| 11. | 详细信息 |
|
常温下,下列物质可以用铝制容器盛装的是 A.氢氧化钠溶液 B.浓硝酸 C.浓盐酸 D.稀硫酸
|
|
| 12. | 详细信息 |
|
下列关于铁及其化合物的描述中,正确的是 A.铁的硬度很小 B.铁可以被磁铁吸引 C.Fe在O2中燃烧生成Fe2O3 D.常温下,Fe与浓硫酸不反应
|
|
| 13. | 详细信息 |
|
下列关于SO2的说法正确的是 A.无色无味 B.难溶于水 C.能使品红溶液褪色 D.密度比空气的小
|
|
| 14. | 详细信息 |
|
下列反应属于吸热反应的是 A.盐酸与氢氧化钠溶液的反应 B.生石灰和水的反应 C.石灰石在高温下的分解反应 D.甲烷在空气中燃烧
|
|
| 15. | 详细信息 |
|
下列叙述正确的是 A.硝酸具有强还原性 B.光导纤维的主要成分是硅酸盐 C.氧化钠可用作潜艇里氧气的来源 D.天然气的主要成分是CH4
|
|
| 16. | 详细信息 |
|
用洁净的 A.紫色 B.红色 C.绿色 D.黄色
|
|
| 17. | 详细信息 |
|
光导纤维已成为信息社会必不可少的高技术材料。光导纤维的主要成分是 A.金刚石 B.二氧化硅 C.铝合金 D.大理石
|
|
| 18. | 详细信息 |
|
下列物质属于共价化合物的是 A.CaCl2 B.H2O C.K2O D.Na2O
|
|
| 19. | 详细信息 |
|
下列气体中不能用浓硫酸干燥的是 A.O2 B.CO2 C.NH3 D.SO2
|
|
| 20. | 详细信息 |
|
下列物质能在空气中燃烧的是 A.N2 B.S C.H2O D.CO2
|
|
| 21. | 详细信息 |
|
下列仪器中一般不用作反应容器的是 A.试管 B.烧瓶 C.烧杯 D.量筒
|
|
| 22. | 详细信息 |
|
下列变化属于物理变化的是 A.碘的升华 B.炭的燃烧 C.铁的锈蚀 D.铝的冶炼
|
|
| 23. | 详细信息 |
|
葡萄糖是活细胞的能量来源和新陈代谢的中间产物。葡萄糖分子中不含的元素是 A.碳 B.氢 C.氧 D.氮
|
|