2017九年级上学期人教版初中化学期末考试
| 1. | 详细信息 |
|
A.氮气B.二氧化碳 C.氧气D.稀有气体
|
|
| 2. | 详细信息 |
|
通过实验测定了空气的组成的科学家是 A.门捷列夫 B.道尔顿 C.拉瓦锡 D.牛顿
|
|
| 3. | 详细信息 |
|
下列安全图标中,表示“禁止烟火”的是
ABCD
|
|
| 4. | 详细信息 |
|
下列物质在氧气中燃烧,发出白光的是 A.木炭 B.甲烷 C.红磷 D.铁丝
|
|
| 5. | 详细信息 |
|
地壳中含量最高的金属元素是 A.氧B.铝 C.硅D.铁
|
|
| 6. | 详细信息 |
|
下列物质的用途中,利用其物理性质的是 A.液氮用作冷冻剂B.二氧化碳作光合作用原料 C.一氧化碳用作燃料D.稀有气体作焊接金属时的保护气
|
|
| 7. | 详细信息 |
|
下列不属于氧气用途的是 A.潜水 B.急救 C.灭火D.气焊
|
|
| 8. | 详细信息 |
|
下列灭火措施中,正确的是 A.炒菜时油锅着火--用水烧灭 B.电器着火--用水烧灭
|
|
| 9. | 详细信息 |
|
下列符号中,能保持氮气化学性质的最小微粒是 A.N2B.2N2 C.2N D.2N3-
|
|
| 10. | 详细信息 |
|
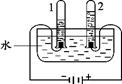
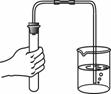
右图是电解水的实验装置。下列说法中,正确的是
B.实验说明水是由氢原子和氧原子构成的 C.2管内产生的气体能使木条复燃 D.1、2两试管产生的气体质量之比为2:1
|
|
| 11. | 详细信息 |
|
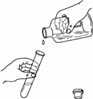
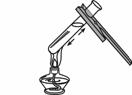
下列实验操作中,正确的是
A.倾倒液体B.加热液体 C.点燃酒精灯D.检查气密性
|
|
| 12. | 详细信息 |
|
吸烟有害健康,烟气中含有的一种有毒气体是 A. 氧气B. 一氧化碳C. 二氧化碳 D.氮气
|
|
| 13. | 详细信息 |
|
下列做法中,不利于保护水资源的是 A.使用节水型马桶 B.合理使用农药和化肥 C.生活污水任意排放D.工业废水处理达标后排放
|
|
| 14. | 详细信息 |
|
已知一种氯原子,原子核内含有17个质子和18个中子,则该氯原子核外电子数为 A.1 B.17C.18 D.35
|
|
| 15. | 详细信息 |
|
下列关于2CO + O2====2CO2的理解不正确的是 A.表示一氧化碳与氧气在点燃条件下反应生成二氧化碳 B.参加反应的一氧化碳与氧气的质量比为5:4 C.反应前后碳原子、氧原子的个数均不变 D.参加反应的氧气与生成的二氧化碳的分子个数比为1:2
|
|
| 16. | 详细信息 | |||||||||||||||
|
下列实验操作中,能达到实验目的的是
|
||||||||||||||||
| 17. | 详细信息 |
|
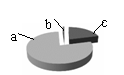
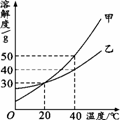
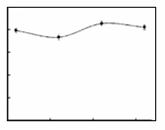
甲、乙两种固体的溶解度曲线如右图所示。下列说法中,不正确的是
B.乙的饱和溶液从40℃降到20℃时,溶液仍饱和 C.20℃时,甲、乙两溶液的溶质质量分数一定相等 D.20℃时,分别向100 g水中加入40 g甲、乙,加热到 40℃时,乙溶液为饱和溶液
|
|
| 18. | 详细信息 |
|
“分子机器”是指在分子尺寸上制造的一类分子器件,其长短仅相当于l纳米左右(1纳米=10-9米)。它的驱动方式是通过外部刺激(如电能、光照等)使分子结构发生改变,从而对外做功。下列关于分子机器的说法中,正确的是 A.肉眼能直接观察到分子机器 B.分子机器驱动过程中,发生了化学变化 C.分子机器的驱动不需要能量 D.分子机器“发动机”驱动方式与普通发动机相同
|
|
| 19. | 详细信息 |
|
已知:2KClO3==== 2KCl + 3O2↑,下列图像表示一定质量的KClO3和MnO2固体混合物受热过程中某些量随加热时间的变化趋势,其中不正确的是
A B C D
|
|
| 20. | 详细信息 |
|
一年分为二十四个节气,立春是二十四节气中的第一个。吃春饼是立春时中国民间饮食风俗之一。制作春饼的主要原料有面粉、食盐、鸡蛋、水、植物油、蔬菜等。 (1)上述原料加水后能形成溶液的是。 (2)下列量杯中,最适于量取400mL水的是(填字母)。
A.10 mL量杯 B.100 mL量杯 C.500 mL量杯
|
|
| 21. | 详细信息 |
|
炒菜过程中散发出诱人的香味,你能闻到香味的原因是 A.分子的体积很小 B.分子的质量很小C.分子之间有间隔 D.分子在不断运动
|
|
| 22. | 详细信息 |
|
明德馆。进入明德馆,桌上的纸墨笔砚映入眼帘。 (1)下列关于宣纸的传统制作工艺中,主要发生化学变化的是(填字母)。
A.粉碎原料B.加碱反应 C.竹帘捞纸 D.剪裁纸张 (2)古代字画能长期保存,是由于单质碳在常温下具有。
|
|
| 23. | 详细信息 |
|
(1)绿原酸分子中氢、氧原子个数比为。 (2)绿原酸的相对分子质量是354,其计算式为。
|
|
| 24. | 详细信息 | ||
|
无土栽培大讲堂。无土栽培是指不用天然土壤而用基质,在定植以后用营养液进行灌溉的栽培方法。 (1)营养液是无土栽培作物所需氮、磷、钾等营养成分和水分主要来源,营养液属于 仙客来营养液配方为每100L中含有: 硝酸钾(KNO3) 50.0g 硫酸钾(K2SO4) 25.0g 磷酸二氢钙[Ca(H2PO4)2] 8.0g 硫酸镁(MgSO4·7H2O) 16.0g 硼酸(H3BO3) 0.14g 硫酸锰(MnSO4·4H2O) 0.14g 硫酸锌(ZnSO4·7H2O) 0.14g 硫酸铜(CuSO4·5H2O) 0.14g 硫酸亚铁(FeSO4·7H2O) 0.14g (2)右图为仙客来(又名萝卜海棠)的营养液配方, 其中能为植物生长提供氮元素的物质是, 计算100L该营养液能提供的氮元素质量 约为g(计算结果精确到0.1)。
|
|||
| 25. | 详细信息 |
|
(1)元素周期表中铁元素的信息如右图所示,其原子的相对原子质量 为。 (2)O2和O3是由氧元素组成的两种单质,但是它们的性质有很大的差异,其原因是。 (3)某有机物在纯氧中完全燃烧只生成CO2和H2O,则该有机物的组成中一定含有的元素是。
|
|
| 26. | 详细信息 | ||||
|
请从28-A或28-B两组趣味实验中任选1个作答,若两题均作答,按28-A计分。
|
|||||
| 27. | 详细信息 | ||||||||||||||
|
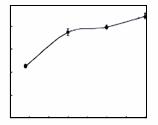
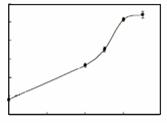
阅读下面科普短文(原文作者:龙门、宋野等,原文有删改) 咸鸭蛋是人们常用的一种食品,咸鸭蛋黄还是制作粽子、点心等食品的材料。咸鸭蛋中富含锌、钙,对儿童身体及骨骼的生长有帮助,并能在一定程度上预防贫血。 资料1:腌制原理 咸鸭蛋在腌制过程中,食盐通过蛋壳及蛋壳膜不断向蛋内渗透,虽然没有改变蛋白质及脂肪的成分,但却改变了蛋白中蛋白质的特性及蛋黄中脂质含量。 资料2:腌制过程 腌制鸭蛋一般经过以下几个步骤:鲜蛋→检验(照蛋)→洗蛋→晾干→放入食盐水溶液中装罐→腌制。一般腌制30天,就能得到味美的咸鸭蛋。资料显示,将晾干后的鲜鸭蛋放入1%的盐酸溶液中浸泡10分钟,蛋壳(主要成分是CaCO3)与盐酸溶液发生反应,蛋壳表面的毛孔增大。放入饱和的食盐水中,溶液更易通过蛋膜进入蛋清,只需7天左右就可腌制出合格的咸蛋(蛋内的食盐含量及蛋黄内的油脂含量均达到国家标准),且口感很好。 资料3:影响咸鸭蛋品质的因素 咸鸭蛋的蛋黄指数是鸭蛋品质的一个重要指标。一般情况下,蛋黄指数越高,品质越好。不同腌制条件对蛋黄指数的影响如下所示。 蛋 黄 指 数 /% 14 19 24 29 不同腌制用盐量/ (g/100g) 注:腌制温度为25oC;腌制时间为30天 0 10 20 30 40 不同腌制时间/天 注:腌制温度为25oC;腌制用盐量为30g/100g 蛋 黄 指 数 /% 蛋 黄 指 数 /% 90 80 70 60 50 40 30 0 5 15 20 25 30 35 40 不同腌制温度/oC 注:腌制时间30天;腌制 用盐量为30g/100g 资料4:咸鸭蛋的食用 咸鸭蛋与鲜蛋的营养价值基本相同,但咸鸭蛋中钠、钙、铁、硒等矿物质元素含量比鲜鸭蛋高。特别是含钠量高,折算成含盐量,每只咸蛋含盐在6g以上。长期高盐摄取是造成高血压、胃粘膜受损等疾病的原因。 依据文章内容,回答下列问题。 (1)鲜鸭蛋及咸鸭蛋中均含锌、钙,“锌”“钙”指的是________(填“分子”、“原子” 或“元素”)。 (2)请写出蛋壳和盐酸反应的化学方程式__________。 (3)影响咸鸭蛋品质的因素有_____________。 (4)当腌制温度为25℃、腌制时间为30天时,用盐量为_____g/(100g),咸鸭蛋品质最高。 (5)请写出一条食用咸鸭蛋的建议_____________。
|
|||||||||||||||
| 28. | 详细信息 | |||
|
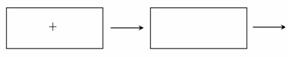
过氧化钠(Na2O2)为淡黄色固体,可用作潜水艇或呼吸面具的供氧剂, 工业制备的主要流程如下:
(1)4Na +O2====2Na2O(反应条件略去),该反应属于基本反应类型中的_____反应。 (2)已知过氧化钠(Na2O2)产生氧气(O2)的化学方程式为: 2Na2O2 +2CO2====2 Na2CO3+O2,理论上156g过氧化钠可制得氧气质量为g。
|
||||
| 29. | 详细信息 | ||||
|
① ② 图1软塑料瓶图2点滴板 【实验1】向图1集满CO2的软塑料瓶中,迅速倒入半瓶蒸馏水,旋紧瓶盖。充分振荡, 观察到塑料瓶变瘪,原因是。 【实验2】在图2点滴板①②两个孔内各滴加2滴紫色石蕊溶液;再向①孔中滴加5滴实验 1塑料瓶中的液体,向②孔中滴加5滴蒸馏水,观察到①孔中紫色石蕊变红,变红的原因是(用化学方程式表示)。②孔中滴加等量蒸馏水的目的是。
|
|||||
| 30. | 详细信息 |
|
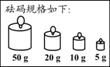
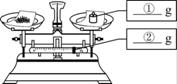
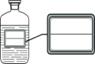
医学中常用溶质的质量分数为0.9%的氯化钠溶液来供给电解质和维持体液的张力。现配制1000g溶质的质量分数为0.9%的氯化钠溶液,实验操作如下: (1)称量氯化钠质量:在下图中分别标出所选砝码的质量和游码的示数。
(3)溶解时用到烧杯和玻璃棒,玻璃棒的作用是。 (4)装瓶、贴标签:在右图的标签中填上相应的内容。
|
|
| 31. | 详细信息 |
|
水寨。走出明德馆,立刻看到“水雾缭绕,如梦如幻,仿佛置身于云端”的水寨。“水寨云雾”是利用专用造雾机将净化后的水输送到造雾专用喷头喷出成雾。 (1)水变成水雾的过程中,没有发生变化的是(填字母)。 A.物质种类B.分子种类 C.分子间隔D.分子质量 (2)净水过程中常用到活性炭,其作用是、过滤水中的杂质。
|
|
| 32. | 详细信息 |
|
能源和人们的生产生活息息相关。 (1)目前人们使用的燃料大多数来自化石燃料。化石燃料包括天然气、煤、。 (2)天然气的主要成分是甲烷,甲烷燃烧的化学方程式为。 (3)化石燃料不可再生,目前人们正在积极开发和利用许多新能源,请例举一种。
|
|
| 33. | 详细信息 |
|
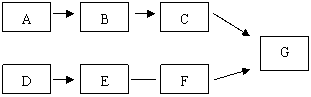
A、B、C、D、E、F、G都是由C、H、O中的一种或两种元素组成的初中化学常见的物质。常温常压下,G是无色、无味的液体,在4℃以上时,它的密度变化符合
(1)C的化学式是。 (2)A、B、C、D、E、F、G七种物质中,属于氧化物的是。 (3)请写出D生成E的化学方程式。 (4)若E与F反应只生成G,写出反应的化学方程式,并画出反应过程中各阶段的微观示意图。
|
|
| 34. | 详细信息 |
|
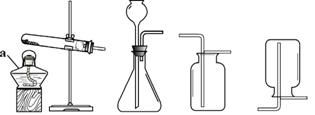
根据下图回答问题。
A B C D E (1)仪器a的名称是。 (2)实验室用高锰酸钾制取氧气应选择的发生装置是(填字母),反应的化学方程式为。 (3)装置E进行铁丝在氧气中燃烧实验,观察到的实验现象为,反应的 化学方程式为。
|
|
| 35. | 详细信息 | ||||||||
|
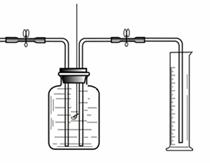
某同学利用下图所示装置进行实验。已知:白磷的着火点是40℃ 步骤I.检查装置的气密性。 步骤II.将盛有足量白磷的带孔燃烧匙伸入A瓶中,向瓶中加满80℃热水,塞紧瓶塞。 步骤III.打开K1、K2,从a口向瓶中鼓入空气,待瓶中的液面低于燃烧匙底部时, 关闭K1、K2。此时量筒中水的体积为200mL。 a K1 K2 80oC的热水 盛有足量 白磷的带孔 燃烧匙 A B (1)步骤Ⅲ中,关闭K1、K2后观察到的现象是,反应的化学方程式为。 (2)对比步骤II和III可知,可燃物燃烧的条件之一是。 (3)待装置冷却至室温后,打开K2,观察到,说明空气中氧气的含量约占1/5。
|
|||||||||
| 36. | 详细信息 | |||||||||||||||||||
|
实验,探究铜生锈的条件。
8cm,宽1cm,试管容积为20mL),分别进行下列7个实验,并持续观察30天。
【解释与结论】 (1)实验3中,要使用经煮沸并迅速冷却的蒸馏水,原因是。 (2) 实验5的目的是。 (3)通过上述实验,得出铜生锈的条件是。 【反思与评价】 (4)请写出一种防止铜制品锈蚀的方法。 (5)查阅资料可知,铜锈的主要成分是碱式碳酸铜,化学式为Cu2(OH)2CO3。 由此,你认为上述实验中只需进行实验(填实验编号),就可探究出铜生锈条件,理由是。 (6)与以上进行的实验对比,你认为铜片在通常状况的空气中,生锈非常缓慢的原因 可能是。
|
||||||||||||||||||||