2018云南高一上学期人教版高中化学月考试卷
| 1. | 详细信息 |
|
下列物质属于电解质的是( ) A.CO2 B.Cu C.Na2CO3溶液 D.NaCl
|
|
| 2. | 详细信息 |
|
设NA表示阿伏加德罗常数的值,下列叙述中正确的是( ) A. 常温常压下,48gO3含有的氧分子数为3NA B. 标准状况下,1.8g的水中含有的氧原子数为0.1NA C. 22.4 L O2中含有的氧气分子数约为6.02×1023 D. 1mol O2氧气分子所占的体积数约为22.4 L
|
|
| 3. | 详细信息 |
|
关于方程:3Cu + 8 HNO3 ═ 3Cu(NO3)2 + 2 NO↑ + 4H2O下列叙述正确的是( ) A. 当有12.8g Cu参加反应,转移的电 B. 还原剂是Cu,还原产物是Cu(NO3)2 C. 反应中HNO3 既表现为酸性又表现为还原性 D. Cu(NO3)2既是氧化产物又是还原产物
|
|
| 4. | 详细信息 |
|
下列反应不是氧化还原反应的是( ) A. 2Cu + O2 ═ 2 CuO B. CaO + H2O ═ Ca(OH)2 C. 2KMnO4 ═ K2MnO4 + MnO2 + O2↑ D. 2Na + 2H2O ═ 2NaOH + H2↑
|
|
| 5. | 详细信息 |
|
下列离子在溶液中能大量共存的是( ) C. Cu2+、Ba2+、Cl﹣、SO42﹣ D. K+、Na+、OH﹣、Cl﹣
|
|
| 6. | 详细信息 |
|
下列离子方程式书写正确的 A. 稀硫酸滴到铁片上:Fe + H+ ═ Fe2+ + H2↑ B. 硫酸铜溶液与氢氧化钠溶液混合:CuSO4 + C. 碳酸钠溶液与稀盐酸反应:CO32﹣ + 2H+ ═ H2CO3 D. 碳酸氢钠溶液与盐酸混合:HCO3﹣+ H+ ═ H2O + CO2↑
|
|
| 7. | 详细信息 |
|
①有尘埃的空气、②溴水、③蒸馏水、④沸水中加几滴FeCl3浓溶液、⑤淀粉溶液,其中不存在丁达尔效应的是( ) A. ② B. ②③⑤ C. ②③ D. ①②③⑤
|
|
| 8. | 详细信息 |
|
下列物质 ①Na ②Br2 ③NaCl溶液 ④CO2 ⑤HCl ⑥Ba(OH)2 ⑦熔融的KCl
A. 属于电解质的是④⑤⑥⑦ B. 属于非电解质的是①②③④⑧ C. 既不是电解质也不是非电解质的是①②③④ D. 能导电的是①③⑦
|
|
| 9. | 详细信息 |
|
下列溶液中的Cl﹣浓度与50mL, 1mol•L﹣1 MgCl2 溶液中的Cl﹣浓度相等的是( ) A. 150 mL ,1 mol•L﹣1 NaCl溶液 B. 75 C. 150 mL ,2 mol•L﹣1 KCl溶液 D. 75 mL, 1 mol•L﹣1 AlCl3 溶液
|
|
| 10. | 详细信息 |
|
下列对氧化还原反应的分析中不合理的是( ) A. Mg变为MgO时化合价升高,故Mg在该反应中作还原剂 B. 在反应 2H2S + SO2 ═ 3S + 2H2O中,氧化产物和还原产物都是S C. 凡是置换反应都是氧化还原反应 D. 在反应2H2O
|
|
| 11. | 详细信息 |
|
.根据下列物质中硫的化合价判断,下列说法错误的是( ) A. Na2S具有还原性 B. SO2既有氧化性又有还原性 C. 浓H2SO4 具有氧化性 D. SO3 具有还原性
|
|
| 12. | 详细信息 |
|
在下列反应中,盐 A. NaOH + HCl ═ NaCl + H2O B. MnO2 + 4HCl(浓)═ MnCl2 + 2H2O C. Fe + 2HCl ═ FeCl2 + H2↑ D. CaCO3+ 2HCl ═ CaCl2 + H2O + CO2↑
|
|
| 13. | 详细信息 |
|
在下列各变化过程中,一定要加还原剂才能实现的是( ) A. HNO3→NO B. H2S→S C. FeCl2 → FeCl3 D. SO32﹣→SO2
|
|
| 14. | 详细信息 |
|
根据反应式: 2Fe3+ + 2 I﹣═ 2Fe2+ + I2, Br2 + 2Fe2+ ═ 2Br﹣ + 2Fe3+, 可以判断微粒的氧化性从强到弱的顺序是( ) A. Fe3+、Br2、I2 B. I2、Br2、Fe3+ C. Br2、Fe3+、I2 D. Br2、I2、Fe3+
|
|
| 15. | 详细信息 |
|
在SO2 + 2 H2S ═ 3 S↓ + 2 H2O中氧化产物和还原产物质量之比为( ) A. 2:3 B. 2:1 C. 1:2 D. 3:2
|
|
| 16. | 详细信息 |
|
将30mL 0.5mol/L的NaOH溶液加水稀释到500mL,稀释后NaOH的物质的量浓度为( ) A. 0.3mol/L B. 0.05mol/L C. 0.04mol/L D. 0.03mol/L
|
|
| 17. | 详细信息 |
|
某溶液只含有Na+、Fe3+、Cl﹣、SO42﹣四种离子,已知Na+、Fe3+、Cl﹣的个数比为 3:2:1则溶液中Fe A. 1:2 B. 1:4 C. 3:4 D. 3:2
|
|
| 18. | 详细信息 |
|
在某无色透明的酸性溶液中,能共存的离子组是( ) A. Na+、K+、SO42﹣、HCO3﹣ B. Cu2+、K+、SO42﹣、NO3﹣ C. Na+、K+、Cl﹣、NO3﹣ D. Fe3+、K+、SO42﹣、Cl﹣
|
|
| 19. | 详细信息 |
|
有一句歌词“雾里看花,水中望月”,有关其中的雾说法正确的是( ) A. 雾是溶液,能永久在空气中稳定存在 B. 雾是胶体,一段时间内能稳定存在 C. 雾是乳浊液,不能稳定存在 D. 雾的悬浊液,在空气中能沉降
|
|
| 20. | 详细信息 |
|
下列反应中,水既不是氧化剂又不是还原剂的氧化还原反应是( ) A. SO3 + H2O ═ H2SO4 B. Cl2 + H2O ═ HCl + HClO C. 2 F2 + 2H2O ═ 4 HF + O2 D. 2 Na + 2 H2O ═ 2 NaOH + H2↑
|
|
| 21. | 详细信息 |
|
写出下列反应的离子方程式 ⑴ NaHCO3溶液和NaOH溶液反应 ____________________________________ ⑵ NaHSO4溶液中滴加Ba(OH)2溶液至呈中性 ____________________________________ ⑶ 2NaClO3 +4HCl ═ 2ClO2 +Cl2↑+2NaCl +2H2O
|
|
| 22. | 详细信息 |
|
现有失去标签的氯化钙、硝酸银、盐酸、碳酸钠四种无色溶液,为了确定四种溶液各是什么,将它们随意编上A、B、C、D后,产生的现象如表所示。根据实验现象推断 写出A、B溶液中溶质的化学式:A_________________;B ________________ ; 写出反应③④的离子方程式: ③ _____________________________________________
④_____________________________________________
|
|
| 23. | 详细信息 |
|
用双线桥标出电子转移的方向和数目 2 KClO3 ═ 2 KCl + 3 O2↑
|
|
| 24. | 详细信息 |
|
用单线桥表示下列反应中电子转移的方向和数目 MnO2+4HCl═MnCl2+Cl2↑+2H2O
|
|
| 25. | 详细信息 |
|
反应KClO3 + 6HCl ═ KCl + 3Cl2↑ + 3H2O,若生成标准状况下6.72 L氯气,则转移电子的物质的量为___
|
|
| 26. | 详细信息 |
|
NaNO2是一种食品添加剂,能致癌。酸性KMnO4溶液与NaNO2反应的离子方程式是 MnO4- + NO2- + ________ →Mn2+ + NO3- + H2O (未配平) 空格中的粒子是_________,氧化剂与还原产物物质的量之比是________ .
|
|
| 27. | 详细信息 |
|
一定条件下PbO2与Cr3+反应,产物是Cr 2 O72-和Pb2+
|
|
| 28. | 详细信息 |
|
在反应2 KNO3 + S + 3C ═ K 2 S + N2↑ + 3CO2↑中,氧化剂是____________________
|
|
| 29. | 详细信息 |
|
12.4gNa2X中含Na+ 0.4mol,则Na2X的摩尔质量是______________ mol
|
|
| 30. | 详细信息 |
|
现需配制450mL 0.1mol/LNaOH溶液,计算所需NaOH的质量为_____________g
|
|
| 31. | 详细信息 |
|
实验室常用浓盐酸的质量分数为36.5%,密度为1.20g/cm-3。此浓盐酸的物质的量浓度为____________
|
|
| 32. | 详细信息 |
|
在同温同压下,同体积的O3和O2密度之比为____________ 。
|
|
| 33. | 详细信息 |
|
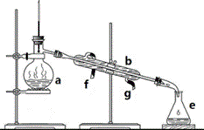
写出下列仪器的名称:a. ____________ 冷凝水由____________ 口通入(填f或g)
|
|