2019福建高一上学期人教版(2019)高中化学中考真题
| 1. | 详细信息 |
|
下列有关物质组成的说法正确的是( ) A.物质均是由分子构成,分子均是由原子构成的 B.某物质经测定,只含有一种组成元素,则该物质不一定是单质 C.不能与酸反应的氧化物一定能跟碱反应 D.碱性氧化物均是金属氧化物,酸性氧化物均是非金属氧化物
|
|
| 2. | 详细信息 | |||||||||||||||||||||||||
|
下列物质分类的正确组合是( )
|
||||||||||||||||||||||||||
| 3. | 详细信息 |
|
下列物质中,易溶于水的是( ) A.KNO3 B.BaCO3 C.AgCl D.CuO
|
|
| 4. | 详细信息 |
|
下列物质属于纯净物的是( ) A.氢氧化铁胶体 B.碘酒 C.胆矾(CuSO4·5H2O ) D.生铁
|
|
| 5. | 详细信息 |
|
下列反应既是化合反应,又是氧化反应的是( ) A.2CO+O2 C. CaO+H2O=Ca(OH)2 D.CO2+Ca(OH)2=CaCO3↓+H2O
|
|
| 6. | 详细信息 |
|
设NA为阿伏加德罗常数的值,下列说法正确的是( ) A.标准状况下,18 g H2O所占的体积约为22.4L B.28g N2所含的原子数目为NA C.在常温常压下,11.2 L N2含有的原子数为NA D.0.5 mol H2SO4含有的原子数目为3.5NA
|
|
| 7. | 详细信息 |
|
下列说法正确的是( ) A.1molO2的质量是32g.mol—1 B.H2的摩尔质量是2g C.1molH+的质量是1g D.对原子而言,摩尔质量就是相对原子质量
|
|
| 8. | 详细信息 |
|
两份质量相同的CH4和NH3比较,下列结论错误的是( ) A.分子个数比为17∶16 B.原子个数比为17∶16 C.氢原子个数比为17∶12 D.氢原子质量比为17∶12
|
|
| 9. | 详细信息 |
|
已知3.01×1023个X气体分子的质量为16g,则X气体的摩尔质量是( ) A.16g B.32g C.64g /mol D.32g /mol
|
|
| 10. | 详细信息 |
|
下列物质,所含分子数最多的是(NA为阿伏加德罗常数)( ) A.10gH2 B.2molCl2 C.1.5NACO2 D.22.4LO2(标况下)
|
|
| 11. | 详细信息 |
|
下列溶液中,跟100mL0.5mol/L NaCl溶液所含的Cl-物质的量浓度相同的是( ) A.100mL 0.5mol/L MgCl2溶液 B.200mL 0.25mol/L AlCl3溶液 C.50ml 1mol/L NaCl溶液 D.25ml 0.5mol/L HCl溶液
|
|
| 12. | 详细信息 |
|
有关2 L 0.1 mol·L-1的K2SO4溶液的叙述正确的是( ) A.含有0.1 mol K2SO4 B.K+的物质的量浓度为0.1 mol·L-1 C.取出1 L溶液后,浓度变为0.05 mol·L-1 D.K+的物质的量为0.4 mol
|
|
| 13. | 详细信息 |
|
13C—NMR(核磁共振)、15N—NMR可用于测定蛋白质、核酸等生物大分子的空间结构,下面有关13C、15N的叙述,正确的是( ) A.15N与14N互为同位素 B.13C与C60互为同位素 C.13C与15N具有相同的中子数 D.15N的核外电子数与中子数相同
|
|
| 14. | 详细信息 |
|
某微粒用符号Mn+表示,下列关于该微粒的叙述中正确的是( ) A.所含质子数为(A-n) B.所含中子数为Z C.中子数-电子数=A-2Z+ n D.所含电子数为(Z+ n)
|
|
| 15. | 详细信息 |
|
下列关于胶体的叙述中,不正确的是( ) A.胶体是一种介稳体系 B.胶体中分散质粒子的直径小于1 nm C.用滤纸能分离胶体和悬浊液 D.利用丁达尔效应可以区分溶液和胶体
|
|
| 16. | 详细信息 |
|
溶液、胶体和浊液这三种分散系的根本区别是( ) A.是否是大量分子或离子的集合体 B.是否能通过滤纸 C.分散质粒子直径的大小 D.是否均一、透明、稳定
|
|
| 17. | 详细信息 |
|
对电解质概念的理解正确的是( ) A.在水溶液或熔融状态下能导电的物质 B.氧化钠溶于水能电离生成钠离子和氢氧根离子,尽管氧化钠是化合物,其水溶液能导电,但溶液中的氢氧根离子并非氧化钠本身电离,因而氧化钠是非电解质 C.凡在水中能生成离子而导电的物质 D.在水溶液里或熔融状态下本身能电离出离子而导电的化合物
|
|
| 18. | 详细信息 |
|
下列按纯净物、混合物、电解质和非电解质顺序排列的是( ) A.盐酸、空气、醋酸、干冰 B.冰醋酸、70%酒精、硫酸钠、乙醇 C.蛋白质、油脂、苛性钾、石灰石 D.胆矾、漂白粉、氯化钾、硫酸钡
|
|
| 19. | 详细信息 |
|
下列电离方程式正确的是( ) A.Al2(SO4)3=2Al3+ + 3SO42- B.NaHCO3=Na+ + H+ + CO32- C.Ba(OH)2= Ba2+ + (OH-)2 D.Na2SO3=Na++SO32-
|
|
| 20. | 详细信息 |
|
下列物质的水溶液能导电,但属于非电解质的是( ) A.CH3COOH B.Cl2 C.(NH4)2CO3 D.SO2
|
|
| 21. | 详细信息 |
|
能够用来鉴别BaCl2、NaCl、Na2CO3三种物质的试剂是( ) A.稀硫酸 B.稀硝酸 C.稀盐酸 D.AgNO3溶液
|
|
| 22. | 详细信息 |
|
为了检验某固体物质中是否含有NH4+,下列组合正确的是( ) ①蒸馏水 ②NaOH溶液 ③红色石蕊试纸 ④蓝色石蕊试纸 ⑤稀硫酸 A.①③ B.④⑤ C.①②③ D.①④⑤
|
|
| 23. | 详细信息 |
|
下列实验操作中正确的是( ) A.蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 B.蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 C.分液操作时,先将分液漏斗中下层液体从下口放出,再将上层液体从下口放出 D.萃取操作时,可以选用CCl4或酒精作为萃取剂从溴水中萃取溴
|
|
| 24. | 详细信息 |
|
关于某无色溶液中所含离子的鉴别,下列判断正确的是( ) A.加入AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不消失,可确定有Cl-存在 B.加入盐酸,生成的气体能使澄清石灰水变浑浊,可确定有CO32-存在 C.加入Ba(NO3)2,生成白色沉淀,加稀盐酸沉淀不消失,可确定有SO42-存在 D.用洁净的铂丝蘸取溶液放在火焰上灼烧,观察到火焰呈黄色,可确定有Na+存在
|
|
| 25. | 详细信息 |
|
下列分离或提纯物质的方法正确的是( ) A.用蒸发法进行海水淡化 B.用酒精萃取碘水中的碘 C.用渗析(带半透膜)的方法除去淀粉溶液中含有的少量NaCl D.用加热→蒸发的方法可以除去粗盐中的CaCl2、MgCl2等杂质
|
|
| 26. | 详细信息 |
|
NH3的摩尔质量为 ,8.5 g NH3的物质的量是________mol,含有 个氨分子,标准状况下占有的体积是___________L。
|
|
| 27. | 详细信息 |
|
将24 g NaOH固体溶于水配成100 mL溶液。 (1)该溶液中NaOH的物质的量浓度为 。 (2)从该溶液中取出10 mL,其中NaOH的物质的量浓度为 ,含NaOH的物质的量为 。 (3)将取出的10 mL溶液加水稀释到100 mL,稀释后溶液中NaOH的物质的量浓度为 。
|
|
| 28. | 详细信息 |
|
已知①NaOH溶液 ②铜丝 ③液态HCl ④盐酸 ⑤稀硫酸 ⑥液氨 ⑦氨水 ⑧SO2 ⑨蔗糖晶体 ⑩熔融NaCl (填序号) (1)属于电解质是 ;(2)属于非电解质的是 ; (3)上述状态下可导电的是 。
|
|
| 29. | 详细信息 |
|
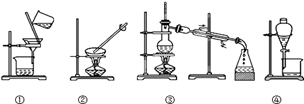
观察下列实验装置图,试回答下列问题:
(1)写出装置④中所用玻璃仪器(除烧杯外)的名称 。 (2)下列实验需要在哪套装置中进行(填序号): a、从海水中提取蒸馏水: ; b、分离氯化钠和水: ; c、分离碳酸钙和水: ; d、分离植物油和水: 。
|
|
| 30. | 详细信息 |
|
实验室要配制80mL 1mol·L-1的NaCl溶液,试回答下列各题: (1)下列仪器中,不会用到的是 ( ) A.锥形瓶 B.200mL容量瓶 C.50mL容量瓶 D.胶头滴管 E.100mL容量瓶 F.托盘天平 (2)若要实施配制,除上述仪器外,尚缺的仪器或用品是 (3)人们常将配制过程简述为以下各步骤: A.冷却 B.称量 C.洗涤 D.定容 E.溶解 F.摇匀 G.转移 其正确的操作顺序应是_____________________________(填各步骤序号)。 (4)配制完毕后,教师指出有四位同学各进行了下列某一项操作,你认为这四项操作会导致所得溶液浓度偏高的是 ( ) A.使用的容量瓶未干燥,瓶底有少量蒸馏水 B.定容时俯视容量瓶刻度线 C.将溶解冷却的溶液转入容量瓶后就直接转入定容操作 D.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处 (5)通过计算可得出可用托盘天平称取NaCl固体______________克。 (6)写出Na+的离子结构示意图 。
|
|
| 31. | 详细信息 |
|
10g碳酸钙与100ml盐酸恰好完全反应,盐酸的物质的量浓度为多少?生成二氧化碳气体的体积(标准状况)为多少?(要求:写出化学反应方程式进行列式计算)
|
|