2018贵州高三上学期人教版高中化学高考模拟
| 1. | 详细信息 |
|
化学与生活、社会、环境等密切相关。下列有关说法正确的是 A. 棉、丝、毛、油脂都是天然有机高分子化合物 B. 天然气作为化工原料可用于合成氨和生产甲醇 C. 酒是厨房中常见物质,其有效成分为CH3COOH D. 为了增加食物的营养成分,可以大量使用视频添加剂
|
|
| 2. | 详细信息 |
|
设NA为阿伏伽德罗常数的值,下列说法正确的是 A. 17g H2S中所含的电子数为9NA B. 9g H2O 中所含H-O键数为2NA C. 0.1mol CO2和2.24L CO 中所含碳原子数均为0.1NA D. 0.3mol NO2与足量水充分反应,生成H+数目为0.3NA
|
|
| 3. | 详细信息 |
|
下列离子方程式正确的是 A. 用NaOH溶液吸收Cl2:Cl2 +2OH- = 2Cl- + H2O B. Fe2(SO4)3和Ba(OH)2溶液混合 :Fe3++3OH-=Fe(OH)3↓ C. 向AgCl悬浊液中加入Na2S溶液 :2AgCl+S2-=Ag2S+2Cl- D. 向NaHCO3溶液中加入澄清石灰水 :HCO3-+OH-=CO32-+H2O
|
|
| 4. | 详细信息 |
|
下列有关有机物的叙述不正确的是 A. 甲烷、乙醇、乙酸和酯类都可以发生取代反应 B. 乙烯和苯都能使溴水褪色,但颜色的原因不同 C. 石油催化裂化的主要目的是提高芳香烃的产量 D. 纤维素和蛋白质都是能发生水解反应的高分子化合物
|
|
| 5. | 详细信息 |
|
以KI为碘剂的加碘食盐,由于受空气作用,容易引起碘的损失,工业生产中需添加稳定剂以减少碘的损失。下列物质中可能做稳定剂的是 A. Na2S2O3 B. FeCl3 C. NaHCO3 D. CaO
|
|
| 6. | 详细信息 |
|
甲、乙、丙、丁为四种主族元素,已知甲与乙、丙、丁三元素相邻;甲、乙的原子序数之和等于丙的原子序数,四种元素原子的最外层电子数之和为20。下列判断中,正确的是 A. 原子半径:丙>乙>甲 B. 最外层电子数:丙=丁 C. 气态氢化物的稳定性:甲>丙 D. 最高价氧化物对应的水化物的酸性:丁>甲
|
|
| 7. | 详细信息 | ||||||||||||||||||||
|
下列根据实验操作和现象所得出的结论不正确的是
A. A B. B C. C D. D
|
|||||||||||||||||||||
| 8. | 详细信息 | ||||||||||||||||||
|
硫酸是中学化学中最常用的试剂之一。请回答下列问题: (1)甲同学稀释浓硫酸的操作如下:用100mL量筒量取20mL 浓硫酸,并向其中小心地加入少量水,搅拌均匀,待冷却至室温后,再加入水至100mL刻度线,再搅拌均匀。该同学操作中的两处错误之处是__________、___________。 (2)乙同学准确配制3.6mol/L稀硫酸的操作为:量取20mL 18mol/L 浓硫酸,小心地倒入盛有少量水的烧杯中,搅拌均匀,待冷却至室温后转移到100ml 容量瓶中,用少量的水将烧杯等仪器洗涤2~3次,每次洗涤液也转移到容量瓶中,然后小心地向容量瓶加入水至刻度线定容,塞好瓶塞,反复上下颠倒摇匀。 ①该实验中两次用到玻璃棒,其作用分别是_________、________。 ②使用容量瓶前必须进行的一步操作是__________。 ③在该实验中,以下操作正确的是_________(填字母)。 a.洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中 b.待稀释后的H2SO4溶液冷却至室温再转移到容量瓶中 c.转移前应将使用的容量瓶烘干 d.定容摇匀后,发现凹液面低于刻度线,又用胶头滴管加蒸馏水至刻度线 ④若定容时不小心使液面超过了刻度线,应采取的措施是_______ (3)丙同学用已知物质的量浓度的硫酸来测定未知物质的量浓度的NaOH溶液时,以酚酞作指示剂。 ①滴定时,当观察到溶液_____________,即为滴定终点。 ②某同学根据3次实验分别记录有关数据如下表:
则待测NaOH溶液的浓度为___________,下列操作中可能使所测NaOH溶液的浓度数值偏低的是_________(填字母)。 A.酸式滴定管未用标准硫酸润洗就直接注入标准硫酸 B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥 C.酸式滴定管在滴定前有气泡,滴定后气泡消失 D.读取硫酸体积时,开始仰视读数,滴定结束时俯视读数
|
|||||||||||||||||||
| 9. | 详细信息 |
|
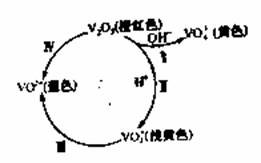
V2O5是工业制硫酸的重要催化剂。V2O5及其含V离子在溶液中存在如下转化关系:
回答下列问题: (1)从性质角度分类。V2O5属于_______(填“酸性”“碱性”或“两性”)氧化物,VO2+中钒元素的化合价为__________。 (2)写出反应Ⅰ的离子方程式:___________。 (3)向20mL 0.05mol/L (VO2)2SO4溶液中加入0.195g 锌粉,恰好完全反应,则还原产物中钒元素的存在形式为_________(填字母)。 a.V2+ b.V3+ c.VO2+ d.VO3- (4)在酸性环境中,向含有VO2+的溶液中滴加草酸(H2C2O4)溶液,可实现反应Ⅲ的转化,写出该反应的离子方程式:__________。 (5)将V2O5加入浓盐酸中可得蓝色溶液,并有黄绿色气体生成,该反应中还原产物与氧化常务的物质的量之比为__________。
|
|
| 10. | 详细信息 |
|
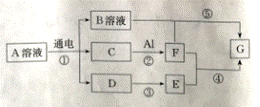
下图所示转化关系(部分物质未列出)中,A的焰色反应呈黄色,C、D、E是常见气体且C、D是单质。
请回答下列问题: (1)A的化学式为__________,电解时B在________极生成。 (2)工业上由D生成E的化学方程式为_____________。 (3)B溶液与G反应的离子方程式为_________________。 (4)上述转化中,属于非氧化还原反应的是__________(填数字代号)。 (5)取适量0.1mol/L 的F溶液,通入过量的E,现象是____________,充分反应后,所得溶液的pH=5.00,则此温度下残留在溶液中的c(Al3+)=________。[已知实验条件下Kap(G)=1.3×10-33]
|
|
| 11. | 详细信息 |
|
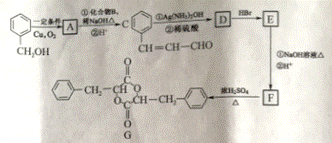
. 白芨有收敛止血,消肿生肌的功效,其有效成分G的一种合成路线如下:
已知: 回答下列问题: (1)A的分子式为_________。 (2)D中含氧官能团名称为__________。D (3)E的结构简式是__________。 (4)F (5)二取代方向化合物W是F的同分异构体,W既能与碳酸氢钠溶液反应生成二氧化碳,又能与FeCl3溶液发生显色反应。W共有_________种(不包括立体异构),其中核磁共振氢谱有6组峰,且峰面积比为1:1:2:2:2:2的是_______(填结构简式)。 (6)参照上述合成路线,以乙醛和丙烯醛为原料(无机试剂任选),设计制备戊酸的合成路线:_____
|
|