2019安徽高二上学期人教版(2019)高中化学期中考试
| 1. | 详细信息 |
|
下列说法正确的是( ) A. CaO+H2O=Ca(OH)2可放出大量热,可利用该反应设计成原电池,把化学能转化为电能 B. 任何化学反应中的能量变化都表现为热量变化 C. 有化学键断裂一定发生化学反应 D. 灼热的铂丝与NH3、O2混合气接触,铂丝继续保持红热,说明氨的氧化反应是放热反应
|
|
| 2. | 详细信息 |
|
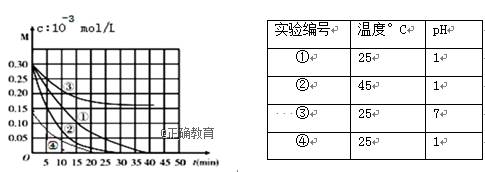
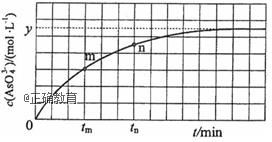
用Na2FeO4溶液氧化废水中的还原性污染物M,为研究降解效果,设计如下对比实验探究温度、浓度、 pH、催化剂对降解速率和效果的影响,实验测得M的浓度与时间关系如图所示:
下列说法正确的是( ) A. 实验①在15 min内M的降解速率为1.33×10-2mol/(L·min) B. 若其他条件相同,实验①②说明升高温度,M降解速率增大 C. 若其他条件相同,实验①③证明pH越高,越有利于M的降解 D. 实验②④说明M的浓度越小,降解的速率越慢
|
|
| 3. | 详细信息 |
|
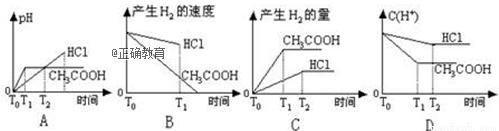
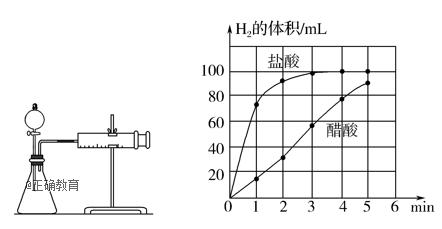
在体积都为1L,pH都等于2的盐酸和醋酸溶液中,投入0.65g锌粒,则下图所示比较符合客观事实的是( )
|
|
| 4. | 详细信息 |
|
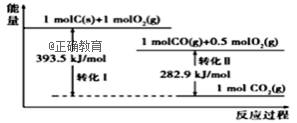
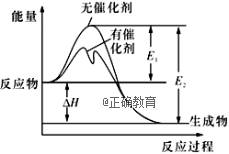
根据如下能量关系示意图,下列说法正确的是( )
A. 1 mol C(g)与1 mol O2(g)的能量之和为393.5 kJ B. 反应2CO(g)+O2(g) ==2CO2(g)中,生成物的总能量大于反应物的总能量 C. 由C→CO的热化学方程式为:2C(s)+O2(g) ==2CO(g) ΔH= −221.2 kJ∙mol−1 D. 热值指一定条件下单位质量的物质完全燃烧所放出热量,则CO热值ΔH= −10.1 kJ∙mol−1
|
|
| 5. | 详细信息 |
|
固态或气态碘分别与氢气反应的热化学方程式如下: ① H2(g) +I2(?) ②H2(g) +I2(?) 下列判断不正确的是( ) A. ①中的I2为气态,②中的I2为固态 B. ②的反应物总能量比①的反应物总能量低 C. 反应①的产物比反应②的产物热稳定性更好 D. lmol固态碘升华时将吸热35.96kJ
|
|
| 6. | 详细信息 |
|
一定温度下,把 2.5 mol A 和 2.5 mol B混合盛入容积为 2 L的密闭容器里,发生如下反应: 3A(g)+B(g) A. x=4 B. 达到平衡状态时 A 的物质的量浓度为 c(A)=1.0 mol·L-1 C. 5s 内 B的反应速率 v(B)=0.05 mol·L-1·s-1 D. 达到平衡状态时容器内气体的压强与起始时压强比为 6:5
|
|
| 7. | 详细信息 |
|
向某密闭容器中加入 0.3 mol A、0.1 mol C 和一定量的 B 三种气体, 一定条件下发生如下反应: 3A(g)
A. 若 t1=15 s,则用 A 的浓度变化表示 t0~t1阶段的平均反应速率为 0.004 mol·L-1·s-1 B. t1时该反应达到平衡,A的转化率为 60% C. 该容器的容积为2 L,B的起始的物质的量为 0.02 mol D. t0~t1 阶段,此过程中容器与外界的热交换总量为 a kJ,该反应的热化学方程式为 3A(g)
|
|
| 8. | 详细信息 |
|
2SO2(g)+O2(g) A. 该反应的逆反应为吸热反应,升高温度可提高活化分子的百分数 B. 500℃、101kPa下,将1molSO2(g)和0.5molO2(g)置于密闭容器中充分反应生成SO3(g)放热akJ,其热化学方程式为2SO2(g)+O2(g) C. 该反应中,反应物的总键能小于生成物的总键能 D. ΔH=E1-E2,使用催化剂改变活化能,但不改变反应热
|
|
| 9. | 详细信息 |
|
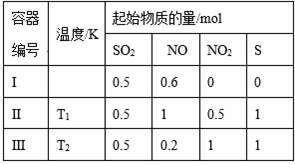
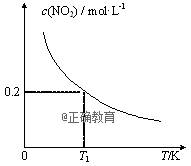
在3个体积均为1 L的恒容密闭容器中发生反应:SO2(g)+2NO(g)
A. 该反应的ΔH>0 B. T1时,该反应的平衡常数为1/16 C. 容器Ⅰ与容器Ⅱ均在T1时达到平衡,总压强之比大于1:2 D. 若T2<T1,达到平衡时,容器Ⅲ中NO的体积分数大于40%
|
|
| 10. | 详细信息 |
|
我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程,该历程示意图如下所示。
下列说法不正确的是( ) A. 生成CH3COOH总反应的原子利用率为100% B. CH4→CH3COOH过程中,有C—H键发生断裂 C. ①→②放出能量并形成了C—C键 D. 该催化剂可有效提高反应物的平衡转化率
|
|
| 11. | 详细信息 |
|
下列有关平衡常数的说法中,正确的是 ( ) A. 改变条件,反应物的转化率增大,平衡常数也一定增大 B. 反应2NO2(g) C. 对于给定可逆反应,温度一定时,其正、逆反应的平衡常数相等 D. CO2+H2
|
|
| 12. | 详细信息 |
|
下列说法错误的有( ) ①化学反应除了生成新物质外,还伴随着能量的变化 ②放热反应不需要加热就能发生 ③需要加热才能发生的反应都是吸热反应 ④化学反应放热还是吸热决定于生成物具有的总能量和反应物具有的总能量的大小 ⑤热化学方程式应注明反应时的温度与压强,如没注明则表示常温常压时的反应 ⑥等量的氢气和氧气分别完全燃烧生成气态水和液态水,前者放出的热量多 ⑦H2(g)+I2(g) ⑧同温同压下,H2(g)+Cl2(g)==2HCl(g)在光照条件下和点燃条件下的ΔH相同 A. 2项 B. 3项 C. 4项 D. 5项
|
|
| 13. | 详细信息 |
|
下列说法正确的是( ) A.室温下, 1mLPH=1的盐酸与100mLNaOH溶液混合后,溶液的PH=7,则NaOH溶液的PH=11 B. 25℃时,0.1mol • L-1的HA溶液中 C. 25℃时,对于pH相同的弱碱ROH和MOH(前者的电离平衡常数Kb较小),加水稀释后溶液的pH仍相同,则后者稀释的倍数更大 D. 25℃时,BaSO4在水中有沉淀和溶解的平衡:BaSO4(s)
|
|
| 14. | 详细信息 |
|
100℃时,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH=2。下列叙述中不正确的是:( ) A. 此时水的离子积Kw=1×10-14 B. 水电离出的c(H+)=1×10-10mol•L-1 C. 水的电离程度随温度升高而增大 D. c(Na+)=c(SO42-)
|
|
| 15. | 详细信息 |
|
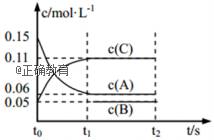
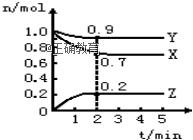
某温度时,在一个2L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:
(1)该反应的化学方程式为___________________________。 (2)反应开始至2min,以气体Z表示的平均反应速率为______________。 (3)平衡时X的转化率为_____________ 。 (4)若X、Y、Z均为气体,2min后反应达到平衡,反应达平衡时:①此时体系内压强与开始时压强之比为________________; ②达平衡时,容器内混合气体的平均相对分子质量比起始投料时____________________(填“增大”“减小”或“相等”)。
|
|
| 16. | 详细信息 |
|
300 ℃时,将2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g) (1)300 ℃时,该反应的平衡常数表达式为:K=___________________。已知K300 ℃<K350 ℃,则ΔH______0(填“>”或“<”)。 (2)在2 min末时,B的平衡浓度为________,D的平均反应速率为________。 (3)若温度不变,缩小容器容积,则A的转化率______(填“增大”“减小”或“不变”),原因是_____________________________________________________________。 (4)如果在相同的条件下,上述反应从逆反应方向进行,开始时加入C、D各
|
|
| 17. | 详细信息 |
|
(1)已知SO2(g)+ 1/2 O2(g) (2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学方程式: Fe2O3(s)+3CO(g)= 2Fe(s)+3CO2(g) △H= ―24.8kJ/mol 3Fe2O3(s)+ CO(g)=2Fe3O4(s)+ CO2(g) △H= ―47.2kJ/mol Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H= +640.5kJ/mol 写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学方程式:_____________________________ (3)在一定条件下,CH4 和CO燃烧的热化学方程式分别为: CH4 ( g ) + 2O2 ( g ) = 2H2O ( l ) + CO2 ( g ) △H = -890 kJ/mol 2CO ( g ) + O2 ( g ) = 2CO2 ( g ) △H = -566 kJ/mol 一定量的CH4和CO的混合气体完全燃烧时,放出的热量为262.9 kJ,生成的CO2用过量的饱和石灰水完全吸收,可得到50 g白色沉淀。求混合气体中CH4 和CO的体积比_____________。
|
|
| 18. | 详细信息 |
|
现有反应mA(g)+nB(g) (1)该反应的逆反应为_____热反应,且m+n___p(填“>”、“<”、或“=”)。 (2)减小压强时,A的质量分数____(填“增大”、“减小”或“不变”)。 (3)若加入B(容器体积不变),则A的转化率______,B的转化率______。 (4)若升高温度,则平衡时B、C的浓度之比c(B)/c(C)将______。 (5)若加入催化剂,平衡时气体混合物的总物质的量_____。 (6)若B是有色物质,A、C均无色,则加入C(容积不变)时混合物颜色________(填变深、变浅或不变,下同),而维持容器内压强不变,充入Ne时,混合物的颜色______。
|
|
| 19. | 详细信息 |
|
砷 (1)写出砷的原子序数______________ (2)工业上常将含砷废渣 (3)已知:
则反应 (4)
①下列可判断反应达到平衡的是 ______
C. ② ③ ④若平衡时溶液pH=14,则该反应的平衡常数K为 ______________
|
|
| 20. | 详细信息 | |||||||||||||||||||||
|
某小组以醋酸为例探究弱酸的性质。 (1)实验一:探究酸的强弱对酸与镁条反应速率的影响。 ①设计实验方案如下表,表中c =________ mol·L-1。
②实验步骤:a)检查装置(下图)的气密性后,添加药品; b)反应开始后,___________________________(填写操作) ; c)将所记录的数据转化为曲线图(右图)。
③写出0~5min醋酸、盐酸与镁条反应的反应速率变化规律:____________。 (2)实验二:现有一瓶醋酸溶液,常温下测定其中醋酸的电离程度(已电离的电解质分子数占原来总分子数的百分比)。 设计实验方案,将待测物理量和对应的测定方法填写在下表中。
|
||||||||||||||||||||||