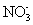2021-2022学年初中化学第九单元练习试题含解析
| 1. | 详细信息 |
|
下列常用调味品中,与水充分混合后不能形成溶液的是 A .砂糖 B .食盐 C .白醋 D .芝麻油 |
|
| 2. | 详细信息 |
|
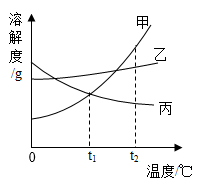
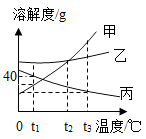
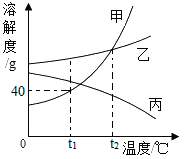
不含结晶水的甲、乙、丙三种固体的溶解度曲线如图所示,下列说法正确的是 A .降低温度一定能使甲从其溶液中结晶出来 B . t 1 ℃ 时,甲、丙两种饱和溶液中溶质质量相等 C . t 2 ℃ 时,向 50g 饱和乙溶液中加入 1g 乙,充分搅拌后溶液质量仍是 50g D .将 t 2 ℃ 时甲、乙、丙的饱和溶液分别降温至 t 1 ℃ ,所得溶液溶质质量分数乙>甲=丙 |
|
| 3. | 详细信息 |
|
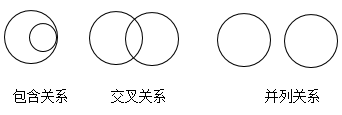
某些化学概念在逻辑上存在如图所示的包含、交叉和并列关系。以下关系界定错误的是 A .金属元素和非金属元素属于并列关系 B .浓溶液和饱和溶液属于交叉关系 C .物理变化和化学变化属于交叉关系 D .太阳能和新能源属于包含关系 |
|
| 4. | 详细信息 |
|
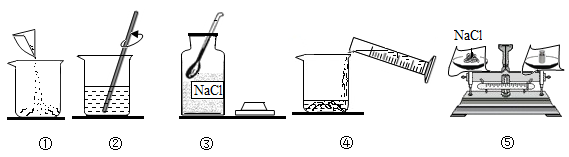
配制 100g 溶质的质量分数为 16% 的 NaCl 溶液。下列说法不正确的是 A .实验操作顺序为 ③⑤①④② B .配制好的溶液倒出 10ml ,剩余溶液浓度变小 C .需称量 NaCl 的质量为 16g D .选用 100ml 量筒量取所需的水 |
|
| 5. | 详细信息 |
|
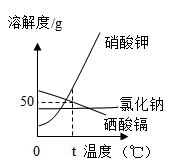
氯化钠、硝酸钾、硒酸镉的溶解度曲线如图所示。下列说法不正确的是 A . t℃ 时,溶解度最小的是氯化钠 B .溶解度变化受温度影响最大的是硝酸钾 C .若要提高 t℃ 时硝酸钾饱和溶液的溶质质量分数,可进行的操作是加入硝酸钾固体 D . t℃ 时,将 25g 硒酸镉加入 50g 水中,完全溶解后,恰好得到该物质的饱和溶液 |
|
| 6. | 详细信息 |
|
某班同学郊游携带了下列 4 种饮品,其中属于溶液的是 A .浓豆浆 B .矿泉水 C .果粒橙 D .鲜牛奶 |
|
| 7. | 详细信息 |
|
下列物质在水中可以形成无色溶液的是 A .冰块 B .植物油 C .氯化铁 D .乙醇 |
|
| 8. | 详细信息 |
|
下列是 “ 小马虎 ” 同学的化学笔记片段,其中正确的是 A . 100g 洁净干燥的空气中,氮气约占 78g ,氧气约占 21g B . 20g 熟石灰加入到 80g 水中,充分搅拌溶解,得到石灰水的质量小于 100g C .在空气中铝制品比铁制品更耐锈蚀,因为铝的化学活动性不如铁强 D . pH=6 的降水呈酸性,属于酸雨 |
|
| 9. | 详细信息 |
|
如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法正确的是 A .甲物质的溶解度大于乙的溶解度 B . t 2 ℃ 时,甲、乙两种物质的溶液浓度相等 C .将 t 3 ℃ 时三种物质的饱和溶液都蒸发 10g 水,析出溶质的质量为甲 > 乙 > 丙 D .当甲中混有少量丙时,可采用蒸发结晶的方法提纯 |
|
| 10. | 详细信息 |
|
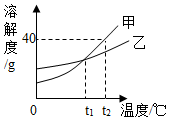
甲、乙的溶解度曲线如图所示。下列有关说法不正确的是 A . t 2 ℃ 时,甲的饱和溶液中溶质和溶剂的质量之比为 2:5 B .等质量的甲、乙的饱和溶液从 t 2 ℃ 降温到 t 1 ℃ ,析出晶体甲大于乙 C . t 1 ℃ 时,甲、乙两种饱和溶液中溶质的质量相等 D .甲、乙的饱和溶液分别从 t 2 ℃ 降温到 t 1 ℃ ,两溶液中溶质质量分数相等 |
|
| 11. | 详细信息 |
|
测得某溶液中仅含有 K + 、 Cu 2+ 、 A . 2n B . 3n C . 6n D . 8n |
|
| 12. | 详细信息 |
|
下列关于溶液的说法正确的是 A .均一、稳定的液体都是溶液 B .饱和溶液降温后都有溶质结晶析出 C .碘酒溶液中,碘是溶质,酒精是溶剂 D .水中加入蔗糖后形成溶液,导电性明显增强 |
|
| 13. | 详细信息 |
|
下列有关溶液的说法错误的是 A .溶液是均一、稳定的混合物 B .溶液中的溶质可以是固体、液体或气体 C .对于同种溶质的溶液来说,在相同条件下,饱和溶液比不饱和溶液浓 D .用汽油和洗涤剂分别洗去衣服上的油污,两者去污原理相同 |
|
| 14. | 详细信息 |
|
溶液在生产、生活中应用广泛。下列有关溶液的说法正确的是 A .溶液一定是混合物 B . 75% 的医用酒精中水是溶质,酒精是溶剂 C .乳化后形成的乳液与溶液同样稳定 D .把 20% 的蔗糖溶液均分成两份,每份溶液的溶质质量分数为 10% |
|
| 15. | 详细信息 |
|
市场上有一种 “ 快速冷冻剂 ” ,主要成分是 Na 2 SO 4 ·10H 2 O 和另一种固体 X 。原理是固体混合后, X 溶解在硫酸钠的结晶水中,迅速降温。 X 可能是下列物质中的 A .硝酸铵 B .氢氧化钠 C .氯化钠 D .生石灰 |
|
| 16. | 详细信息 |
|
将少量下列物质分别放入水中,充分搅拌,可以得到溶液的是 A .植物油 B .白砂糖 C .面粉 D .泥沙 |
|
| 17. | 详细信息 |
|
若要配制 50g 质量分数为 14% 的氯化钠溶液,下列说法错误的是 A .需用托盘天平称取氯化钠固体 7.0g B .选用 200mL 量筒量取所需水的体积 C .用托盘天平称氯化钠固体时,在两盘各放一张质量相等的纸 D .实验中用到的玻璃仪器有烧怀、量筒、胶头滴管、玻璃棒等 |
|
| 18. | 详细信息 |
|
下列有关溶液的说法,正确的是 A .均一、稳定的液体一定是溶液 B .面粉加入水中可形成溶液 C .氢氧化钠固体溶于水,溶液温度升高 D . NaCl 饱和溶液不能再溶解其他物质 |
|
| 19. | 详细信息 |
|
抗击 “ 新冠肺炎 ” 时常用体积分数为 75% 的酒精溶液消毒。下列有关说法错误的是 A .该溶液是混合物 B .该溶液中溶剂是酒精 C .喷洒该溶液时能闻到气味,说明分子在不断运动 D .使用该溶液消毒时,应严禁明火否则易引发火灾 |
|
| 20. | 详细信息 |
|
下列厨房常用的调味品中,与水充分混合不能得到溶液的是 A .白糖 B .食盐 C .白醋 D .花生油 |
|
| 21. | 详细信息 |
|
下列关于 “ 粗盐中难溶性杂质的去除 ” 实验的说法不正确的是 A .实验步骤依次为溶解、过滤、蒸发、计算产率 B .溶解时,若所加粗盐未充分溶解,不会影响精盐的产率 C .过滤时,若所得滤液仍浑浊,应再过滤一次 D .蒸发时,玻璃棒不断搅拌,防止因局部温度过高,造成液滴飞溅 |
|
| 22. | 详细信息 |
|
实验室配制一定量溶质质量分数为 10% 的 FeCl 3 溶液,下列说法正确的是 A .需要用到的玻璃仪器只有二种 B .称量时,若天平指针偏向左端,则所配溶液的溶质质量分数小于 10% C .当溶质完全溶解后,形成稳定的黄色溶液,因为溶液中存在的粒子都是静止的 D .溶质以 Fe 3+ 和 Cl - 存在溶液中,其中一个 Fe 3+ 带三个单位正电荷 |
|
| 23. | 详细信息 |
|
下列有关实验的说法正确的是 A .测定空气里氧气的含量实验中可以用木炭代替红磷进行实验 B .将燃着的木条分别插入空气样品和呼出气体样品中可比较出吸入气体和呼出气体中 CO 2 含量不同 C .在薄铜片上同时加热乒乓球碎片和滤纸碎片可探究燃烧的条件之一:温度要达到可燃物的着火点 D .配制一定质量分数的氯化钠溶液实验中用量筒量取水时,若仰视读数会导致配制的溶液溶质质量分数偏大 |
|
| 24. | 详细信息 |
|
下列说法中正确的是 A .可以用肥皂水鉴别硬水和软水 B .用洗涤剂去油污属于溶解现象 C .溶液一定是无色的,且溶剂一定是水 D .硝酸铵溶于水,放出大量的热 |
|
| 25. | 详细信息 |
|
某金属粉末可能由镁、锌、铁、铝中的一种或几种组成,向 4.8g 该金属粉末样品中加入 100g 一定溶质质量分数的稀硫酸,恰好完全反应,生成 0.4g 氢气。下列说法正确的是 A .样品中可能只含铝和镁 B .充分反应后溶液一定为浅绿色 C .所得溶液中溶质的总质量为 24g D .加入的稀硫酸的溶质质量分数为 9.8% |
|
| 26. | 详细信息 |
|
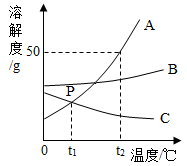
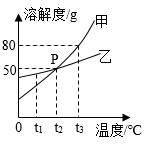
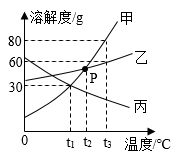
我们在生活和化学实验活动中经常用到水或溶液。 (1) 硬水有害。区分硬水与软水的方法是向水样中滴加适量的 __________ ,家用净水器中的活性炭 _________( 填 “ 能 ” 或 “ 不能 ”) 将硬水软化。 (2) 如图是 A 、 B 、 C 三种固体物质的溶解度曲线,据图做答: ①P 点的意义是 ____________________ 。 ②A 、 B 、 C 三种物质中,溶解度随着温度的上升而减小的物质是 __________ 。 ③t 2 ℃ 时,将 30gA 物质加入到 50g 水中可形成 __________g 溶液,此时溶液是 __________( 填 “ 饱和 ” 或 “ 不饱和 ”) 溶液。 ④ 将 t 2 ℃ 时 A 、 B 、 C 三种物质的饱和溶液均降温至 t 1 ℃ ,所得溶液中溶质质量分数由大到小的顺序是 __________ 。 ⑤A 物质中混有少量的 C 物质,若提纯 A 物质,可采用的结晶方法是 __________ 。 |
|
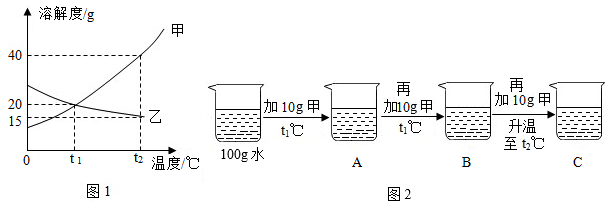
| 27. | 详细信息 |
|
如图 1 为甲、乙两种固体物质的溶解度曲线。 (1) 某同学按图 2 所示进行实验,得到相应温度下的 A 、 B 、 C 溶液,在 A 、 B 、 C 三种溶液中属于饱和溶液的是 _________ (填字母)。向溶液 C 中再加入 25g 甲,充分搅拌,恢复到 t 2 ℃ 时,所得溶液中溶质的质量为 ___________g 。 (2) 将 t 2 ℃ 时等质量的甲、乙两种物质的饱和溶液降温至 t 1 ℃ ,下列说法正确的是 __________ 。 A .降温后,甲溶液的质量大于乙溶液的质量 B .降温前,甲溶液中溶剂的质量比乙溶液中溶剂的质量小 C .降温后,甲溶液的质量分数大于乙溶液的质量分数 D .降温前后乙溶液的质量分数保持不变 |
|
| 28. | 详细信息 |
|
请用化学知识回答下列问题。 (1) 博物馆把贵重的书画保存在充满 N 2 的圆桶中,使用 N 2 的原因是 ______________ 。 (2) 从微观角度解释,变瘪的乒乓球放在热水中又鼓起来的原因是 ______________ 。 (3)“ 釜底抽薪 ” 的灭火原理是 ______________ 。 (4) 喝了汽水后常常会打隔,说明 ______________ 。 |
|
| 29. | 详细信息 |
|
如图是甲、乙两种固体物质的溶解度曲线。 t 1 ℃ 时,配制等质量的甲、乙饱和溶液,所需水的质量甲 ___________ 乙(填 “>”“<” 或 “=” ); t 2 ℃ 时,乙饱和溶液中溶质和溶剂质量比为 ___________ ; t 3 ℃ 时,向 50g 水中加入 50g 甲,所得溶液的质量为 ___________ 。 |
|
| 30. | 详细信息 |
|
如图是甲、乙两种固体的溶解度曲线。甲和乙的溶解度相等时的温度为 _______ ; t 2 ℃ 时,把等质量的甲、乙的饱和溶液降温到 t 1 ℃ ,则溶液中溶质质量分数的关系为甲 _______ 乙 ( 填 “ 大于 ” 、 “ 小于 ” 或 “ 等于 ”) ; t 2 ℃ 时,将 60g 甲的饱和溶液稀释为质量分数为 20% 的溶液,需加水的质量为 ___g 。 |
|
| 31. | 详细信息 | ||||||||
|
抗击新冠肺炎。做好消毒很关键。一些家庭常见消毒液的主要成分如下。
(1)NaClO 中,氯元素的化合价为 _______ 。 (2) 医疗上用体积分数为 75% 的酒精溶液作消毒剂,该酒精溶液的溶剂是 _______ (填物质名称)。 (3) 某同学发现用双氧水清洗伤口时出现泡沫,其原因是 ______ (用化学方程式解释)。 |
|||||||||
| 32. | 详细信息 |
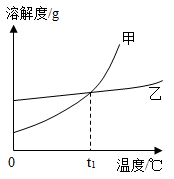
|
已知甲、乙两种固体物质的溶解度曲线如图所示。 (1)t 1 ℃ 时,甲、乙两种物质的溶解度 ___________ (填 “ 相等 ” 或 “ 不相等 ” )。 (2) 两种物质中, ___________ 的溶解度受温度的影响较大。 (3) 要使接近饱和的乙溶液变成饱和溶液,可采用的方法有 ___________ (写一种即可)。 |
|
| 33. | 详细信息 |
|
如图是甲、乙、丙三种固体物质的溶解度曲线图,请回答: (1) 物质的溶解度随温度的升高而减小的是 ______ 。 (2) 甲中有少量乙,除去乙得到甲的方法是 ______ 。 (3)t 1 ℃ 时,向 50g 水中加入 25g 甲,充分溶解后,所形成溶液质量为 ______ 。 (4) 将 t 1 ℃ 时丙的饱和溶液升温到 t 2 ℃ ,观察到的现象 ______ 。 (5)t 2 ℃ 时,甲、乙饱和溶液降温到 t 1 ℃ ,析出晶体的质量关系是 ______ 。(填 “ 甲 > 乙 ” 、 “ 甲 < 乙 ” 、 “ 无法确定 ” ) |
|
| 34. | 详细信息 |
|
如图是甲、乙、丙三种物质的溶解度曲线。请回答下列问题: (1)t 3 ℃ 时,乙的溶解度为 _______ 。 (2)t 1 ℃ 时,将 20g 甲物质溶解到 50g 水中可得到此温度时的 ___ 溶液 ( 填 “ 饱和 ” 或 “ 不饱和 ”) ; (3)t 3 ℃ 时,将丙的饱和溶液降温,丙溶液溶质的质量分数 ___( 填 “ 变大 ” 、 “ 变小 ” 或 “ 不变 ”) 。 |
|
| 35. | 详细信息 |
|
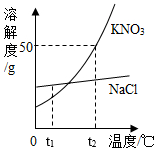
结合 KNO 3 和 NaCl 两种物质的溶解度曲线,回答下列问题。 (1)t 1 ℃ 时两种物质溶解度的大小关系: NaCl ______KNO 3 (填 “ > ” 、 “ = ” 或 “ < ” )。 (2)t 2 ℃ 时将 35g 硝酸钾固体投入 50g 水中,充分搅拌后可得到该温度下的溶液 ____g 。 (3) 若 KNO 3 中混有少量 NaCl ,提纯 KNO 3 可采取的方法是 _______ (填 “ 降温结晶 ” 或 “ 蒸发结晶 ” )。 (4)t 2 ℃ 时将两种物质的饱和溶液各 100g ,分别降温到 t 1 ℃ ,对所得溶液的叙述正确的是 (填字母序号)。 A .溶质质量分数大小关系是: NaCl > KNO 3 B .溶剂质量大小关系是: NaCl > KNO 3 C .溶液质量大小关系是: NaCl > KNO 3 |
|
| 36. | 详细信息 |
|
铁矿石是钢铁生产企业的重要原材料,我国铁矿石储存量世界排名前五。某校科技小组同学为测定本地赤铁矿中氧化铁的质量分数,进行了以下实验: (1) 取 10 g 赤铁矿样品,与足量稀盐酸充分混合 ( 杂质不溶于水,也不与酸反应 ) ,反应结束后过滤,经洗涤、干燥,称得固体质量为 2 g 。该样品中氧化铁的质量分数为 ________ 。 (2) 为测定上述稀盐酸的质量分数,另一小组同学另取 20 g 赤铁矿样品研碎后,向其中不断滴加稀盐酸至装置内剩余固体质量不再变化,此时共消耗 225 g 稀盐酸。请计算该稀盐酸的质量分数 _____ 。 ( 写出计算过程,结果精确到 0.1%) |
|
| 37. | 详细信息 |
|
根据下图所示的实验过程进行计算: (1) 加入的稀硫酸质量为 ______g 。 (2) 计算反应后溶液中的溶质质量分数。(提示: |
|
| 38. | 详细信息 |
|
实验室配制 50g 质量分数为 6% 的氯化钠溶液。 (1) 需要称量氯化钠固体的质量为 ______ 。 (2) 若所配制溶液的溶质质量分数偏大,则可能是用量筒量取所需水时 ______ (填 “ 俯视 ” 或 “ 仰视 ” )所致。 (3) 用已配好的质量分数为 6% 的氯化钠溶液,配制 50g 质量分数 3% 的氯化钠溶液需加水的质量为 ______g 。 |
|
| 39. | 详细信息 |
|
过氧化氢( H 2 O 2 )溶液俗称双氧水,是一种常见的消毒剂。实验员用下列方法制取了少量过氧化氢溶液:在低温下,向 100g 稀硫酸中逐渐加入过氧化钡( BaO 2 ),直到恰好完全反应,可制得 6.8g 过氧化氢。(已知: (1) 反应生成硫酸钡的质量为 ___________g 。 (2) 求稀硫酸中溶质的质量分数。(结果精确到 0.1% ) |
|
| 40. | 详细信息 |
|
某品牌炉具清洁剂的有效成分是氢氧化钠。化学兴趣小组的同学用质量分数为 9.8% 的稀硫酸测定一定量该炉具清洁剂中含有的氢氧化钠的质量。当消耗稀硫酸 200g 时,反应后的溶液呈中性,求该一定量炉具清洁剂中含氢氧化钠的质量是多少?(反应的化学方程式: |
|