2018河北高三下学期人教版高中化学开学考试
| 1. | 详细信息 |
|
下列各组溶液中的各种溶质的物质的量浓度均为0.1 mol/L。①H2S溶液;②KHS溶液;③K2S溶液;④H2S和KHS混合溶液。 下列说法正确的是 A. 溶液pH从大到小的顺序是:③ > ② > ① > ④ B. 在KHS溶液中有:c(H+) + c(K+) = c(OH-) + c(HS-) + c(S2-) C. c(H2S)从大到小的顺序是:① > ④ > ③ > ② D. 在H2S和KHS混合溶液中有:c(H2S) + c(HS-) + c(S2-) = 2c(K+)
|
|
| 2. | 详细信息 |
|
下列实验设计或操作能达到实验目的的是 A. 除去乙酸乙酯中的乙酸:加入乙醇和浓硫酸,共热,使乙酸全部转化为乙酸乙酯 B. 液态溴乙烷中加入NaOH溶液共热几分钟,然后加入足量稀HNO3,再加入AgNO3溶液检验溴乙烷中含溴元素 C. 除去甲苯中的少量苯酚:加浓溴水,振荡、静置、过滤 D. 检验甲酸中是否混有乙醛:可向样品中加入足量稀NaOH溶液中和甲酸后,再做银镜反应实验
|
|
| 3. | 详细信息 |
|
已知H2X为二元弱酸,常温下,0.1 mol/L的NaHX溶液中c(H+) > c(OH-),下列关系中一定正确的是 A. c(Na+) + c(H+) = c(HX-) + 2c(X2-) B. c(H+)·c(OH-) = 10-14 mol2·L-2 C. c(Na+) = c(X2-) + c(HX-) D. 溶液中pH = 1
|
|
| 4. | 详细信息 |
|
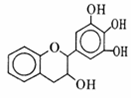
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂。其中没食子儿茶素(EGC)的结构如图所示。关于EGC的下列说法中正确的是
A. 遇FeCl3溶液不发生显色反应 B. 1 mol EGC与4 mol NaOH恰好完全反应 C. 易发生氧化反应和取代反应,难发生加成反应 D. 分子中所有的原子共平面
|
|
| 5. | 详细信息 |
|
用惰性电极电解一定浓度的硫酸铜溶液,长时间通电后,向所得溶液中加入0.2 mol CuO,恰好恢复到电解前的浓度和pH。则电解过程中转移电子的物质的量为 A. 0.2 mol B. 0.4 mol C. 0.6 mol D. 1.0 mol
|
|
| 6. | 详细信息 |
|
在一密闭容器中,可逆反应:aA(g) + bB(g) A. a + b > c B. 平衡向正反应方向移动 C. 物质A的转化率降低 D. 物质C的质量分数增加
|
|
| 7. | 详细信息 |
|
分离下列各组物质,采用的方法正确的是 A. 铝粉中混有铁粉:加氢氧化钠溶液过滤 B. 乙醇和水:分液 C. 氯化钠和氯化铵固体:加热 D. 苯和苯酚:加水后分液
|
|
| 8. | 详细信息 |
|
下列物质的水溶液经加热浓缩、蒸干灼烧仍能得到原物质的是 A. Ca(HCO3)2 B. Na2SO3 C. AlCl3 D. NaAlO2
|
|
| 9. | 详细信息 |
|
X、Y、Z、M、W为五种短周期元素.X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76g/L;W的质子数是X、Y、Z、M四种元素质子数之和的一半。下列说法正确的是( ) A. 原子半径:W>Z>Y>X>M B. 将XZ2通入W单质与水反应后的溶液中,一定只生成碳酸钠 C. 由X、Y、Z、M四种元素形成的化合物中一定有共价键可能有离子键 D. CaX2、CaM2、CaZ2等3种化合物中,阳离子和阴离子个数比均为1:2
|
|
| 10. | 详细信息 |
|
下图是某有机物的球棍模型,下列关于该有机物的性质叙述中错误的是( )
A. 能与NaOH发生反应,也能与盐酸反应 B. 能发生缩聚反应 C. 能发生加成反应 D. 能发生水解反应
|
|
| 11. | 详细信息 |
|
四种短周期元素在周期表中的位置如图,其中只有M为金属元素。下列说法不正确的是( )
A. 原子半径Z<M B. Y的最高价氧化物对应水化物的酸性比X的弱 C. X的最简单气态氢化物的热稳定性比Z的弱 D. Z位于元素周期表中第二周期、第ⅥA族
|
|
| 12. | 详细信息 |
|
将相同物质的量的甲烷和氯气混合后,在光照下充分反应,生成物中物质的量最大的是( ) A. CH3Cl B. CH2Cl2 C. CCl4 D. HCl
|
|
| 13. | 详细信息 |
|
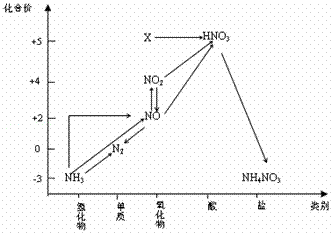
依据图中氮元素及其化合物的转化关系,判断下列说法不正确的是( )
A. X是N2O5 B. 可用排水法收集NO、NO2气体 C. 工业上以NH3、空气、水为原料生产硝酸 D. 由NH3→N2,从原理上看,NH3可与NO2反应实现
|
|
| 14. | 详细信息 |
|
用氧化铝作原料,碳热法冶铝的两步反应为: ①2173~2473K时:2Al2O3+9C ②温度高于2473K时:Al2O3+Al4C3 下列有关说法不正确的是( ) A. A12O3属于两性氧化物 B. 两步反应中CO均是氧化产物 C. Al4C3与盐酸反应可生成烃,该烃为乙烯 D. 生成的铝粉不能在空气中冷却
|
|
| 15. | 详细信息 |
|
在给定条件下,下列选项所示的物质间转化均能实现的是 A. Fe B. S C. CaCO3 D. NH3
|
|
| 16. | 详细信息 |
|
甲烷和一氧化碳的混合气体共2.2g,完全燃烧后生成二氧化碳气体4.4g,则混合气体中甲烷和一氧化碳的质量比为( ) A. 1︰1 B. 4︰7 C. 8︰3 D. 5︰2
|
|
| 17. | 详细信息 |
|
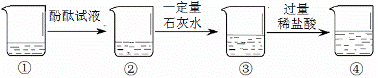
已知①中盛有一定量的碳酸钠溶液, 根据下图所示的实验过程,下列说法正确的是( )
A. ②中溶液为无色 B. ③中溶液的溶质组成有2种情况 C. ④中溶液的溶质除酚酞外,还有3种 D. 加入过量稀盐酸后,③中只观察到沉淀消失,产生大量气泡
|
|
| 18. | 详细信息 |
|
下列各组物质中,所含分子数目不相同的是( )。 A. 同温同压下,相同体积的N2和H2 B. 10 g H2和10 g O2 C. 9 g H2O和0.5 mol Br2 D. 22 g CO2和3.01×1023个N2
|
|
| 19. | 详细信息 |
|
测得某溶液中仅含Na+、Mg2+、SO42—、Cl— 四种离子,其中离子个数比为:N(Na+)︰N(Mg2+)︰N(Cl—) = 4︰5︰8,若设N(Na+)为4a个,则SO42—离子个数为( ) A. 2a B. 3a C. 6a D. 8a
|
|
| 20. | 详细信息 |
|
在反应式:a FeCl2 + b KNO3 + c HCl = d FeCl3 + e KCl + f X + g H2O中,若b=1,d=3,则X的分子式为( ) A. NO B. N2 C. NO2 D. NH4Cl
|
|
| 21. | 详细信息 |
|
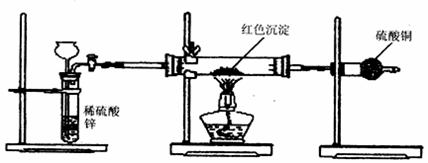
I.回答下列问题: (1)欲量取20.00 mL KMnO4酸性溶液,应选用的仪器是________________。 (2)中和热测定的实验中,用到的玻璃仪器有烧杯、温度计、_____________、___________。 (3)在测定硫酸铜晶体中结晶水含量的实验中,称量操作至少要进行__________次。 II.氢氧化铜是一种常用试剂。例如,利用新制氢氧化铜验证醛类物质的还原性。 (1)新制氢氧化铜悬浊液的配制。实验室制取氢氧化铜悬浊液的操作方法:在试管里加入10%的氢氧化钠溶液2 mL,滴入2%的硫酸铜溶液4~6滴,振荡即成。这样操作的目的是________________________________________________________________________________ 下面是三个研究性学习小组分别从不同层面开展的研究性学习活动: (2)研究性学习小组甲:对教材实验结论“乙醛与新制氢氧化铜反应生成的红色沉淀是Cu2O”提出质疑,他们认为红色沉淀不一定是氧化亚铜。为了确定红色沉淀的成分,开展了如下研究,提出猜想:_______________________________________________。 查阅资料:①氧化亚铜属于碱性氧化物;②+1价的铜离子在酸性条件下易发生自身氧化还原反应,生成+2价的铜离子和单质铜;③在空气中灼烧氧化亚铜生成氧化铜。 设计方案: 方案1:取该红色沉淀溶于足量的稀硝酸中,观察溶液颜色变化。 方案2:取该红色沉淀溶于足量的稀硫酸中,观察是否有残渣。 方案3:称取红色沉淀a g,在空气中充分灼烧至完全变黑,并在干燥器里冷却,再称量,反复多次至固体恒重,称得质量为b g,比较a、b关系。 方案4:取该红色固体沉淀装入试管里,加入酸化的硝酸银溶液,观察是否有银白色银析出。 你认为合理的方案是____________________________。 (3)研究性学习小组乙针对甲的质疑,设计新的探究方案,装置如下图所示。
你认为要测定上述红色沉淀成分必须测定下列哪些物理量(只填序号):________________。 ①通入氢气体积;②反应前,红色沉淀 + 硬质玻璃管的总质量;③完全反应后红色固体 + 硬质玻璃管的总质量;④实验前,干燥管质量;⑤硬质玻璃管质量;⑥锌粒质量;⑦稀硫酸中含溶质的量;⑧实验后,干燥管质量。 (4)研究性学习小组丙上网查阅新闻得知:“2005年诺贝尔化学奖授予了三位研究绿色化学的科学家”。绿色化学强调对环境友好,实现零排放。“变废为宝”符合绿色化学要求。他们收集上述红色沉淀制备化学试剂:蓝矾。请你帮助他们设计一个简单且符合绿色化学要求的实验方案:____________________________________________________________________________。
|
|
| 22. | 详细信息 |
|
有机物A由碳、氢、氧三种元素组成。现取2.3 g A与2.8 L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(假设反应物没有剩余)。将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重2.7 g,碱石灰增重2.2 g。回答下列问题: (1)2.3 g A中所含氢原子、碳原子的物质的量各是___________,_______________。 (2)通过计算确定该有机物的分子式__________________。 (3)若该物质能和钠反应产生氢气,试写出该物质的结构简式______________________。
|
|