2018河南高二上学期人教版高中化学月考试卷
| 1. | 详细信息 |
|
在物质混合、反应等过程中,常会出现“1+1≠2”的现象。而通常情况下,下列各种混合或反应过程中,“1+1”等于“2”的是 A. B. 1mL酒精与1 mL水混合均匀后所得 C. 1g碳酸钠溶液和1g盐酸溶液反应后溶液的总质量 D. 1g酒精和1g水混合后的总质量 |
|
| 2. | 详细信息 |
|
分类是学习和研究化学的一种常用的科学方法。下列分类肯定合理的是 ① 根据酸分子中含有的H原子个数将酸分为一元酸、二元酸等 ② 根据电解质在熔融状态下能否完全电离将电解质分为强电解质和弱电解质 ③ 根据元素原子最外层电子数的多少将元素分为金属和非金属 ④ 根据反应的热效应将化学反应分为放热反应和吸热反应 ⑤ 根据氧化物的组成将所有氧化物分为酸性、碱性和两性氧化物 A. ①③ B. ④ |
|
| 3. | 详细信息 |
|
用NA表示阿伏加德罗常数的值。下列叙述正确的是 A. 23 g钠在氧气中完全燃烧得到电子数为1 NA B. 标准状况下,22.4 L己烷中共价键数目为19NA C. 在常温常压下,32g O3和O2的混合气体中共有2NA个氧原子 D. 6.8g熔融的NaHSO4中含有0.1NA个阳离子 |
|
| 4. | 详细信息 |
|
其他条件不变时只改变下列条件,一定能使反应速率加快的是 ①增加反应物的物质的量 ②升高温度 ③缩小反应容器的体积 ④加入生成物 ⑤加入MnO2 A.全部 B.①②⑤ C.② D.②③ |
|
| 5. | 详细信息 |
|
对处于化学平衡的体系,由化学平衡与化学反应速率的关系可知 A.化学反应速率变化时,化学平衡一定发生移动 B.化学平衡发生移动时,化学反应速率一定变化 C.正反应进行的程度大,正反应速率一定大 D.改变压强,化学反应速率一定改变,平衡一定移动 |
|
| 6. | 详细信息 |
|
下列离子方程式书写正确的是 A.金属钠与水反应: Na + H2O = Na+ + OH- + H2↑ B.用惰性电极电解熔融氯化钠:2Cl- + 2H2O = Cl2↑ + H2↑+ 2OH- C. FeBr2溶液中通入足量的氯气:2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- D.在H2O2中加入酸性高锰酸钾溶液:2MnO4-+ 6H+ + 5H2O2 = 2Mn2+ + 5O2↑+ 8H2O |
|
| 7. | 详细信息 |
|
下列说法不正确的是 A.具有较高能量的反应物分子称为活化分子 B.升高温度增大了活化分子百分数 C.催化剂能够改变化学反应途径 D.增大压强能提高活化分子的浓度 |
|
| 8. | 详细信息 |
|
下列表示物质结构的化学用语或模型正确的是
A.聚丙烯结构简式: B.NaCl的电子式: C.CH4分子比例模型 |
|
| 9. | 详细信息 |
|
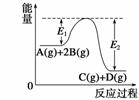
所示,有关叙述正确的是 A.该反应是吸热反应 B.当反应达到平衡时,升高温度,A的转化率增大 C.反应体系中加入催化剂对反应热无影响 D.在反应体系中加入催化剂,反应速率增大,E1减小,E2不变 |
|
| 10. | 详细信息 |
|
下列事实不能用勒夏特列原理解释的是 A.打开汽水瓶时,有大量气泡溢出 B.在配制硫酸亚铁溶液时往往要加入一定量铁粉 C.氨水应密闭保存于低温处 D.实验室用排饱和食盐水的方法收集氯气 |
|
| 11. | 详细信息 |
|
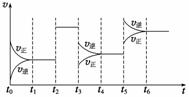
某密闭容器中发生如下反应:X(g)+3Y(g) 的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质 的初始加入量。下列说法中正确的是
A.t2时加入催化剂 B.t3时降低了温度 C.t5时增大了压强 D.t4~t5时间内转化率一定最低 |
|
| 12. | 详细信息 |
|
X、Y、Z三种气体,取X和Y按1∶1的物质的量之比混合,放入密闭容器中发生如下反应:X+2Y A.33% B.40% C.50% D.65% |
|
| 13. | 详细信息 |
|
下列关于反应速率的说法正确的是 A.对于任意化学反应,其他条件不变时,增大压强都一定能加快化学反应速率 B.相同条件下,大小相等的铝片与浓硫酸反应比与稀硫酸反应放出氢气的速率大 C.可逆反应达到化学平衡状态时,正、逆反应的速率相等且都为0 D.反应速率用于衡量化学反应进行的快慢,决定反应速率的主要因素是反应物性质 |
|
| 14. | 详细信息 |
|
可逆反应2NH3 ①单位时间内生成n mol N2的同时生成2n mol NH3 ②单 A.①④⑤ B.②③⑤ C.①③④ D.①②③④⑤ |
|
| 15. | 详细信息 |
|
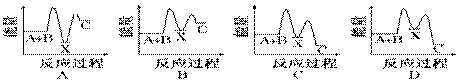
反应A+B→C(ΔH<0)分两步进行:①A+B→X(ΔH>0),②X→C(ΔH<0)。下列示意图中,能正确表示总反应过程中能量变化的是
|
|
| 16. | 详细信息 |
|
相同温度下,已知2H2 (g)+ O2 (g)==2H2O(g) △H1 ; 2H2 (g)+ O2 (g)==2H2O(l) △H2 ; H2 (g) + 1/2 A.△H1=△H2=△H3 B. 2△H3=△H2>△H1 C.△H3>△H2>△H1 D. 2|△H3|=|△H2|>|△H1| |
|
| 17. | 详细信息 |
|
将V1 mL 1.00 mol·L-1 HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。下列叙述正确的是 ( )
A.做该实验时环境温度为22 ℃ B.该实验表明化学能可以转化为热能 C.NaOH溶液的浓度约为1.00 mol·L-1 D.该实验表明有水生成的反应都是放热反应 |
|
| 18. | 详细信息 |
|
航天飞船可用肼(N2H4)和过氧化氢(H2O2)为动力源。已知1 g液态肼和足量液态过氧化氢反应生成氮气和水蒸气时放出20.05 kJ的热量。下列说法中错误的是 ( ) A.该反应中肼作还原剂 B.液态肼的燃烧热为20.05 kJ·mol-1 C.该动力源的突出优点之一是生成物对环境无污染 D.肼和过氧化氢反应的热化学方程式为 N2H4(l)+2H2O2(l)===N2(g)+4H2O(g) ΔH=-641.6 kJ·mol-1 |
|
| 19. | 详细信息 |
|
I (1)在25 ℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ。则表示 甲醇燃烧热的热化学方程式为____________________________________________________。 (2)用NA表示阿伏加德罗常数,在C2H2(气态)完全燃烧生成CO2和液态水的反应中,每有 5NA个电子转移时,放出650 kJ的热量。其热化学方程式为______________________ Ⅱ 发射卫星可用肼(N2H4)为燃料和二氧化氮(NO2)作氧化剂,两者反应生成氮气和气态水。 已知: N2(g)+2O2(g)===2NO2(g) ΔH=+67.7 kJ·mol-1① N2H4(g)+O2(g)===N2(g)+2H2O(g) ΔH=-543 kJ·mol-1②
H2(g)+ (1)肼和二氧化氮反应的热化学方程式为________________________________________ (2)有人认为若用氟气代替二氧化氮作氧化剂,反应释放的能量更大,试写出肼和氟气 反应的热化学方程式:___________________________________________________ |
|
| 20. | 详细信息 |
|
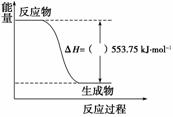
①如图是一定量丙烷完全燃烧生成CO2和1 mol H2O(l) 过程中的能量变化图,请在图中的括号内填入“+”或 “-”。 ②写出表示丙烷燃烧热的热化学方程式: ________________________________________________________________________。 ③二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1 mol 二甲醚完全燃烧生 液态水放出1455 kJ热量。若1 mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1645 kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为________。 (2)碳(s)在氧气供应不足时,生成CO同时还部分生成CO2,因此无法通过实验直接测得 反应:C(s)+ |
|
| 21. | 详细信息 |
|
M、N的物质的量随时间的变化曲线如图所示: (1)此反应的化学方程式中 (2)t1到t2时刻,以M的浓度变化表示的平均反应速率为:_______ (3)平衡时,N的转化率为 。 (4)下列叙述中能说明上述反应达到平衡状态的是 A.反应中M与N的物质的量之比为1︰1 B.混合气体的总质量不随时间的变化而变化 C.混合气体的总物质的量不随时间的变化而变化 D.单位时间内每消耗a mol N,同时生成b mol M E.混合气体的压强不随时间的变化而变化 F.N的质量分数在混合气体中保持不变 Ⅱ、1molN2(g)和1molO2(g)在一定条件下反应生成2molNO(g),吸收180kJ的热量,已 知断裂1molN2(g)中的N≡N和1m 则1molNO分子中的化学键形成时可释放_______kJ的能量。 |
|
| 22. | 详细信息 | |||||||||||||||||||||||||||||||||||||||||||||||||||
|
某实验小组用0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸溶液进行中和热的测定。 Ⅰ.配制0.50 mol·L-1 NaOH溶液 (1)若实验中大约要使用245 mL NaOH溶液,至少需要称量NaOH固体________g。
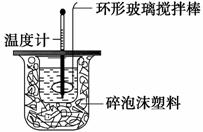
(2)从上图中选择称量NaOH固体所需要的仪器(填字母):__________。 Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如下图所示。
(1)写出该反应的热化学方程式(中和热为57.3 kJ·mol-1): ____________________________________________________________________ (2)取50 mL NaOH溶液和30 mL硫酸溶液进行实验,实验数据如下表。 ①请填写下表中的空白:
②近似认为0.50 mol·L-1 NaOH溶液和0.50 mol·L-1硫酸溶液的密度都是1 g·cm-3, 中和后生成溶液的比热容c=4.18 J·g-1·℃-1。 则中和热ΔH=_______________________(取小数点后一位)。 ③上述实验数值结果与57.3 kJ·mol-1有偏差,产生偏差的原因可能是(填字母)____________。 a.实验装置保温、隔热效果差 b.量取NaOH溶液的体积时仰视读数 c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中 d.用温度计测定NaOH溶液起始温度后直接测定H2SO4溶液的温度 |
||||||||||||||||||||||||||||||||||||||||||||||||||||
| 23. | 详细信息 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
(一)甲同学做浓度对化学反应速率的影响的实验时,将3支试管分别编号为①②③,并按下表中物质的量进行实验,记录下的时间数据是16 s、28 s、33 s。
(1) 实验结论:_____________________________________________________________ (2)写出反应的离子方程式:_________________________________________________ (二)乙同学同样进行了硫代硫酸钠与硫酸反应的有关实验,实验过程的数据记录如下(见表格),请结合表中信息,
(1)根据你所掌握的知识判断,在上述实验中,反应速率最快的可能是______________(填实验序号)。 (2)在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控 制好与实验有关的各项反应条件,其中: ①能说明温度对该反应速率影响的组合是__________(填实验序号 ); ②A和B、A和C的组合比较,所研究的问题是________________________________ ________________________________________________________________________; (3)教材中利用了出现黄色沉淀的快慢来比较反应速率的快慢,请你分析为何不采用 排水法测量单位时间内气体体积的大小进行比较:______________________________。 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 反应
反应