2020人教版初中化学中考真题
| 1. | 详细信息 |
|
实验室加热氯酸钾和二氧化锰的混合物28g制取氧气,完全反应后剩余固体质量为18.4g,请计算: (1)生成氧气的质量_______; (2)原混合物中氯酸钾的质量是多少?(写出过程)
|
|
| 2. | 详细信息 |
|
H2和O2混合气体20 g,点燃反应后生成18 g H2O,则反应前混合气体中,H2最多不超过____g,最少不少于____g。
|
|
| 3. | 详细信息 |
|
写出下列化学方程式 (1)磷在空气中燃烧_______________ (2)铁丝在氧气中燃烧_______________ (3)实验室高锰酸钾制氧气的化学反应_______________ (4)实验室氯酸钾和二氧化锰加热制氧气的化学反应_______________ (5)实验室过氧化氢和二氧化锰制氧气的化学反应__________________
|
|
| 4. | 详细信息 |
|
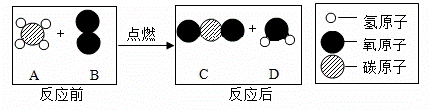
下图是某反应的微观示意图。
请回答: (1)B框中的物质属于___________(填序号:①化合物、②单质、③纯净物、④混合物)。 (2)此反应的化学方程式为____________________,此图说明化学反应前后发生改变的微粒是_________。
|
|
| 5. | 详细信息 |
|
新版《生活饮用水卫生标准》(简称新国标)中水质检测指标从原来的35项增加到106项。对供水各环节的水质提出了相应的要求。 (1)新国标在无机物指标中修订了镉、铅等的限量。这里的镉、铅指的是_____(填序号)。 A 原子 B 分子 C 元素 D 单质 (2)日常生活中,可用_____区分硬水和软水;常用_____的方法将硬水软化。 (3)新国标中消毒剂由1项增至4项,加入了对用臭氧、二氧化氯和氯胺消毒的规定。 ①臭氧(O3)在消毒过程中转化为氧气。臭氧转化为氧气属于_____(填“物理”或者“化学”)变化。 ②氯胺(NH2C1)由_____(填数字)种元素组成。用氯胺消毒时,反应的化学方程式是NH2Cl+X=NH3+HCO,其中X的化学式为_____。
|
|
| 6. | 详细信息 |
|
在化学反应前后,下列各项中①原子的数目,②分子的数目,③原子的种类④物质的组成⑤分子的种类,肯定不会改变的是_________;肯定会改变的是_________;可能改变也可能不变的是__________。
|
|
| 7. | 详细信息 |
|
(1)用化学用语填写下列空白: 2个氢原子____,硝酸根离子____,亚铁离子____,硫酸钠____,氧化铜_____。 (2)写出下列反应的化学方程式: ①电解水:_____________________________________; ②氢气在氧气里燃烧:_______ 。
|
|
| 8. | 详细信息 |
|
在A+B==C+D的反应中,5gA物质跟4gB物质恰好完全反应,生成3gC物质和_____克D物质,这是根据_____定律进行上述计算的。
|
|
| 9. | 详细信息 |
|
在化学反应A+2B===C+D中,5.6 g A和7.3 g B恰好完全反应,生成12.7 g C,同时得到D的质量是( )。 A.0.2 g B.5.6 g C.0.4 g D.0.73 g
|
|
| 10. | 详细信息 |
|
现将10gA和足量B混合加热,A和B发生化学反应,10gA完全反应后生成8gC和4gD,则参加反应的A和B的质量比是( ) A.1:1 B.2:1 C.4:1 D.5:1
|
|
| 11. | 详细信息 |
|
化学方程式是描述化学反应的语言,正确的化学方程式是 ( ) A.S+O2 B.4Fe+3O2 C.2KClO3+MnO2 D.Fe+H2SO4
|
|
| 12. | 详细信息 |
|
化学方程式aC2H2 +bO2 A.15 B.14 C.13 D.10
|
|
| 13. | 详细信息 |
|
根据化学方程式不能获得的信息是: ( ) A.反应中的反应物和生成物 B.各反应物、生成物之间的质量比 C.化学反应速率的快慢程度 D.反应发生所需要的条件
|
|
| 14. | 详细信息 |
|
在反应2CO+O2 A.2:1:2 B.56:32:88 C.28:32:44 D.1:1:2
|
|
| 15. | 详细信息 |
|
现有化学反应X+Y=Z,若将agX与bgY充分混合,在一定条件下发生反应,则关于生成物Z的质量的说法错误的是( ) A.可能等于(a+b)g B.可能小于(a+b)g C.一定大于(a+b)g D.一定小于或等于(a+b)g
|
|
| 16. | 详细信息 |
|
“84消毒剂”是以次氯酸钠为主要有效成分的消毒液。制备次氯酸钠的原理可表示为:2NaOH + Cl2 = NaClO+X+H2O,则X的化学式是( ) A.Na2O
|
|
| 17. | 详细信息 |
|
某有机物燃烧后生成CO2和H2O两种物质,则此有机物的组成是( ) A.只含有碳、氢元素 B.一定含有碳、氢元素,可能含有氧元素 C.一定含有碳、氢、氧元素 D.肯定含有碳、氧元素
|
|
| 18. | 详细信息 |
|
摩托罗拉公司研发了一种由甲醇为原料的新型手机电池,其容量为锂电池的10倍,可连续使用一个月才充一次电,其电池反应原理为: 2CH3OH + 3X + 4NaOH = 2Na2CO3+ 6H2O其中X的化学式为 A.O2 B.CO C.CO2 D.H2
|
|
| 19. | 详细信息 |
|
碱式碳酸铜受热能分解成CuO、CO2和H2O三种物质,请你判断碱式碳酸铜的组成是( ) A.只含有碳、氢、氧元素 B.一定含有碳、氢、铜元素,可能含有氧元素 C.一定含有碳、氢、氧元素,可能含有铜元素 D.肯定含有碳、氢、氧、铜元素
|
|
| 20. | 详细信息 |
|
化学反应遵循质量守恒定律的原因是化学反应前后( ) A.分子的种类没有改变 B.分子的数目没有改变 C.原子的种类、数目和质量都没有改变 D.物质的种类没有改变
|
|
| 21. | 详细信息 |
|
不能用质量守恒定律解释的现象是( ) A.蜡烛燃烧时,越来越短、最后消失 B.铁丝燃烧,其固体质量增加 C.潮湿的衣服在阳光下晒干 D.高锰酸钾受热后,固体质量减少
|
|
| 22. | 详细信息 |
|
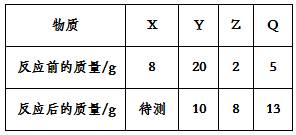
在一密闭容器中,有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
对该反应,下列说法中正确的是( ) A.反应后X的质量为4 g B.该反应为分解反应 C.参加反应的X、Y的质量比是2∶5 D.Y、Q的相对分子质量比一定为5∶4
|
|
| 23. | 详细信息 |
|
我国是世界上第一个在海域成功试采可燃冰的国家,可燃冰主要含有甲烷水合物,用作燃料时 反应的微观示意图如图,下列说法正确的是( )
A.反应前后原子数目不变 B.参加反应的A和B的质量比为1:4 C.反应的化学方程式为CH4+O2
|
|
| 24. | 详细信息 |
|
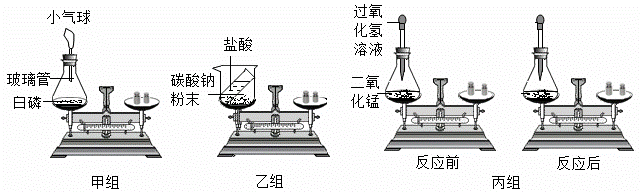
初三某化学兴趣小组同学。依据教材实验对化学反应前后质量变化进行了探究。 (查阅资料)碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳气体。 (实验装置设计)甲、乙、丙小组同学分别设计如图装置:
(讨论与探究)(1)甲小组实验中,白磷燃烧时,在锥形瓶底部加入少量水,其目的是:_____。 (2)请根据乙组和丙组设计的“质量守恒定律”的实验装置进行探究,并按要求完成乙组和丙组。 ①乙组实验结束后可观察到天平_____(是或否)平衡;此反应_____(填“遵守”或“不遵守”)质量守恒定律。 ②丙组过氧化氢溶液分解反应前后各物质质量总和的测定,得出参加化学反应的各物质的质量总和_____(填“大于”、“等于”或“小于”)反应后生成的各物质的质量总和。该反应中二氧化锰起_____作用。 (实验结论)通过甲、乙、丙实验探究,你得到的结论是:_____。 (实验分析)化学反应的过程是_____重新组合的过程,即在一切化学反应中,反应前后原子的_____没有改变,原子的_____没有增减,原子的_____也没有变化,所以化学反应遵守质量守恒定律。 (反思与交流)通过甲、乙、丙小组实验的探究,你得到的启示是:_____。
|
|