2019江苏高二上学期苏教版高中化学期末考试
| 1. | 详细信息 |
|
2018年12月,中共中央、国务院印发了《关于全面推行河长制的意见》,进一步加强水污染治理工作,下列做法不应该提倡的是( ) A.用碱性废水中和酸性废水 B.生活污水无害化处理后用于绿化灌溉 C.将工业废液排入海洋以减少河道污染 D.推广使用高效、低毒农药,减轻水体污染 |
|
| 2. | 详细信息 |
|
下列组合属于同素异形体的是( ) A. C.CH3CH2CH2CH3和(CH3)2CHCH3 D.CH3CH3与CH3CH2CH3 |
|
| 3. | 详细信息 |
|
下列过程属于物理变化的是( ) A.蛋白质的盐析 B.石油裂化 C.钢铁生锈 D.工业制钠 |
|
| 4. | 详细信息 |
|
下列四个氧化还原反应中,水起的作用与其他不相同的是( ) ①Cl2+H2O ②Na+H2O ③NO2+H2O ④Na2O2+H2O A.① B. ② C. ③ D.④ |
|
| 5. | 详细信息 |
|
随着人们生活节奏的加快,方便的小包装食品己被广泛接受。为了延长食品的保质期,防止食品受潮及富脂食品氧化变质,可用适当方法在包装袋中装入( ) A.无水硫酸铜、蔗糖 B.食盐、硫酸亚铁 C.生石灰、硫酸亚铁 D.生石灰、食盐 |
|
| 6. | 详细信息 |
|
下列有关物质的性质与用途具有对应关系的是( ) A. Al2O3可溶于强酸强碱,可用作为耐火材料 B. 硅是良好的半导体,可用作为光导纤维 C.Na2O2具有氧化性,可用作为供氧剂 D.液氨汽化时吸收大量的热,可用作为制冷剂 |
|
| 7. | 详细信息 |
|
下列现象或事实的原因相同的是( ) A.浓硝酸和浓硫酸暴露在空气中浓度降低 B.碳酸氢铵和碘都可以用加热法进行提纯 C.氯水和二氧化硫气体均能使品红溶液褪色 D.硫酸亚铁和亚硫酸钠在空气中久置后均会变质 |
|
| 8. | 详细信息 |
|
下列反应的离子方程式书写正确的是( ) A.向KI溶液中通入少量氯气:Cl2+2I-=2Cl-+I2 B.向AlCl3溶液中滴入少量氨水:Al3++3OH-=Al(OH)3↓ C.向NaHCO3溶液中滴入少量稀硫酸:2H++CO D.向Fe2(SO4)3溶液中加入少量铁粉:Fe3++Fe=2Fe2+ |
|
| 9. | 详细信息 | ||||||||||||||||||||
|
下列实验操作、现象和结论均正确的是( )
|
|||||||||||||||||||||
| 10. | 详细信息 |
|
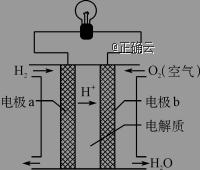
A.该电池工作时化学能转化为电能 B.该电池中电极b是正极,发生还原反应 C.外电路中电流由电极a通过导线流向电极b D.该电池的总反应:2H2+O2=2H2O |
|
| 11. | 详细信息 |
|
对于某些离子的检验及结论一定正确的是( ) A.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,原溶液一定有SO42- B.验证烧碱溶液中是否含有Cl-,先加稀硝酸除去OH-,再加入AgNO3溶液,有白色沉淀, 证明有Cl﹣ C.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,原溶液中一定有CO32- D.加入氯水后,滴加KSCN溶液,溶液变红,原溶液中一定有Fe2+ |
|
| 12. | 详细信息 |
|
下列说法正确的是( ) A.标准状况下,22.4L酒精中含有的分子数为6.02×1023 B.常温常压下,48gO3中含有的分子数为3×6.02×1023 C.1mol·L-1Al2(SO4)3中含有的硫酸根离子数为3×6.02×10 23 D.1molCl2与足量NaOH完全反应,转移电子数为1×6.02×1023 |
|
| 13. | 详细信息 |
|
下列物质转化在一定条件下不能实现的是( ) A.Al2O3→Al(OH)3→Al B.Cu→CuO→CuSO4 C.Na→NaOH→Na2CO3 D.Fe(OH)3→Fe2O3→Fe3+ |
|
| 14. | 详细信息 |
|
有关实验操作,下列说法中正确的是( )
甲 乙 丙 丁 A.甲装置可用于灼烧胆矾,制备无水硫酸铜 B.乙装置可用于分离溴单质与四氯化碳 C.丙装置可用于蒸馏,分离乙醇和水 D.丁装置可用于过滤,分离汽油和水的混合物 |
|
| 15. | 详细信息 |
|
下列由相关实验现象所推出的结论正确的是( ) A.Cl2、SO2均能使品红溶液褪色,说明二者均有氧化性 B.向溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有SO42— C.Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应 D.分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水 |
|
| 16. | 详细信息 |
|
下列反应属于放热反应的是( ) A.C+CO2 C.C+H2O |
|
| 17. | 详细信息 |
|
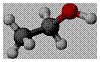
右图是某有机物分子的球棍模型。关于该物质的说法正确的是( )
B.能与氢氧化钠发生取代反应 C.能使紫色石蕊试液变红色 D.能发生催化氧化反应 |
|
| 18. | 详细信息 |
|
下列物质中只含离子键而不含共价键的是( ) A.NH4Cl B.氩气 C.CCl4 D.CaCl2 |
|
| 19. | 详细信息 |
|
钚( A.原子序数为94 B.电子数为94 C.中子数为94 D.质量数为239 |
|
| 20. | 详细信息 |
|
CO和H2在一定条件下可合成甲醇CO(g)+2H2(g) A.CO和H2可全部转化为甲醇 B.降低体系温度能加快反应速率 C.增大CO浓度能加快反应速率 D.使用催化剂不影响反应速率 |
|
| 21. | 详细信息 |
|
X、Y、Z、W为四种短周期主族元素。其中X、Z同族,Y、Z同周期,W与X、Y既不同族也不同周期;X原子最外层电子数是核外电子层数的3倍;Y的最高正价与最低负价的代数和为6。下列说法正确的是( ) A.X与W可以形成W2X、W2X2两种氧化物 B.原子半径由小到大的顺序为:W<X<Z<Y C.Y、Z两元素的气态氢化物中,Z的气态氢化物稳定 D.Y元素最高价氧化物对应水化物的化学式为H2YO4 |
|
| 22. | 详细信息 |
|
足量铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入5mol·L-1氢氧化钠溶液至Cu2+恰好完全沉淀,则消耗NaOH溶液的体积是( ) A.60mL B.45mL C.30mL D.15mL |
|
| 23. | 详细信息 |
|
在含有较多NH4+、Ba2+、NO3-、Cl-的溶液中还能大量共存的离子是( ) A.Ag+ B. Mg2+ C.SO42- D.OH- |
|
| 24. | 详细信息 |
|
A.《化学与生活》 (1)(3分)一年前8月我国自主研制的“海斗”号无人潜水器成功进行万米级下潜应用,这标志着我国研制无人潜水器能力已进入先进国家行列之中。 ①无人潜水器耐压壳使用的是钛铝合金材料。下列不属于钛铝 合金性质的是 ▲ (填字母)。 a.密度大 b.硬度大 c.抗腐蚀 ②无人潜水器通信传输系统中采用PC(聚碳酸酯)及PC合金板材,PC属于 ▲ (填字母)。 a. 金属材料 b. 无机非金属材料 c. 有机高分子材料 ③无人潜水器中的管道通常用塑胶为原料生产。塑胶主要含聚乙烯、聚丙烯、涤纶、聚酯、氯纶、聚氯乙烯等,聚丙烯属于 ▲ 塑料(填“热固性”或“热塑性”)。 (2)(8分)营养平衡,合理用药是保证人体健康和生活质量的重要途径。 ①人体必需从食物中获取多种营养元素和维生素。钙、铁、碘中不属于微量元素的是 ▲ (填元素符号);新鲜蔬菜富含维生素C,蔬菜生吃比熟吃时维生素C的损失小,原因是 ▲ 。 ②人体摄入的油脂、蛋白质,都能在酶的催化作用下发生水解反应。油脂水解的最终产物是高级脂肪酸和 ▲ (填名称);蛋白质完全水解的产物A中一定含有的官能团为-COOH和 a.与氢氧化钠溶液反应 b.发生水解反应 c.发生成肽反应 ③雾霾会刺激呼吸道,使人易患流行性感冒。治疗该病应该给病人服用 ▲ 药品(填字母)。 a.麻黄碱 b.抗酸药 c.阿司匹林 ④Mg2Si3O8·nH2O(三硅酸镁)具有治疗胃酸过多的作用,写出其与胃酸反应生成SiO2·H2O 等物质的化学方程式 ▲ (3) (4分)“十三五”规划纲要明确提出,积极构建智慧能源系统,其中控制传统能源的生产和合理使用尤为重要。 ①往燃煤中加入 ▲ 可减少烟气中的SO2的含量,燃煤产生的SO2用NH3处理可生产多种化工产品。用氨水吸收SO2可制得亚硫酸氢铵(NH4HSO3)写出该反应的化学方程式 ▲ ②天然水中杂质较多,常需要加入明矾,ClO2等物质处理后才能饮用。加入ClO2的作用是 ▲ |
|
| 25. | 详细信息 |
|
有关物质的转化关系如下图所示(部分物质与条件已略去)。其中D、F、G为常见的气体,D为单质,F、G为氧化物,G为棕红色;B为淡黄色固体,X是最常见的液体,Y是常见的金属单质,I溶液为蓝色。
请回答下列问题: (1)B的化学式为 ▲ 。 (2)X的电子式为 ▲ 。 (3)写出反应①的化学方程式: ▲ 。 (4)写出反应②的离子方程式(反应时H为稀溶液): ▲ 。 |
|
| 26. | 详细信息 |
|
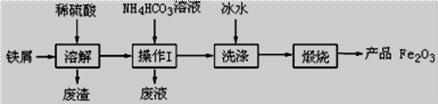
铁红(主要成分为Fe2O3)是一种用途广泛的颜料,用废铁屑制备铁红的流程如下:
(1)操作Ⅰ的名称是 ▲ 。 (2)检验FeCO3沉淀是否洗净的实验方法是 ▲ 。 (3)在空气中煅烧FeCO3的化学方程式是 ▲ 。 (4)称取3.0 g 产品,用稀硫酸溶解,逐滴加入0.10 mol·L-1 KMnO4溶液20.00 mL,二者恰 好反应完全。若此产品中只含有FeO、Fe2O3,求算产品中Fe2O3的质量分数,写出计算 过程。 (已知:10FeSO4+2KMnO4+8H2SO4===5Fe2(SO4)3+2MnSO4+K2SO4+8H2O) |
|