2019江苏高一上学期苏教版高中化学期末考试
| 1. | 详细信息 |
|
食品脱氧剂应无毒、无味、及环境友好。下列可用作食品包装袋中作脱氧剂的是 A.硅胶 B.铁粉 C.CaO D.KMnO4
|
|
| 2. | 详细信息 |
|
为防止缺碘,可在食盐中加入少量KIO3。KIO3属于 A.单质 B.氧化物 C.酸 D.盐
|
|
| 3. | 详细信息 |
|
下列物质属于纯净物的是 A.氨水 B.漂白粉 C.液氯 D.碘酒
|
|
| 4. | 详细信息 |
|
下列过程中,没有发生化学变化的是 A.铝热反应 B.液溴挥发 C.浓硫酸脱水 D.碘化银分解
|
|
| 5. | 详细信息 |
|
下列反应类型中,不可能属于氧化还原反应的是 A.化合反应 B.分解反应 C.置换反应 D.复分解反应
|
|
| 6. | 详细信息 |
|
含有Ba2+、NH A. K+ B.OH- C.SO
|
|
| 7. | 详细信息 |
|
下列有关化学用语表示正确的是 A.O2-的结构示意图: C.中子数为8的碳原子: D.NaOH的电离方程式:NaOH=Na++OH-
|
|
| 8. | 详细信息 |
|
下列试剂的保存正确的是 A.过氧化钠保存在潮湿的环境中 B.保存NaOH的试剂瓶用玻璃塞 C.新制氯水保存在棕色瓶中 D.金属钠保存在CCl4中
|
|
| 9. | 详细信息 |
|
下列关于铝及其化合物的叙述正确的是 A.铝在常温下不会被氧气氧化 B.氧化铝可用于冶炼金属铝 C.氢氧化铝不能与NaOH溶液反应 D.明矾可用于饮用水消毒
|
|
| 10. | 详细信息 |
|
下列有关物质性质与用途具有对应关系的是 A.Al2O3熔点高,可用作耐高温材料 B.FeCl3溶液呈酸性,可用于腐蚀Cu C.铝导热性好,可用铝罐贮运浓硝酸 D.浓硫酸具有强氧化性,可用于干燥CO2
|
|
| 11. | 详细信息 |
|
下列离子方程式中书写正确的是 A.Na2CO3稀溶液中通入少量CO2:CO2+CO B.向氯化铁溶液中加入铁粉:Fe3++Fe=2Fe2+ C.大理石溶于盐酸:CaCO3+2HCl=Ca2++CO2↑+H2O+2Cl- D.铁粉投入稀硝酸:Fe+2H+=Fe2++H2↑
|
|
| 12. | 详细信息 |
|
在给定条件下,下列选项中所示的物质间转化能一步实现的是 A.Fe C.NH3
|
|
| 13. | 详细信息 |
|
下列实验装置原理正确且能达成实验目的的是
A.制SO2 B.分离乙醇和水 C.收集NO2 D.制作喷泉
|
|
| 14. | 详细信息 |
|
下列说法正确的是 A.相同温度时,气体分子间的距离相等 B.2 g H2和2 g O2能恰好反应生成4 g H2O C.3.2 g O3中含有的氧原子数是1.204×1023个 D.1 mol·L−1 MgCl2中含Cl-的数目为1.204×1024个
|
|
| 15. | 详细信息 |
|
下列说法正确的是 A.用加热的方法除去NaCl固体中的NH4Cl B.用丁达尔效应可以鉴别NaCl溶液和KNO3溶液 C.除去粗盐溶液中的Ca2+、Mg2+、SO D.向等浓度、等体积的纯碱和小苏打溶液中分别加入相同的盐酸,反应剧烈的是纯碱
|
|
| 16. | 详细信息 |
|
为测定某铜器表面Cux(OH)yClz(Cu为+2价,x、y、z为正整数)的组成,现进行如下实验:取少量Cux(OH)yClz,将其完全溶解于稀硝酸中,将所得溶液分成两等份。向其中一份滴加足量AgNO3溶液,将所得沉淀过滤、洗涤、干燥,得到固体0.1435 g。向另一份中加入0.1000 mol·L−1 EDTA(已知Cu2+与EDTA反应的化学计量数比为1∶1),恰好完全反应时消耗EDTA 20mL。则Cux(OH)yClz的化学式中y的值为 A.1 B.2 C.3 D.4
|
|
| 17. | 详细信息 |
|
下列物质属于含有共价键的离子化合物的是 A.MgCl2 B.H2O C.Na2SO4 D.N2
|
|
| 18. | 详细信息 |
|
W、Q、X、Y、Z属于周期表中前20号元素,且原子序数依次增大。W元素最外层电子数是次外层的3倍,Q是所在周期中原子半径最大的元素,X是地壳中含量最高的金属元素,Y元素最高化合价与最低化合价之和为4,Z和Q同主族。下列判断正确的是 A.原子半径:r(Q)>r(X)>r(Y)>r(Z) B.简单氢化物的热稳定性:W>Y C.最高价氧化物对应水化物的碱性:Q>X>Z D.Q、Y、Z最高价氧化物对应水化物两两之间均能反应
|
|
| 19. | 详细信息 |
|
下列依据相关实验得出的结论正确的是 A.将SO2通入品红溶液中,红色褪去,说明SO2具有强氧化性 B.向FeCl3溶液中滴加淀粉KI溶液,溶液变蓝,说明氧化性:Fe3+>I2 C.用坩埚钳夹住一小块用砂纸打磨过的铝箔在酒精灯上加热,铝熔化但不滴落,说明Al2O3的熔点高于Al D.向某溶液中滴加BaCl2溶液,再加入稀盐酸,先有白色沉淀,后沉淀不溶解,说明溶液中含有SO
|
|
| 20. | 详细信息 |
|
铅丹(Pb3O4)可作防锈用涂料,其中铅的化合价为+2价和+4价,它与浓盐酸反应的化学方程式为Pb3O4+8HCl(浓)=3PbCl2+Cl2↑+4H2O。下列说法正确的是 A.Pb3O4与浓盐酸反应时,Pb3O4作为还原剂 B.物质的氧化性:Cl2>Pb3O4 C.Pb3O4中+2价的铅与+4价的铅的物质的量之比为2∶1 D.当上述反应中消耗1 mol Pb3O4时,转移电子数为2×6.02×1023
|
|
| 21. | 详细信息 |
|
根据物质所处的类别,以及是否具有氧化性或还原性能帮助我们认识其化学性质。 ⑴请从下列试剂中选择合适的完成指定转化(试剂可以重复选择)。 试剂:盐酸、NaOH溶液、NaCl溶液、Na2SO4溶液、稀硝酸、FeSO4溶液 ①P2O5(一种酸性氧化物)→Na3PO4的离子方程式: ▲ ;
③(NH4)2CO3→Na2CO3的离子方程式: ▲ 。 ⑵根据右图所示物质的转化信息书写相应的反应方程式。 ①“反应Ⅰ”的条件是高温,写出该反应的化学方程式: ▲ ; ②“反应Ⅱ”的条件是1700℃,写出该反应的化学方程式: ▲ 。
|
|
| 22. | 详细信息 |
|
有关物质的转化关系如下图所示,A为常见调味品,B为常见液体,C、E是金属。D、F为气态单质,其中D为黄绿色。J为红褐色固体,A、C、G、I、K的焰色反应均为黄色。K是一种含+6价元素的含氧酸盐,其摩尔质量为166 g·mol-1。
⑴物质B的电子式为 ▲ 。物质D所含元素在周期表中的位置是 ▲ 。 ⑵写出反应②的化学方程式,并用单线桥表示电子转移的方向和数目: ▲ 。 ⑶写出反应④的离子方程式: ▲ 。 ⑷写出反应⑥的化学方程式: ▲ 。
|
|
| 23. | 详细信息 |
|
七铝十二钙(12CaO·7Al2O3)是新型的超导材料和发光材料,用白云石(主要含CaCO3)和铝矿渣(主要含Al2O3和SiO2)制备七铝十二钙的工艺如下:
已知“煅烧Ⅲ”时发生反应为:12CaCO3+7Al2O3 ⑴写出“浸出”过程中CaO与NH4NO3溶液反应的化学方程式: ▲ 。
⑶右图所示装置中可用于实验室吸收NH3的是 ▲ (填字母)。 ⑷溶液X中所含主要溶质的化学式为 ▲ 。 ⑸设计由铝矿渣制取Al(OH)3的方法,并简述过程: ▲ 。
|
|
| 24. | 详细信息 | |||||||||||
|
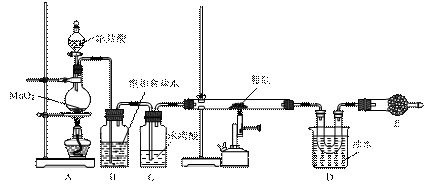
物质 SiCl4 BCl3 沸点/℃ 57.7 12.8 熔点/℃ -70.0 -107.2 已知:①SiCl4遇水易反应;BCl3与SiCl4互溶。 ②高温下硅、硼与氯气反应后所得物质 的部分性质如右表: ⑴装置A中盛装浓盐酸的仪器名称是 ▲ 。 ⑵用湿润的淀粉KI试纸可以检验Cl2,写出表示该反应原理的离子方程式: ▲ 。 ⑶装置B中饱和食盐水的作用是 ▲ 。 ⑷装置D中收集到的物质,可用 ▲ 方法分离出纯净的SiCl4。 ⑸装置E中应装入的试剂名称是 ▲ ,其作用有 ▲ 、 ▲ 。
|
||||||||||||
| 25. | 详细信息 |
|
某兴趣小组利用废旧电池的铜帽(铜锌总含量约99%)制备了CuSO4·5H2O样品,制备流程如下:
⑴“溶解Ⅱ”过程中,发生反应的离子方程式为 ▲ 。 ⑵“溶解Ⅱ”过程中应控制反应温度,温度不能过高的原因是 ▲ 。 ⑶为测定所得CuSO4·5H2O样品的纯度,兴趣小组进行了如下实验:称取2.540g样品,配制成250mL溶液,取25.00mL溶液于锥形瓶中,加入过量KI并充分振荡后,滴加几滴淀粉溶液,再滴入0.0400mol·L-1的Na2S2O3溶液至刚好完全反应,恰好完全反应时消耗Na2S2O3溶液的体积为25.00 mL。实验过程中发生的反应如下: 2Cu2++4I-=2CuI↓+I2 2S2O ①配制250mL溶液所需的玻璃仪器除烧杯、胶头滴管外还有 ▲ 。 ②计算出样品中CuSO4·5H2O的质量分数。(写出计算过程
|
|